Wodorek glinu - Aluminium hydride

|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
Wodorek glinu |
|
|
Systematyczna nazwa IUPAC
Aluman |
|
| Inne nazwy
Alane
Wodorek |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CZEBI | |
| ChemSpider | |
| Karta informacyjna ECHA |
100.029.139 |
| 245 | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| AlH 3 | |
| Masa cząsteczkowa | 29,99 g/mol |
| Wygląd zewnętrzny | białe, krystaliczne ciało stałe, nielotne, wysoce spolimeryzowane, igiełkowate kryształy |
| Gęstość | 1,477 g / cm 3 , stałe |
| Temperatura topnienia | 150 °C (302 °F; 423 K) zaczyna się rozkładać w 105 °C (221 °F) |
| reaguje | |
| Rozpuszczalność | rozpuszczalny w eterze reaguje w etanolu |
| Termochemia | |
|
Pojemność cieplna ( C )
|
40,2 J/mol K |
|
Standardowa
entropia molowa ( S |
30 J/mol K |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-11,4 kJ/mol |
|
Energia swobodna Gibbsa (Δ f G ˚)
|
46,4 kJ/mol |
| Związki pokrewne | |
|
Związki pokrewne
|
Wodorek litowo-glinowy , diboran |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Wodorek glinu (znany również jako alan lub alumane) jest nieorganiczny związek o wzorze Al H 3 . Ma postać białego ciała stałego i może być zabarwiony na szaro ze zmniejszającym się rozmiarem cząstek i poziomami zanieczyszczeń. W zależności od warunków syntezy powierzchnię alanu można pasywować cienką warstwą tlenku i/lub wodorotlenku glinu. Alan i jego pochodne są stosowane jako środki redukujące w syntezie organicznej .
Struktura
Alane to polimer. Stąd jego wzór jest czasami przedstawiany wzorem (AlH 3 ) n . Alan tworzy liczne polimorfy , które są nazywane α-alanami, α'-alanami, β-alanami, γ-alanami, δ-alanami, ε-alanami i ζ-alanami. α-Alan ma morfologię sześcienną lub romboedryczną, podczas gdy α'-alan tworzy kryształy przypominające igły, a γ-alan tworzy wiązkę skondensowanych igieł. Alan jest rozpuszczalny w tetrahydrofuranie (THF) i eterze. Szybkość wytrącania stałego alanu z eteru zmienia się w zależności od metody wytwarzania.
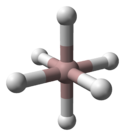
Struktura krystaliczna α-alanu została określona i zawiera atomy glinu otoczone 6 atomami wodoru, które łączą się z 6 innymi atomami glinu. Wszystkie odległości Al-H są równoważne (172pm), a kąt Al-H-Al wynosi 141°.
 |
 |

|
| Komórka elementarna α-AlH 3 | Koordynacja Al | koordynacja H |
α-Alane jest najbardziej stabilnym termicznie polimorfem. β-alan i γ-alan są wytwarzane razem i przekształcają się w α-alan po podgrzaniu. δ, ε i θ-alan są wytwarzane w jeszcze innych warunkach krystalizacji. Chociaż są one mniej stabilne termicznie, polimorfy δ, ε i θ nie przekształcają się w α-alan po podgrzaniu.
Formy molekularne alan
Monomeryczne AlH 3 został wyizolowany w niskiej temperaturze, w postaci stałej, gazu szlachetnego matrycy i wykazano, że jest płaska. Dimer Al 2 H 6 wyizolowano w postaci stałej wodoru. Jest izostrukturalna z diboranem (B 2 H 6 ) i digallanem (Ga 2 H 6 ).
Przygotowanie
Wodorki glinu i ich różne kompleksy są znane od dawna. Jego syntezę pierwszej została opublikowana w 1947 roku, a także patent Syntezę nadawane 1999 Glinowym wytwarza się przez traktowanie wodorku litowo-glinowego z trichlorku glinu . Procedura jest skomplikowana: należy zwrócić uwagę na usunięcie chlorku litu .
- 3 LiAlH 4 + AlCl 3 → 4 AlH 3 + 3 LiCl
Eterowy roztwór alanu wymaga natychmiastowego użycia, ponieważ materiał polimerowy szybko wytrąca się w postaci ciała stałego. Wiadomo, że roztwory wodorku glinu ulegają degradacji po 3 dniach. Wodorek glinu jest bardziej reaktywny niż LiAlH 4 .
Istnieje kilka innych metod otrzymywania wodorku glinu:
- 2 LiAlH 4 + BeCl 2 → 2 AlH 3 + Li 2 BeH 2 Cl 2
- 2 LiAlH 4 + H 2 SO 4 → 2 AlH 3 + Li 2 SO 4 + 2 H 2
- 2 LiAlH 4 + ZnCl 2 → 2 AlH 3 + 2 LiCl + ZnH 2
- 2 LiAlH 4 + I 2 → 2 AlH 3 + 2 LiI + H 2
Synteza elektrochemiczna
Kilka grup wykazało, że alan można wytwarzać elektrochemicznie . Opatentowano różne elektrochemiczne metody produkcji alanu. Alan generujący elektrochemicznie zapobiega zanieczyszczeniom chlorkami. Omówiono dwa możliwe mechanizmy powstawania alanu w ogniwie elektrochemicznym Clasena zawierającym THF jako rozpuszczalnik, wodorek glinowo-sodowy jako elektrolit, anodę aluminiową i drut żelazny (Fe) zanurzony w rtęci (Hg) jako katodę. Sód tworzy amalgamat z katodą Hg zapobiegającą reakcjom ubocznym, a wodór wytworzony w pierwszej reakcji może zostać wychwycony i ponownie przereagowany z amalgamatem sodowo-rtęciowym w celu wytworzenia wodorku sodu. System Clasen nie powoduje strat materiału wyjściowego. Dla anod nierozpuszczalnych zachodzi reakcja 1, natomiast dla anod rozpuszczalnych oczekuje się rozpuszczenia anodowego zgodnie z reakcją 2:
- AlH 4 − - e − → AlH 3 · nTHF + 1 ⁄ 2 H 2
- 3AlH 4 − + Al - 3e − → 4AlH 3 · nTHF
W reakcji 2 anoda aluminiowa jest zużywana, co ogranicza wytwarzanie wodorku glinu dla danego ogniwa elektrochemicznego.
Wykazano krystalizację i odzyskiwanie wodorku glinu z elektrochemicznie wytworzonego alanu.
Uwodornienie pod wysokim ciśnieniem aluminium metalicznego
α-AlH 3 można wytworzyć przez uwodornienie metalicznego glinu przy 10GPa i 600 ° C (1112 ° F). Reakcja między skroplonym wodoru wytwarza α-ALH 3 , które mogą być odzyskiwane w warunkach otoczenia.
Reakcje
Tworzenie adduktów z zasadami Lewisa
AlH 3 łatwo tworzy addycyjnych z silnymi zasadami Lewisa . Na przykład, z trimetyloaminą tworzą się zarówno kompleksy 1:1, jak i 1:2 . Kompleks 1:1 jest tetraedryczny w fazie gazowej, ale w fazie stałej jest dimeryczny z mostkowymi centrami wodorowymi (NMe 3 Al(μ-H)) 2 . Kompleks 1:2 przyjmuje dwupiramidową strukturę trygonalną . Niektóre związki addycyjne (np dimetyloetyloaminy alan, NMe 2 Et · AlH 3 ) termicznie ulegać rozkładowi aluminiowej i może mieć zastosowanie w MOCVD zastosowań.
Jego kompleks z eterem dietylowym tworzy się zgodnie z następującą stechiometrią:
- AlH 3 + (C 2 H 5 ) 2 O → H 3 Al · O (C 2 H 5 ) 2
Reakcja z wodorkiem litu w eterze daje wodorek litowo-glinowy :
- AlH 3 + LiH → LiAlH 4
Redukcja grup funkcyjnych
W chemii organicznej wodorek glinu stosowany jest głównie do redukcji grup funkcyjnych. Pod wieloma względami reaktywność wodorku glinu jest podobna do reaktywności wodorku litowo-glinowego . Wodorek glinu zredukuje aldehydy , ketony , kwasy karboksylowe , bezwodniki , chlorki kwasowe , estry i laktony do odpowiadających im alkoholi . Amidy , nitryle i oksymy są redukowane do odpowiednich amin .
Pod względem selektywności grup funkcyjnych alan różni się od innych odczynników wodorkowych. Na przykład, w poniższej redukcji cykloheksanonem, wodorek litowo-glinowy daje stosunek trans:cis 1,9:1, podczas gdy wodorek glinu daje stosunek trans:cis 7,3:1.
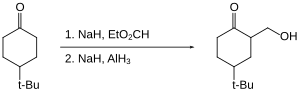
Alane umożliwia hydroksymetylację niektórych ketonów (czyli zastąpienie CH przez C-CH 2 OH w pozycji alfa ). Sam keton nie jest redukowany, ponieważ jest „chroniony” jako jego enolan.
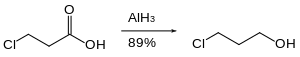
Organohalogenki są redukowane powoli lub wcale przez wodorek glinu. Dlatego reaktywne grupy funkcyjne, takie jak kwasy karboksylowe, można zredukować w obecności halogenków.
Grupy nitrowe nie są redukowane przez wodorek glinu. Podobnie, wodorek glinu może przeprowadzić redukcję estru w obecności grup nitrowych.
Wodorek glinu może być stosowany do redukcji acetali do w połowie zabezpieczonych dioli.
Wodorek glinu może być również stosowany w reakcji otwierania pierścienia epoksydowego, jak pokazano poniżej.
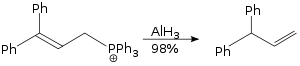
Allilowy reakcję przegrupowania prowadzi się przy użyciu wodorku glinu stanowi S N 2 reakcji, nie jest przestrzennie wymagającego.
Wodorek glinu redukuje nawet dwutlenek węgla do metanu podczas ogrzewania:
- 4 AlH 3 + 3 CO 2 → 3 CH 4 + 2 Al 2 O 3
Hydroaluminacja
Wykazano, że wodorek glinu dodaje się do alkoholi propargilowych . Stosowany razem z tetrachlorkiem tytanu , wodorek glinu może tworzyć wiązania podwójne . Podobną reakcją jest hydroborowanie .
Paliwo
W swojej pasywowanej formie Alane jest aktywnym kandydatem do przechowywania wodoru i może być wykorzystywany do wydajnego wytwarzania energii za pomocą ogniw paliwowych, w tym ogniw paliwowych i pojazdów elektrycznych oraz innych lekkich zastosowań energetycznych. AlH 3 zawiera do 10% wodoru wagowo, co odpowiada 148 g H 2 / l, lub dwa razy gęstość wodoru ciekłego H 2 . W swojej niepasywowanej postaci alan jest również obiecującym dodatkiem do paliwa rakietowego , zdolnym do zwiększenia wydajności impulsu nawet o 10%.
Środki ostrożności
Alane nie jest samozapalny. Powinien być traktowany podobnie jak inne złożone środki redukujące wodorki metali, takie jak wodorek litowo-glinowy. Alane ulegnie rozkładowi w powietrzu i wodzie, chociaż pasywacja znacznie zmniejsza szybkość rozkładu. Pasywowanemu alanowi przypisuje się generalnie klasę zagrożenia 4,3 (chemikalia, które w kontakcie z wodą wydzielają gazy palne).
Bibliografia
Zewnętrzne linki
- Wodorek glinu w bazie danych chemicznych EnvironmentalChemistry.com
- Magazyn wodoru z Brookhaven National Laboratory
- Trójwodorek glinu na WebElements