Tetratlenek antymonu - Antimony tetroxide
 |
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
tlenek antymonu (III, V)
|
|
| Identyfikatory | |
| Karta informacyjna ECHA |
100.014.161 |
|
PubChem CID
|
|
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
| Nieruchomości | |
| SbO 2 ; Sb 2 O 4 | |
| Masa cząsteczkowa | 153,7588; 307,5176 g / mol |
| Wygląd | białe ciało stałe |
| Gęstość | 6,64 g / cm 3 (forma rombowa) |
| Temperatura topnienia | > 930 ° C (1710 ° F; 1200 K) (rozkłada się) |
| Temperatura wrzenia | rozkłada się |
| nierozpuszczalny | |
|
Współczynnik załamania ( n D )
|
2.0 |
| Struktura | |
| rombowe | |
| Zagrożenia | |
| NFPA 704 (ognisty diament) | |
| NIOSH (limity narażenia zdrowotnego w USA): | |
|
PEL (dopuszczalny)
|
TWA 0,5 mg / m 3 (jako Sb) |
|
REL (zalecane)
|
TWA 0,5 mg / m 3 (jako Sb) |
| Związki pokrewne | |
|
Związki pokrewne
|
Trójtlenek antymonu Pentatlenek antymonu |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Tetratlenek antymonu jest związkiem nieorganicznym o wzorze Sb 2 O 4 . Ten materiał, który występuje jako mineralny cerwantyt, jest biały, ale po podgrzaniu żółknie odwracalnie. Materiał o wzorze empirycznym SbO 2 nazywany jest czterotlenkiem antymonu, co oznacza obecność dwóch rodzajów centrów Sb.
Formacja i struktura
Materiał tworzy się, gdy Sb 2 O 3 jest ogrzewany w powietrzu:
- Sb 2 O 3 + 0,5 O 2 → Sb 2 O 4 ΔH = −187 kJ / mol
W 800 ° C tlenek antymonu (V) traci tlen, dając ten sam materiał:
- Sb 2 O 5 → Sb 2 O 4 + 0,5 O 2 ΔH = −64 kJ / mol
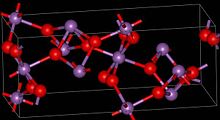
Materiał jest mieszaną wartościowością, zawierającą zarówno centra Sb (V), jak i Sb (III). Znane są dwa polimorfy , jeden rombowy (pokazany w infobox) i jeden jednoskośny. Obie formy mają ośmiościenne centra Sb (V) ułożone w arkusze ze zniekształconymi centrami Sb (III) związanymi z czterema tlenkami.
Bibliografia
- ^ a b Amador, J .; Puebla, E. Gutierrez; Monge, MA; Rasines, I .; Valero, C. Ruiz (1988). „Diantymony Tetraoxides Revisited”. Chemia nieorganiczna . 27 : 1367–1370. doi : 10.1021 / ic00281a011 .
- ^ a b Kieszonkowy przewodnik NIOSH po zagrożeniach chemicznych. „# 0036” . Narodowy Instytut Bezpieczeństwa i Higieny Pracy (NIOSH).
- ^ „Cervantite” . Webminerals . Źródło 2009-06-06 .
- ^ Holleman, AF; Wiberg, E. „Inorganic Chemistry” Academic Press: San Diego, 2001. ISBN 0-12-352651-5 .

