Tribromek antymonu - Antimony tribromide
|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
tribromostiban
|
|
| Inne nazwy
Bromek antymonu (III)
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.029.254 |
| Numer WE | |
|
PubChem CID
|
|
| Numer RTECS | |
| UNII | |
| Numer ONZ | 1549 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| SbBr 3 | |
| Masa cząsteczkowa | 361,472 g / mol |
| Wygląd | kryształy bezbarwne do żółtych, higroskopijne |
| Gęstość | 4,35 g / cm 3 |
| Temperatura topnienia | 96,6 ° C (205,9 ° F, 369,8 K) |
| Temperatura wrzenia | 288 ° C (550 ° F, 561 K) |
| rozpuszczalna, częściowa hydroliza | |
| Rozpuszczalność | rozpuszczalny w rozcieńczonym HCl , HBr , CS 2 , acetonie , benzenie , chloroformie , amoniaku , alkoholu |
| -115,0 · 10-6 cm 3 / mol | |
|
Współczynnik załamania ( n D )
|
1.74 |
| 2,47 D | |
| Struktura | |
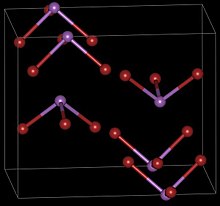
| Orthorhombic , oP16 , SpaceGroup = Pnma, nr 62 (forma β) | |
| Termochemia | |
|
Pojemność cieplna ( C )
|
96 J / mol K |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-259 kJ / mol |
| Zagrożenia | |
| Piktogramy GHS |
 
|
| Hasło ostrzegawcze GHS | Ostrzeżenie |
| H302 , H332 , H411 | |
| P261 , P264 , P270 , P271 , P273 , P301 + 312 , P304 + 312 , P304 + 340 , P312 , P330 , P391 , P501 | |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
7000 mg / kg |
| NIOSH (limity narażenia zdrowotnego w USA): | |
|
PEL (dopuszczalny)
|
TWA 0,5 mg / m 3 (jako Sb) |
|
REL (zalecane)
|
TWA 0,5 mg / m 3 (jako Sb) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Tribromek antymonu ( Sb Br 3 ) to związek chemiczny zawierający antymon na +3 stopniu utlenienia.
Produkcja
Można go wytworzyć w reakcji antymonu z bromem pierwiastkowym lub w reakcji trójtlenku antymonu z kwasem bromowodorowym .
Alternatywnie można go wytworzyć przez działanie bromu na mieszaninę siarczku antymonu i trójtlenku antymonu w temperaturze 250 ° C.
Używa
Można go dodawać do polimerów, takich jak polietylen, jako środek zmniejszający palność . Wykorzystywany jest również do produkcji innych związków antymonu, w analizach chemicznych, jako zaprawa oraz do barwienia.
Właściwości chemiczne
Tribromek antymonu ma dwie formy krystaliczne, obie mające symetrie rombowe . Gdy ciepły roztwór dwusiarczku węgla SbBr 3 jest gwałtownie schładzany, krystalizuje on do postaci przypominającej igłę α-SbBr 3 , która następnie powoli przekształca się w bardziej stabilną formę β.
Tribromek antymonu hydrolizuje w wodzie, tworząc kwas bromowodorowy i trójtlenek antymonu:
- 2 SbBr 3 + 3 H 2 O → Sb 2 O 3 + 6 HBr
Bibliografia
- ^ a b Kieszonkowy przewodnik NIOSH po zagrożeniach chemicznych. „# 0036” . Narodowy Instytut Bezpieczeństwa i Higieny Pracy (NIOSH).
- ^ Yang, YP; DG Brewer; JES Venart (1991). „Badanie synergistycznego działania tlenku antymonu w ognioodpornym polietylenie”. Ogień i materiały . 15 : 37–42. doi : 10.1002 / fam.810150107 .
- ^ „Tribromek antymonu” http://cameochemicals.noaa.gov/chemical/2501
- ^ Okuda, Tsutomu; Terao, Hiromitsu; Ege, Osamu; Negita, Hisao (1970). „Badania strukturalne tribromku antymonu i jego kompleksu molekularnego z benzenem za pomocą jądrowego rezonansu kwadrupolowego 81Br” . Biuletyn Towarzystwa Chemicznego Japonii . 43 (8): 2398. doi : 10.1246 / bcsj.43.2398 .
