Trójchlorek antymonu - Antimony trichloride

|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Trójchlorek antymonu |
|||
|
Systematyczna nazwa IUPAC
Trichlorostyban |
|||
| Inne nazwy
Chlorek antymonu(III), Masło antymonu, Chlorek antymonu, Chlorek Stibous, Trichlorostybina
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| CZEBI | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.030.031 |
||
| Numer WE | |||
| KEGG | |||
| Siatka | Antymon + trójchlorek | ||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS | |||
| UNII | |||
| Numer ONZ | 1733 | ||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| Ćw 3 Sb | |||
| Masa cząsteczkowa | 228,11 g·mol -1 | ||
| Wygląd | Bezbarwne ciało stałe, bardzo higroskopijne | ||
| Zapach | Ostry, ostry | ||
| Gęstość | 3,14 g / cm 3 (25 ° C) 2,51 g / cm 3 (150 ° C) |
||
| Temperatura topnienia | 73,4°C (164,1°F; 346,5 K) | ||
| Temperatura wrzenia | 223,5 ° C (434,3 ° F; 496,6 K) | ||
| 601,1 g/100 ml (0°C) 985,1 g/100 ml (25°C) 1,357 kg/100 ml (40°C) |
|||
| Rozpuszczalność | Rozpuszczalny w acetonie , etanolu , CH 2 Cl 2 , fenylach , eterze , dioksanie , CS 2 , CCl 4 , CHCl 3 , cykloheksanie , tlenochlorku selenu(IV) Nierozpuszczalny w pirydynie , chinolinie , zasadach organicznych |
||
| Rozpuszczalność w kwasie octowym | 143,9 g/100 g (0°C) 205,8 g/100 g (10 °C) 440,5 g/100 g (25°C) 693,7 g/100 g (45°C) |
||
| Rozpuszczalność w acetonie | 537,6 g/100 g (18°C) | ||
| Rozpuszczalność w chlorku benzoilu | 139,2 g/100 g (15 °C) 169,5 g/100 g (25 °C) 2,76 kg/100 g (70 °C) |
||
| Rozpuszczalność w kwasie solnym | 20 °C: 8,954 g/g (4,63% w/w) 8 576 g/g (14,4% w/w) 7,898 g/g (36,7% w/w) |
||
| Rozpuszczalność w p-Cymene | 69,5 g/100 g (-3,5 °C) 85,5 g/100 g (10 °C) 150 g/100 g (30 °C) 2,17 kg/100 g (70 °C) |
||
| Ciśnienie pary | 13,33 Pa (18,1 °C) 0,15 kPa (50 °C) 2,6 kPa (100 °C) |
||
| -86,7 x 10 -6 cm 3 / mol | |||
|
Współczynnik załamania ( n D )
|
1,46 | ||
| Struktura | |||
| rombowy | |||
| 3,93 D (20 °C) | |||
| Termochemia | |||
|
Pojemność cieplna ( C )
|
183,3 J/mol·K | ||
|
Standardowa
entropia molowa ( S |
110,5 J/mol·K | ||
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-381,2 kJ/mol | ||
|
Energia swobodna Gibbsa (Δ f G ˚)
|
-322,5 kJ/mol | ||
| Zagrożenia | |||
| Arkusz danych dotyczących bezpieczeństwa | ICSC 1224 | ||
| Piktogramy GHS |
 
|
||
| Hasło ostrzegawcze GHS | Niebezpieczeństwo | ||
| H314 , H411 | |||
| P273 , P280 , P305+351+338 , P310 | |||
| NFPA 704 (ognisty diament) | |||
| Temperatura zapłonu | Nie palne | ||
| Dawka lub stężenie śmiertelne (LD, LC): | |||
|
LD 50 ( mediana dawki )
|
525 mg/kg (doustnie, szczur) | ||
| NIOSH (limity ekspozycji dla zdrowia w USA): | |||
|
PEL (dopuszczalne)
|
TWA 0,5 mg/m 3 (jako Sb) | ||
|
REL (zalecane)
|
TWA 0,5 mg/m 3 (jako Sb) | ||
| Związki pokrewne | |||
|
Inne aniony
|
Trifluorek antymonu Tribromek antymonu Trijodek antymonu |
||
|
Inne kationy
|
Trichlorek azotu Trichlorek fosforu Trichlorek arsenu Chlorek bizmutu |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
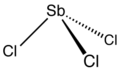
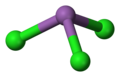
Trójchlorek antymonu jest związek chemiczny o wzorze SBCL 3 . Jest to miękkie bezbarwne ciało stałe o ostrym zapachu, znane alchemikom jako masło antymonu .
Przygotowanie
Trójchlorek antymonu otrzymuje się przez reakcję chloru z antymonem , antymonu, trójbromek , trójtlenku antymonu lub antymonu trisiarczkową . Można go również wytworzyć działając na trójtlenek antymonu stężonym kwasem solnym .
Reakcje
SbCl 3 łatwo ulega hydrolizie, a próbki SbCl 3 należy chronić przed wilgocią. Przy ograniczonej ilości wody tworzy tlenochlorek antymonu uwalniając chlorowodór :
- SBCL 3 + H 2 O → SbOCl + 2 HCI
Z większą ilością wody tworzy Sb
4O
5Cl
2który po podgrzaniu do 460° pod argonem zamienia się w Sb
8O
11Cl
12.
SbCl 3 łatwo tworzy kompleksy z halogenkami, ale stechiometrie nie są dobrym przewodnikiem po składzie, na przykład (C
5H
5NH)SbCl
4zawiera anion łańcucha ze zniekształconą oktaedrą Sb III . Podobnie sól (C
4H
9NH
3)
2SbCl
5zawiera polimeryczny anion o składzie [SbCl2-
5]
nieze zniekształconym oktaedrycznym Sb III .
Z ligandami donorowymi azotu, L, tworzą się kompleksy ze stereochemicznie aktywną samotną parą, na przykład Ψ-trygonalny bipiramidalny LSbCl 3 i Ψ-oktaedryczny L
2SbCl
3.
SBCL 3 ma tylko słabą zasadą Lewisa, ale niektóre kompleksy są znane na przykład kompleksy karbonylowe , Fe (CO)
3(SbCl
3)
2i Ni(CO)
3SbCl
3.
Struktura
W fazie gazowej SBCL 3 jest ostrosłupa o kącie Cl SBCL 97,2 ° i długości wiązania 233 pm. W SbCl 3 każdy Sb ma trzy atomy Cl o godzinie 234 pm, co wskazuje na trwałość jednostki molekularnej SbCl 3 , jednakże istnieje jeszcze pięć sąsiednich atomów Cl, dwa o 346 pm, jeden o 361 pm i dwa o 374 pm. Te osiem atomów można uznać za tworzące dwukołkowy pryzmat trygonalny. Odległości te mogą być skontrastowane z BiCl 3 , który ma trzy najbliższymi sąsiadami przy 250 pm, z dwoma w 324 pm, a trzy średnio po 336 godz. Należy tutaj zauważyć, że wszystkich ośmiu bliskich sąsiadów Bi jest bliżej niż ośmiu najbliższych sąsiadów Sb, co wskazuje na tendencję Bi do przyjmowania wyższych liczb koordynacyjnych.
Zastosowania
SbCl 3 to odczynnik do wykrywania witaminy A i pokrewnych karotenoidów w teście Carr-Price . Trójchlorek antymonu reaguje z karotenoidem, tworząc niebieski kompleks, który można zmierzyć kolorymetrycznie .
Trichlorek antymonu był również używany jako środek do zafałszowania w celu wzmocnienia efektu louche w absyncie . Był używany w przeszłości do rozpuszczania i usuwania rogów z cieląt bez konieczności ich odcinania.
Jest również stosowany jako katalizator reakcji polimeryzacji, hydrokrakingu i chlorowania; jako zaprawa ; oraz w produkcji innych soli antymonu. Jego roztwór jest używany jako odczynnik analityczny dla chloralu, aromatów i witaminy A . Ma bardzo potencjalne zastosowanie jako katalizator kwasu Lewisa w syntetycznej transformacji organicznej.
Dobrym przewodnikiem jest roztwór trichlorku antymonu w ciekłym siarkowodorze , chociaż jego zastosowania są ograniczone przez bardzo niską temperaturę lub wysokie ciśnienie wymagane, aby siarkowodór był ciekły.
Odniesienia w kulturze popularnej
W 12 odcinku trzeciego sezonu popularnego brytyjskiego programu All Creatures Great and Small (zaadaptowanego z rozdziału szóstego książki All Things Wise and Wonderful ) kilka cieląt zmarło po epizodzie niespecyficznego zapalenia żołądka i jelit , którego przyczyna została później ustalona: być spożycie trójchlorku antymonu obecnego w roztworze używanym do rozpuszczania kikutów rogów.