Arsenat - Arsenate
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Nazwa IUPAC
Arsorate
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| ChemSpider | |||
|
Identyfikator klienta PubChem
|
|||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
|
AsO3− 4 |
|||
| Masa cząsteczkowa | 138,919 | ||
| Kwas sprzężony | kwas arsenowy | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
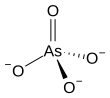
Arsenian jonów jest jako O3−
4. Arsenian (związek) jest dowolny związek , który zawiera ten jon. Arseniany są sole lub estry z kwasem arsenu . Atom arsenu w arsenianu ma wartościowość 5 i jest również znany jako pięciowartościowy arsen lub As(V) . Arsenat pod wieloma względami przypomina fosforan , ponieważ arsen i fosfor występują w tej samej grupie (kolumnie) układu okresowego pierwiastków . Arseniany są umiarkowanymi utleniaczami o potencjale elektrody +0,56 V do redukcji do arseninów .
Występowanie
Arseniany występują naturalnie w różnych minerałach . Minerały te mogą zawierać uwodnione lub bezwodne arseniany. W przeciwieństwie do fosforanów, arseniany nie są tracone z minerału podczas wietrzenia . Przykłady minerałów zawierających arsenian obejmują adamitowego , alarsite , annabergit , erytryn i legrandite . Tam, gdzie do zrównoważenia ładunku w formule potrzebne są dwa jony arsenianowe, nazywa się to diarsenatem, na przykład diarsenianem tricynku, Zn 3 (AsO 4 ) 2 .
Jony
Słowo arsenian pochodzi od kwasu arsenowego , H 3 AsO 4 . Ten umiarkowanie silny kwas przekształca się w arsenian diwodoru ( H
2AsO−
4), arsenian wodoru ( HAsO2-
4) i arsenian ( AsO3−
4), w zależności od pH. Zależność ilościową między tymi gatunkami określają stałe dysocjacji kwasu:
- H 3 AsO 4 + H 2 O ⇌ H
2AsO−
4 + H 3 O + (log K 1 = −2,19) -
h
2AsO−
4 + H 2 O ⇌ HAsO2-
4 + H 3 O + (log K 2 = -6,94) -
HASO2-
4 + H 2 O ⇌ AsO3−
4 + H 3 O + (log K 3 = −11,5)
Wartości te są zbliżone do wartości wodorofosforanów. W roztworze wodnym o pH zbliżonym do obojętnego przeważają arsenian wodoru i arsenian diwodoru.
Zatrucie Arsenatem
Arsenat może zastąpić nieorganiczny fosforan na etapie glikolizy, który wytwarza 1,3-bisfosfoglicerynian z 3-fosforanu aldehydu glicerynowego . Daje to zamiast tego 1-arseno-3-fosfoglicerynian , który jest niestabilny i szybko hydrolizuje, tworząc kolejny produkt pośredni na szlaku, 3-fosfoglicerynian . Dlatego glikoliza postępuje, ale cząsteczka ATP , która byłaby generowana z 1,3-bisfosfoglicerynianu, jest tracona – arsenian jest czynnikiem rozprzęgającym glikolizę, wyjaśniając jego toksyczność.
Podobnie jak w przypadku innych związków arsenu, arsenin wiąże się z kwasem liponowym , hamując konwersję pirogronianu do acetylo-CoA , blokując cykl Krebsa, a tym samym powodując dalszą utratę ATP.