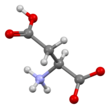
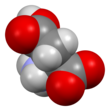
Kwas asparaginowy - Aspartic acid

Szkieletowa formuła kwasu L- asparaginowego
|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
| Nazwa IUPAC | |||
| Inne nazwy | |||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| CZEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.000.265 |
||
| Numer WE | |||
| KEGG | |||
|
Identyfikator klienta PubChem
|
|||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
| Nieruchomości | |||
| C 4 H 7 N O 4 | |||
| Masa cząsteczkowa | 133,103 g·mol -1 | ||
| Wygląd zewnętrzny | bezbarwne kryształy | ||
| Gęstość | 1,7 g / cm 3 | ||
| Temperatura topnienia | 270 ° C (518 ° F; 543 K) | ||
| Temperatura wrzenia | 324 ° C (615 ° F; 597 K) (rozkłada się) | ||
| 4,5 g/l | |||
| Kwasowość (p K a ) | |||
| Podstawa sprzężona | Asparaginian | ||
| -64,2 x 10 -6 cm 3 / mol | |||
| Zagrożenia | |||
| Arkusz danych dotyczących bezpieczeństwa | Zobacz: strona danych | ||
| NFPA 704 (ognisty diament) | |||
| Strona z danymi uzupełniającymi | |||
|
Współczynnik załamania ( n ), stała dielektryczna (ε r ) itp. |
|||
|
Dane termodynamiczne |
Zachowanie fazowe ciało stałe-ciecz-gaz |
||
| UV , IR , NMR , MS | |||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
Kwas asparaginowy (symbol Asp lub D ; forma jonowa znana jest jako asparaginian ) jest α-aminokwasem, który jest wykorzystywany w biosyntezie białek. Jak wszystkie inne aminokwasy zawiera grupę aminową i kwas karboksylowy. Jego grupa α-aminowa znajduje się w protonowanym –NH+
3tworzą się w warunkach fizjologicznych, podczas gdy jego grupa kwasu α-karboksylowego ulega deprotonacji −COO − w warunkach fizjologicznych. Kwas asparaginowy ma kwaśny łańcuch boczny (CH 2 COOH), który reaguje z innymi aminokwasami, enzymami i białkami w organizmie. W warunkach fizjologicznych (pH 7,4) w białkach łańcuch boczny zwykle występuje jako ujemnie naładowana forma asparaginianu, −COO − . Jest nieistotnym aminokwasem u ludzi, co oznacza, że organizm może go syntetyzować w razie potrzeby. Jest kodowany przez kodony GAT i GAC. W mRNA, CUA i CUG.
D- asparaginian jest jednym z dwóch D- aminokwasów powszechnie występujących u ssaków. [3]
W białkach asparaginianowe łańcuchy boczne są często połączone wiązaniami wodorowymi, tworząc skręty asx lub motywy asx , które często występują na końcach N alfa helis .
L izomer Asp jest jednym z 22 tworzących białka aminokwasów , czyli bloków strukturalnych z białkami . Kwas asparaginowy, takie jak kwas glutaminowy , klasyfikuje się jako aminokwas kwasowy o pKa a 3,9, przy czym w peptyd jest wysoce zależna od środowiska lokalnego, a może być tak wysoka, jak 14 Asp jest wszechobecny w biosyntezę.
Odkrycie
Kwas asparaginowy został po raz pierwszy odkryty w 1827 roku przez Augusta-Arthur Plisson i Etienne Ossian Henry przez hydrolizę z asparaginy , które zostały odizolowane od szparagów soku w 1806. dotychczasowej metody stosowane wodorotlenku ołowiu , ale wiele innych kwasów lub zasad, są obecnie powszechnie stosowane zamiast .
Formy i nazewnictwo
Istnieją dwie formy lub enancjomery kwasu asparaginowego. Nazwa „kwas asparaginowy” może odnosić się do enancjomeru lub mieszaniny dwóch. Z tych dwóch form tylko jedna, „ kwas L- asparaginowy”, jest bezpośrednio włączana do białek. Biologiczne role jego odpowiednika, „ kwasu D- asparaginowego” są bardziej ograniczone. Tam, gdzie synteza enzymatyczna da jedną lub drugą, większość syntez chemicznych da obie formy, „ kwas DL- asparaginowy”, znane jako mieszanina racemiczna .
Synteza
Biosynteza
W organizmie ludzkim, asparaginian najczęściej syntetyzowane przez transaminacji z szczawiooctanem . Biosyntezę asparaginianu ułatwia enzym aminotransferaza : przeniesienie grupy aminowej z innej cząsteczki, takiej jak alanina lub glutamina, daje asparaginian i alfa-ketokwas.
Asparaginian odgrywa również ważną rolę w cyklu mocznikowym .
Synteza chemiczna
Przemysłowo asparaginian jest wytwarzany przez aminowanie fumaranu katalizowanego przez amoniak-liazę L- asparaginianową .
Racemiczny kwas asparaginowy może być zsyntetyzowany z dietylowy phthalimidomalonate sodu, (C 6 H 4 (CO) 2 NC (CO 2 Et) 2 ).
Metabolizm
W roślinach i mikroorganizmach asparaginian jest prekursorem kilku aminokwasów, w tym czterech niezbędnych dla człowieka: metioniny , treoniny , izoleucyny i lizyny . Konwersja asparaginianu do tych innych aminokwasów rozpoczyna się od redukcji asparaginianu do jego „semialdehydu”, O 2 CCH (NH 2 )CH 2 CHO. Asparagina pochodzi z asparaginianu poprzez transamidację:
- -O 2 CCH(NH 2 )CH 2 CO 2 - + G C(O)NH 3 + O 2 CCH(NH 2 )CH 2 CONH 3 + + G C(O)O
(gdzie G C (O) NH 2 , a G C (O) OH glutaminy i kwas glutaminowy , odpowiednio)
Udział w cyklu mocznikowym
W cyklu mocznikowym asparaginian i amoniak oddają grupy aminowe prowadząc do powstania mocznika .
Inne role biochemiczne
Asparaginian pełni wiele innych ról biochemicznych. Jest metabolitem w cyklu mocznikowym i uczestniczy w glukoneogenezie . Niesie równoważniki redukujące w przewodzie jabłczan-asparaginian , który wykorzystuje szybką konwersję asparaginianu i szczawiooctanu , który jest utlenioną (odwodornioną) pochodną kwasu jabłkowego . Asparaginian oddaje jeden atom azotu w biosyntezie inozyny , prekursora zasad purynowych . Ponadto kwas asparaginowy działa jako akceptor wodoru w łańcuchu syntazy ATP. Pokarmowy kwas L-asparaginowy został pokazany na działanie jako inhibitor beta-glukuronidaza , które służy do regulacji jelitowo obiegu z bilirubiny i kwasów żółciowych.
Interaktywna mapa ścieżek
Kliknij poniżej geny, białka i metabolity, aby połączyć się z odpowiednimi artykułami.
Neuroprzekaźnik
Asparaginian ( skoniugowana zasada kwasu asparaginowego) stymuluje receptory NMDA , choć nie tak silnie jak neuroprzekaźnik aminokwasów L-glutaminian .
Aplikacje i rynek
W 2014 r. globalny rynek kwasu asparaginowego wynosił 39,3 tys. krótkich ton (35,7 tys. ton ) lub około 117 mln USD rocznie, przy czym potencjalne obszary wzrostu stanowią rynek adresowalny o wartości 8,78 mld USD (Bn). Trzy największe segmenty rynku to Stany Zjednoczone, Europa Zachodnia i Chiny. Obecne zastosowania obejmują biodegradowalne polimery ( kwas poliasparaginowy ), niskokaloryczne słodziki ( aspartam ), inhibitory kamienia i korozji oraz żywice.
Polimery superchłonne
Jednym z obszarów wzrostu rynku kwasu asparaginowego są biodegradowalne superabsorbenty polimerowe (SAP) i hydrożele. Oczekuje się, że rynek superchłonnych polimerów będzie rósł w łącznym rocznym tempie wzrostu wynoszącym 5,5% w latach 2014-2019, aby osiągnąć wartość 8,78 mld USD na całym świecie. Około 75% superchłonnych polimerów jest używanych w jednorazowych pieluchach, a dodatkowe 20% w przypadku nietrzymania moczu dla dorosłych i produktów higieny kobiecej . Kwas poliasparaginowy , produkt polimeryzacji kwasu asparaginowego, jest biodegradowalnym substytutem poliakrylanu . Rynek poliasparaginianu stanowi niewielką część (szac. <1%) całego rynku SAP.
Dodatkowe zastosowania
Oprócz SAP, kwas asparaginowy ma zastosowanie w przemyśle nawozów o wartości 19 miliardów dolarów, gdzie poliasparaginian poprawia retencję wody i pobór azotu; warty 1,1 miliarda dolarów (2020 r.) rynek betonowych powłok do posadzek, gdzie poliasparaginowy jest niskoenergetyczną alternatywą dla tradycyjnych żywic epoksydowych o niskiej zawartości lotnych związków organicznych (VOC); i wreszcie rynek inhibitorów kamienia i korozji o wartości >5 miliardów dolarów.
Źródła
Źródła dietetyczne
Kwas asparaginowy nie jest aminokwasem egzogennym , co oznacza, że może być syntetyzowany z produktów pośrednich centralnego szlaku metabolicznego u człowieka. Jednak kwas asparaginowy znajduje się w:
- Źródła zwierzęce: ostrygi, mielonka, kiełbasa, dziczyzna
- Źródła roślinne: kiełkujące nasiona, płatki owsiane , awokado , szparagi, młoda trzcina cukrowa i melasa z buraków cukrowych .
- Suplementy diety , zarówno sam kwas asparaginowy, jak i sole (takie jak asparaginian magnezu )
- Słodzik aspartam , kwas asparaginowy, fenyloalanina , trimer formaldehydu (marki: NutraSweet, Equal, Canderel itp.)
Zobacz też
Bibliografia
Zewnętrzne linki
- Widmo GMD MS
- Amerykańskie Towarzystwo Chemiczne (21 kwietnia 2010). „Crystal Ewy przodków może wyjaśniać pochodzenie leworęczności życia” . NaukaCodziennie . Zarchiwizowane z oryginału w dniu 23 kwietnia 2010 . Źródło 2010-04-21 .