Chlorek cezu - Caesium chloride

|
|
|
|

|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Chlorek cezu
|
|
| Inne nazwy
Chlorek cezu
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.028.728 |
| Numer WE | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| CsCl | |
| Masa cząsteczkowa | 168,36 g/mol |
| Wygląd zewnętrzny | białe ciało stałe higroskopijne |
| Gęstość | 3,988 g/cm 3 |
| Temperatura topnienia | 646 ° C (1,195 ° F; 919 K) |
| Temperatura wrzenia | 1297 ° C (2367 ° F; 1570 K) |
| 1910 g/l (25°C) | |
| Rozpuszczalność | rozpuszczalny w etanolu |
| Pasmo wzbronione | 8.35 eV (80 K) |
| -56,7 x 10 -6 cm 3 / mol | |
|
Współczynnik załamania ( n D )
|
1,712 (0,3 μm) 1,640 (0,59 μm) 1,631 (0,75 μm) 1,626 (1 μm) 1,616 (5 μm) 1,563 (20 μm) |
| Struktura | |
| CsCl, cP2 | |
| Pm 3 m, nr 221 | |
|
a = 0,4119 nm
|
|
|
Objętość sieci ( V )
|
0,0699 nm 3 |
|
Jednostki wzoru ( Z )
|
1 |
| Sześcienny (Cs + ) Sześcienny (Cl - ) |
|
| Zagrożenia | |
| Piktogramy GHS |
 
|
| Hasło ostrzegawcze GHS | Ostrzeżenie |
| H302 , H341 , H361 , H373 | |
| P201 , P202 , P260 , P264 , P270 , P281 , P301+312 , P308+313 , P314 , P330 , P405 , P501 | |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
2600 mg/kg (doustnie, szczur) |
| Związki pokrewne | |
|
Inne aniony
|
Fluorek cezu Bromek cezu Jodek cezu Astatyd cezu |
|
Inne kationy
|
chlorek litu chlorek sodu chlorek potasu chlorek rubidu chlorek franku |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Chlorek cezu lub chlorek cezu jest związkiem nieorganicznym o wzorze Cs Cl . Ta bezbarwna sól jest ważnym źródłem jonów cezu w różnych niszowych zastosowaniach. Jego struktura krystaliczna tworzy główny typ strukturalny, w którym każdy jon cezu jest koordynowany przez 8 jonów chlorkowych. Chlorek cezu rozpuszcza się w wodzie. CsCl zmienia się w strukturę NaCl podczas ogrzewania. Chlorek cezu występuje naturalnie jako zanieczyszczenia w karnalitu (aż do 0,002%), Sylvit i kainit . Na całym świecie produkuje się rocznie mniej niż 20 ton CsCl, głównie z pollucytu zawierającego cez .
Chlorek cezu jest szeroko stosowaną strukturą medyczną w wirowaniu izopiknicznym do oddzielania różnych typów DNA . Jest odczynnikiem w chemii analitycznej , gdzie służy do identyfikacji jonów na podstawie koloru i morfologii osadu. Po wzbogaceniu w radioizotopy , takie jak 137 CsCl lub 131 CsCl, chlorek cezu jest wykorzystywany w zastosowaniach medycyny nuklearnej , takich jak leczenie raka i diagnostyka zawału mięśnia sercowego . Badano inną formę leczenia raka przy użyciu konwencjonalnego nieradioaktywnego CsCl. Podczas gdy konwencjonalny chlorek cezu ma raczej niską toksyczność dla ludzi i zwierząt, forma radioaktywna łatwo zanieczyszcza środowisko ze względu na wysoką rozpuszczalność CsCl w wodzie. Rozprzestrzenienie się proszku 137 CsCl z 93-gramowego pojemnika w 1987 roku w Goiânia w Brazylii spowodowało jeden z najgorszych w historii wypadków związanych z rozlaniem promieniowania, w którym zginęło cztery osoby i bezpośrednio dotknął 249 osób.
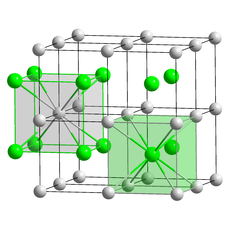
Struktura krystaliczna
Struktura chlorku cezu przyjmuje prymitywną sieć sześcienną o podstawie dwuatomowej, w której oba atomy mają ośmiokrotną koordynację. Atomy chlorku leżą w punktach sieci w rogach sześcianu, podczas gdy atomy cezu leżą w otworach w środku sześcianu; alternatywne i dokładnie równoważne „ustawienie” ma jony cezu w rogach i jon chlorkowy w środku. Struktura ta jest wspólna dla CsBr i CsI oraz wielu binarnych stopów metali . Natomiast inne halogenki alkaliczne mają strukturę chlorku sodu ( soli kamiennej). Gdy oba jony są podobnej wielkości (Cs + promień jonu 174 pm dla tej liczby koordynacyjnej, Cl − 181 pm) przyjmuje się strukturę CsCl, gdy są różne (Na + promień jonu 102 pm, Cl − 181 pm) chlorek sodu struktura została przyjęta. Po podgrzaniu do temperatury powyżej 445 °C normalna struktura chlorku cezu (α-CsCl) przechodzi w formę β-CsCl ze strukturą soli kamiennej ( grupa przestrzenna Fm 3 m ). Strukturę soli kamiennej obserwuje się również w warunkach otoczenia w nanometrowych warstwach CsCl wyhodowanych na podłożach z miki , LiF, KBr i NaCl.
Właściwości fizyczne
Chlorek cezu jest bezbarwny w postaci dużych kryształów i biały po sproszkowaniu. Łatwo rozpuszcza się w wodzie, a maksymalna rozpuszczalność wzrasta od 1865 g/l w 20 °C do 2705 g/l w 100 °C. Kryształy są bardzo higroskopijne i stopniowo rozpadają się w warunkach otoczenia. Chlorek cezu nie tworzy hydratów .
| Т (°C) | 0 | 10 | 20 | 25 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| S (% wag.) | 61,83 | 63,48 | 64,96 | 65,64 | 66,29 | 67,50 | 68,60 | 69,61 | 70,54 | 71,40 | 72,21 | 72,96 |
W przeciwieństwie do chlorku sodu i chlorku potasu, chlorek cezu łatwo rozpuszcza się w stężonym kwasie solnym. Chlorek cezu ma również stosunkowo wysoką rozpuszczalność w kwasie mrówkowym (1077 g/l w 18°C) i hydrazynie ; średnia rozpuszczalność w metanolu (31,7 g/l w 25°C) i niska rozpuszczalność w etanolu (7,6 g/l w 25°C), dwutlenek siarki (2,95 g/l w 25°C), amoniak (3,8 g/l w 0°C), aceton (0,004% w 18°C), acetonitryl (0,083 g/l w 18°C), octany etylu i inne złożone etery , butanon , acetofenon , pirydyna i chlorobenzen .
Pomimo szerokiego pasma zabronionego wynoszącego około 8,35 eV przy 80 K, chlorek cezu słabo przewodzi elektryczność, a przewodność nie jest elektroniczna, ale jonowa . Przewodność ma wartość rzędu 10-7 S/cm w 300°C. Dochodzi do tego poprzez skoki najbliższych sąsiadów wakatów sieci, a mobilność jest znacznie wyższa dla wakatów Cl − niż wakatów Cs + . Przewodność wzrasta wraz z temperaturą do około 450°C, a energia aktywacji zmienia się od 0,6 do 1,3 eV przy około 260°C. Następnie gwałtownie spada o dwa rzędy wielkości z powodu przejścia fazowego z fazy α-CsCl do β-CsCl. Przewodnictwo jest również tłumione przez zastosowanie ciśnienia (około 10-krotny spadek przy 0,4 GPa), co zmniejsza ruchliwość wakatów sieci.
| Stężenie, % wag. |
Gęstość, kg/L |
Stężenie, mol/L |
współczynnik załamania światła (przy 589 nm) |
Obniżenie temperatury zamarzania , °С w stosunku do wody |
Lepkość , 10 -3 Pa·s |
|---|---|---|---|---|---|
| 0,5 | – | 0,030 | 1.3334 | 0,10 | 1.000 |
| 1,0 | 1.0059 | 0,060 | 1.3337 | 0,20 | 0,997 |
| 2,0 | 1,0137 | 0,120 | 1.3345 | 0,40 | 0,992 |
| 3,0 | 0,182 | 1,3353 | 0,61 | 0,988 | |
| 4.0 | 1,0296 | 0,245 | 1,3361 | 0,81 | 0,984 |
| 5.0 | 0,308 | 1.3369 | 1,02 | 0,980 | |
| 6,0 | 1,0461 | 0,373 | 1.3377 | 1,22 | 0,977 |
| 7,0 | 0,438 | 1.3386 | 1,43 | 0,974 | |
| 8,0 | 1.0629 | 0,505 | 1,3394 | 1.64 | 0,971 |
| 9,0 | 0,573 | 1.3403 | 1.85 | 0,969 | |
| 10,0 | 1,0804 | 0,641 | 1.3412 | 2,06 | 0,966 |
| 12,0 | 1,0983 | 0,782 | 1.3430 | 2,51 | 0,961 |
| 14,0 | 1,1168 | 0,928 | 1.3448 | 2,97 | 0,955 |
| 16,0 | 1.1358 | 1,079 | 1.3468 | 3.46 | 0,950 |
| 18,0 | 1.1555 | 1,235 | 1.3487 | 3,96 | 0,945 |
| 20,0 | 1.1758 | 1,397 | 1.3507 | 4,49 | 0,939 |
| 22,0 | 1.1968 | 1,564 | 1.3528 | – | 0,934 |
| 24,0 | 1,2185 | 1,737 | 1,3550 | – | 0,930 |
| 26,0 | 1.917 | 1.3572 | – | 0,926 | |
| 28,0 | 2.103 | 1.3594 | – | 0,924 | |
| 30,0 | 1,2882 | 2.296 | 1.3617 | – | 0,922 |
| 32,0 | 2,497 | 1.3641 | – | 0,922 | |
| 34,0 | 2,705 | 1.3666 | – | 0,924 | |
| 36,0 | 2,921 | 1.3691 | – | 0,926 | |
| 38,0 | 3,146 | 1.3717 | – | 0,930 | |
| 40,0 | 1.4225 | 3.380 | 1.3744 | – | 0,934 |
| 42,0 | 3,624 | 1.3771 | – | 0,940 | |
| 44,0 | 3,877 | 1.3800 | – | 0,947 | |
| 46,0 | 4.142 | 1.3829 | – | 0,956 | |
| 48,0 | 4.418 | 1.3860 | – | 0,967 | |
| 50,0 | 1.5858 | 4,706 | 1.3892 | – | 0,981 |
| 60,0 | 1,7886 | 6,368 | 1.4076 | – | 1.120 |
| 64,0 | 7.163 | 1.4167 | – | 1,238 |
Reakcje
Chlorek cezu całkowicie dysocjuje po rozpuszczeniu w wodzie, a kationy Cs + są solwatowane w rozcieńczonym roztworze. CsCl przekształca się w siarczan cezu po podgrzaniu w stężonym kwasie siarkowym lub podgrzaniu z wodorosiarczanem cezu w temperaturze 550–700 °C:
- 2 CsCl + H 2 SO 4 → Cs 2 SO 4 + 2 HCl
- CsCl + CsHSO 4 → CS 2 SO 4 + HCl
Chlorek cezu tworzy różne sole podwójne z innymi chlorkami. Przykłady obejmują 2CsCl·BaCl 2 , 2CsCl·CuCl 2 , CsCl·2CuCl i CsCl·LiCl oraz ze związkami międzyhalogenowymi :
Występowanie i produkcja
Chlorek cezu występuje naturalnie jako zanieczyszczenie w halogenku minerały karnalit (KMgCl 3 x 6 2 O z aż do 0,002%), CsCI Sylvit (KCI) i kainit (MgSO 4 · KCI · 3H 2 O) wody oraz w minerały. Na przykład woda uzdrowiska Bad Dürkheim , która została użyta do izolacji cezu, zawierała około 0,17 mg/l CsCl. Żaden z tych minerałów nie ma znaczenia komercyjnego.
Na skalę przemysłową CsCl jest produkowany z mineralnego pollucytu , który jest sproszkowany i poddany działaniu kwasu solnego w podwyższonej temperaturze. Ekstrakt traktuje się chlorkiem antymonu , monochlorkiem jodu lub chlorkiem ceru(IV) w celu uzyskania słabo rozpuszczalnej soli podwójnej, np.:
- CsCl + SBCL 3 → CsSbCl 4
Traktowanie soli podwójnej siarkowodorem daje CsCl:
- 2 CsSbCl 4 + 3 H 2 S → 2 CsCl + Sb 2 S 3 + 8 HCl
CsCl o wysokiej czystości jest również wytwarzany z rekrystalizacji (i ) przez rozkład termiczny:
Tylko około 20 ton związków cezu, z dużym udziałem CsCl, było produkowanych rocznie w latach 70. i 2000. na całym świecie. Chlorek cezu wzbogacony cezem-137 do zastosowań w radioterapii jest produkowany w jednym zakładzie Mayak na Uralu w Rosji i jest sprzedawany na arenie międzynarodowej przez dealera w Wielkiej Brytanii. Sól jest syntetyzowana w temperaturze 200 °C ze względu na jej higroskopijny charakter i jest szczelnie zamykana w stalowym pojemniku w kształcie gilzy, który jest następnie zamykany w innej stalowej obudowie. Uszczelnienie jest wymagane, aby chronić sól przed wilgocią.
Metody laboratoryjne
W laboratorium CsCl można otrzymać traktując wodorotlenek cezu , węglan , wodorowęglan cezu lub siarczek cezu kwasem solnym:
- CsOH + HCI → CsCl + H 2 O
- Cs 2 CO 3 + 2 HCl → 2 CsCl + 2 H 2 O + CO 2
Zastosowania
Prekursor Cs metalu
Chlorek cezu jest głównym prekursorem cezu metalicznego przez redukcję w wysokiej temperaturze:
- 2 CsCl (l) + Mg (l) → MgCl 2 (s) + 2 Cs (g)
Podobną reakcję – ogrzewanie CsCl z wapniem w próżni w obecności fosforu – po raz pierwszy opisał w 1905 roku francuski chemik ML Hackspill i nadal jest ona stosowana w przemyśle.
Wodorotlenek cezu otrzymuje się przez elektrolizę wodnego roztworu chlorku cezu:
- 2 CsCl + 2 H 2 O → 2 CsOH + Cl 2 + H 2
Solute do ultrawirowania
Chlorek cezu jest szeroko stosowany w wirowaniu w technice znanej jako wirowanie izopikniczne . Siły dośrodkowe i dyfuzyjne ustalają gradient gęstości, który umożliwia rozdzielanie mieszanin na podstawie ich gęstości cząsteczkowej. Technika ta pozwala na oddzielenie DNA o różnej gęstości (np. fragmenty DNA o różnej zawartości AT lub GC). Zastosowanie to wymaga roztworu o dużej gęstości, a jednocześnie stosunkowo niskiej lepkości, a CsCl jest do niego odpowiedni ze względu na wysoką rozpuszczalność w wodzie, dużą gęstość ze względu na dużą masę Cs oraz niską lepkość i wysoką stabilność roztworów CsCl.
Chemia organiczna
Chlorek cezu jest rzadko stosowany w chemii organicznej. Może działać jako odczynnik katalizatora przeniesienia fazowego w wybranych reakcjach. Jedną z takich reakcji jest synteza pochodnych kwasu glutaminowego
gdzie TBAB oznacza bromek tetrabutyloamoniowy (katalizator międzyfazowy), a CPME oznacza eter cyklopentylowo-metylowy (rozpuszczalnik).
Kolejną reakcją jest zastąpienie tetranitrometanu
gdzie DMF to dimetyloformamid (rozpuszczalnik).
Chemia analityczna
Chlorek cezu jest odczynnikiem w tradycyjnej chemii analitycznej używanym do wykrywania jonów nieorganicznych poprzez kolor i morfologię osadów. Ilościowy pomiar stężenia niektórych z tych jonów, np. Mg 2+ , za pomocą spektrometrii mas z plazmą indukcyjnie sprzężoną , służy do oceny twardości wody.
| Jon | Towarzyszące odczynniki | Pozostałość | Morfologia | Granica wykrywalności (μg) |
|---|---|---|---|---|
| AsO 3 3- | KI | CS 2 [AsI 5 ] lub CS 3 [AsI 6 ] | Czerwone sześciokąty | 0,01 |
| Au 3+ | AgCl , HCl | Cs 2 Ag[AuCl 6 ] | Szaro-czarne krzyże, cztero- i sześcioramienne gwiazdy | 0,01 |
| Au 3+ | NH 4 SCN | Cs[Au(SCN) 4 ] | Igły pomarańczowo-żółte | 0,4 |
| Bi 3+ | KI , HCl | Cs 2 [BiI 5 ] lub 2,5 H 2 O | Czerwone sześciokąty | 0,13 |
| Cu 2+ | (CH 3 COO) 2 Pb, CH 3 COOH, KNO 2 | Cs 2 Pb[Cu(NO 2 ) 6 ] | Małe czarne kostki | 0,01 |
| Za 3+ | — | Cs 3 [InCl 6 ] | Mały ośmiościan | 0,02 |
| [IrCl 6 ] 3- | — | Cs 2 [IrCl 6 ] | Mała ciemnoczerwona ośmiościan | – |
| Mg 2+ | Na 2 HPO 4 | CsMgPO 4 lub 6 H 2 O | Małe czworościany | – |
| Pb 2+ | KI | Cs[PbI 3 ] | Igły żółto-zielone | 0,01 |
| Pd 2+ | NaBr | CS 2 [PdBr 4 ] | Ciemnoczerwone igły i pryzmaty | – |
| [ReCl 4 ] − | — | Cs [RECL 4 ] | Ciemnoczerwone romby, bipiramidy | 0,2 |
| [RECL 6 ] 2- | — | CS 2 [ReCl 6 ] | Mała żółto-zielona ośmiościana | 0,5 |
| ReO 4 − | — | CSReO 4 | Dwupiramidy tetragonalne | 0,13 |
| Rh 3+ | KNO 2 | Cs 3 [Rh(NO 2 ) 6 ] | Żółte kostki | 0,1 |
| Ru 3+ | — | Cs 3 [RuCl 6 ] | Różowe igły | – |
| [RuCI 6 ] 2- | — | Cs 2 [RuCl 6 ] | Małe ciemnoczerwone kryształy | 0,8 |
| Sb 3+ | — | Cs 2 [SbCl 5 ] · n H 2 O | Sześciokąty | 0,16 |
| Sb 3+ | Nai | lub | Czerwone sześciokąty | 0,1 |
| Sn 4+ | — | CS 2 [SnCl 6 ] | Mały ośmiościan | 0,2 |
| TeO 3 3− | HCl | Cs 2 [TeCl 6 ] | Jasnożółty ośmiościan | 0,3 |
| Tl 3+ | Nai | Pomarańczowo-czerwone sześciokąty lub prostokąty | 0,06 |
Służy również do wykrywania następujących jonów:
| Jon | Towarzyszące odczynniki | Wykrycie | Granica wykrywalności (μg/ml) |
|---|---|---|---|
| Al 3+ | K 2 SO 4 | Bezbarwne kryształy tworzą się w neutralnych mediach po odparowaniu | 0,01 |
| Ga 3+ | KHSO 4 | Po podgrzaniu tworzą się bezbarwne kryształy | 0,5 |
| Cr 3+ | KHSO 4 | Jasnofioletowe kryształy wytrącają się w lekko kwaśnym środowisku | 0,06 |
Medycyna
American Cancer Society stwierdza, że „dostępne dowody naukowe nie obsługuje twierdzi, że nieradioaktywne suplementy chlorek cezu mieć żadnego wpływu na nowotwory.” Food and Drug Administration ostrzega o zagrożeniach bezpieczeństwa, w tym znacznej toksyczności serca i śmierci, związanych ze stosowaniem chlorku cezu w medycynie naturopatyczną.
Medycyna nuklearna i radiografia
Chlorek cezu złożony z radioizotopów, takich jak 137 CsCl i 131 CsCl, jest stosowany w medycynie nuklearnej , w tym w leczeniu nowotworów ( brachyterapia ) i diagnostyce zawału mięśnia sercowego . W produkcji źródeł promieniotwórczych normalne jest wybieranie takiej postaci chemicznej izotopu promieniotwórczego, która nie ulegnie łatwemu rozproszeniu w środowisku w razie wypadku. Na przykład generatory radiotermiczne (RTG) często wykorzystują tytanian strontu , który jest nierozpuszczalny w wodzie. Jednak w przypadku źródeł teleterapii gęstość promieniotwórcza ( Ci w danej objętości) musi być bardzo wysoka, co nie jest możliwe w przypadku znanych nierozpuszczalnych związków cezu. Aktywnym źródłem jest pojemnik z radioaktywnym chlorkiem cezu w kształcie gilzy.
Różne zastosowania
Chlorek cezu jest używany do wytwarzania szkieł przewodzących prąd elektryczny i ekranów lamp katodowych. W połączeniu z gazami szlachetnymi CsCl jest stosowany w lampach ekscymerowych i laserach ekscymerowych . Inne zastosowania obejmują aktywację elektrod podczas spawania; produkcja wody mineralnej, piwa i płuczki wiertniczej ; i lutowie wysokotemperaturowe. Wysokiej jakości monokryształy CsCl mają szeroki zakres przezroczystości od UV do podczerwieni i dlatego były stosowane w kuwetach, pryzmatach i okienkach w spektrometrach optycznych; to zastosowanie zostało przerwane wraz z opracowaniem mniej higroskopijnych materiałów.
CsCl jest silnym inhibitorem kanałów HCN, które przenoszą prąd h w pobudliwych komórkach, takich jak neurony. Dlatego może być przydatny w eksperymentach elektrofizjologicznych w neuronauce.
Toksyczność
Chlorek cezu ma niską toksyczność dla ludzi i zwierząt. Jego średnia dawka śmiertelna (LD 50 ) u myszy wynosi 2300 mg na kilogram wagi ciała przy podawaniu doustnym 910 mg / kg wstrzyknięcie dożylne. Łagodna toksyczność CsCl związana jest z jego zdolnością do obniżania stężenia potasu w organizmie i częściowego zastępowania go w procesach biochemicznych. Jednak przyjmowane w dużych ilościach może powodować znaczne zaburzenia równowagi potasu i prowadzić do hipokaliemii , arytmii i ostrego zatrzymania akcji serca . Jednak proszek chlorku cezu może podrażniać błony śluzowe i powodować astmę .
Ze względu na wysoką rozpuszczalność w wodzie chlorek cezu jest wysoce mobilny i może nawet dyfundować przez beton. Jest to wada jego radioaktywnej postaci, która skłania do poszukiwania mniej mobilnych chemicznie materiałów radioizotopowych. Komercyjne źródła radioaktywnego chlorku cezu są dobrze zamknięte w podwójnej stalowej obudowie. Jednak w wypadku Goiânia w Brazylii takie źródło zawierające około 93 gramy 137 CsCl zostało skradzione z opuszczonego szpitala i otwarte przez dwóch padlinożerców. Niebieska poświata emitowana w ciemności przez radioaktywny chlorek cezu przyciągnęła nieświadomych niebezpieczeństw złodziei i ich bliskich i rozsypała proszek. Spowodowało to jeden z najgorszych wypadków związanych z rozlaniem promieniowania, w którym 4 osoby zmarły w ciągu miesiąca od narażenia, 20 wykazywało objawy choroby popromiennej , 249 osób zostało skażonych radioaktywnym chlorkiem cezu, a około tysiąc otrzymało dawkę przekraczającą roczną ilość promieniowanie tła. Ponad 110 000 ludzi przytłoczyło lokalne szpitale, a kilka bloków miejskich musiało zostać zburzonych podczas operacji porządkowych. W pierwszych dniach skażenia dolegliwości żołądkowe i nudności w wyniku choroby popromiennej doświadczyło kilka osób, ale dopiero po kilku dniach jedna osoba skojarzyła objawy z proszkiem i przyniosła próbkę władzom.
Zobacz też
Bibliografia
Bibliografia
- Haynes, William M., wyd. (2011). CRC Handbook of Chemistry and Physics (wyd. 92). Boca Raton, FL: CRC Prasa . Numer ISBN 1-4398-5511-0.
- Lidin, RA; Andreeva, LL; Moloczko VA (2006). Константы неорганических веществ: справочник (Związki nieorganiczne: książka danych) . Moskwa. Numer ISBN 978-5-7107-8085-5.
- Pleszew, WE; Stepin BD (1970). Химия и техtestнология соединений лития, рубидия и цезия(po rosyjsku). Moskwa: Chimija.

![{\ Displaystyle {\ ce {CsCl + ICl3 -> CS[ICl4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6b106856bd4fcba7764e52dc61de8ec0049b4a3e)
![{\displaystyle {\ce {Cs[ICl2]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/179cfcb1c479f90128c3ac48e2906b3f844d8781)
![{\displaystyle {\ce {Cs[ICl4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7ae265895d0004997e064fbc7fa581ef0db7a2c4)
![{\ Displaystyle {\ ce {Cs [ICl2] -> {CsCl} + ICL}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7824fed40e3efe7816a0e91633974ab54eb1aa87)
![{\ Displaystyle \ overbrace {\ ce {CH2 = CHCOOCH3}} ^ {\ tekst {akrylan metylu}} + {\ ce {ArCH = N-CH (CH3)-COOC (CH3) 3-> [{\ ce {TBAB ,\ CsCl,\ K2CO3}}][{\ce {CPME,\ 0^{\circ }C}}]{ArCH=NC(C2H4COOCH3)(CH3)-COOC(CH3)3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5f20c83eb7669c6266c0cc534608d0b13cef0f5a)
![{\ Displaystyle \ overbrace {{\ ce {C (NO2) 4}}} ^ {\ tekst {tetranitrometan}} + {\ ce {CsCl -> [{\ ce {DMF}}] {C (NO2) 3Cl} + CsNO2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ddc9c983cd359a8ffceb4f8aeb9a0aa392b3f0da)
![{\displaystyle {\ce {Cs[SbI4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/78c190f0fcfde2966d052ab2d73b0e938953df43)
![{\displaystyle {\ce {CS2[SbI5]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1eb7ac284505510c341e93e2c1743311fb4e25b6)
![{\displaystyle {\ce {Cs[TlI4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d3c1830f454449a2bcdcf18f352984bf51997de0)