Jodek cezu - Caesium iodide
 Kryształ CSI
|
|
 Kryształ iskrzący CsI
|
|
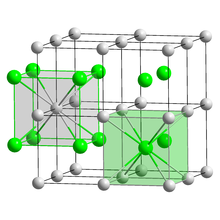 Struktura krystaliczna
|
|

|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Jodek cezu
|
|
| Inne nazwy
Jodek cezu
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.029.223 |
| Numer WE | |
|
PubChem CID
|
|
| Numer RTECS | |
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| CsI | |
| Masa cząsteczkowa | 259,809 g / mol |
| Wygląd | białe krystaliczne ciało stałe |
| Gęstość | 4,51 g / cm 3 |
| Temperatura topnienia | 632 ° C (1170 ° F, 905 K) |
| Temperatura wrzenia | 1280 ° C (2340 ° F; 1550 K) |
| 848 g / l (25 ° C) | |
| -82,6 · 10-6 cm 3 / mol | |
|
Współczynnik załamania ( n D )
|
1,9790 (0,3 µm) 1,7873 (0,59 µm) 1,7694 (0,75 µm) 1,7576 (1 µm) 1,7428 (5 µm) 1,7280 (20 µm) |
| Struktura | |
| CsCl , cP2 | |
| Pm 3 m, nr 221 | |
a = 0,4503 nm
|
|
|
Objętość kraty ( V )
|
0,0913 nm 3 |
|
Jednostki formuły ( Z )
|
1 |
| Sześcienny (Cs + ) Sześcienny (I - ) |
|
| Termochemia | |
|
Pojemność cieplna ( C )
|
52,8 J / mol · K |
|
Entropia trzonowa standardowa ( S |
123,1 J / mol · K |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-346,6 kJ / mol |
|
Energia swobodna Gibbsa (Δ f G ˚)
|
-340,6 kJ / mol |
| Zagrożenia | |
| Piktogramy GHS |
  
|
| Hasło ostrzegawcze GHS | Ostrzeżenie |
| H315 , H317 , H319 , H335 | |
| P201 , P202 , P261 , P264 , P270 , P271 , P272 , P273 , P280 , P281 , P301 + 312 , P302 + 352 , P304 + 340 , P305 + 351 + 338 , P308 + 313 , P312 , P321 , P330 , P332 + 313 , P333 + 313 , P337 + 313 , P362 , P363 , P391 , P403 + 233 | |
| Temperatura zapłonu | Nie palne |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
2386 mg / kg (doustnie, szczur) |
| Związki pokrewne | |
|
Inne aniony
|
Fluorek cezu Chlorek cezu Bromek cezu Astatyd cezu |
|
Inne kationy
|
Jodek litu Jodek sodu Jodek potasu Jodek rubidu Jodek wapnia |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Jodek cezu i jodku cezu ( wzór chemiczny CsI ) jest związek jonowy z cezu i jodu . Jest często używany jako luminofor wejściowy do wzmacniacza obrazu rentgenowskiego znajdującego się w sprzęcie do fluoroskopii . Fotokatody na bazie jodku cezu są bardzo wydajne przy ekstremalnych długościach fal ultrafioletowych.
Synteza i struktura
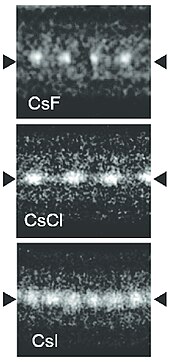
Masowe kryształy jodku cezu mają sześcienną strukturę krystaliczną CsCl, ale rodzaj struktury nanometrycznych warstw CsI zależy od materiału podłoża - jest to CsCl dla miki i NaCl dla LiF, NaBr i NaCl.
Łańcuchy atomowe jodku cezu można hodować w dwuściennych nanorurkach węglowych . W takich łańcuchach atomy I wydają się jaśniejsze niż atomy Cs na zdjęciach z mikroskopu elektronowego, pomimo mniejszej masy. Różnica ta została wyjaśniona różnicą ładunków między atomami Cs (dodatnimi), wewnętrznymi ściankami nanorurek (ujemnymi) i atomami I (ujemnymi). W rezultacie atomy Cs są przyciągane do ścian i wibrują silniej niż I atomy, które są wypychane w kierunku osi nanorurek.
Nieruchomości
| Т (° C) | 0 | 10 | 20 | 25 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| S (% wag.) | 30.9 | 37.2 | 43.2 | 45.9 | 48.6 | 53.3 | 57.3 | 60.7 | 63.6 | 65.9 | 67.7 | 69.2 |
Aplikacje
Ważnym zastosowaniem kryształów jodku cezu , które są scyntylatorami , jest kalorymetria elektromagnetyczna w eksperymentalnej fizyce cząstek . Pure CsI to szybki i gęsty materiał scyntylacyjny o stosunkowo niskiej wydajności świetlnej, która znacznie wzrasta wraz z chłodzeniem. Pokazuje dwa główne składniki emisji: jeden w obszarze bliskiego ultrafioletu przy długości fali 310 nm i jeden przy 460 nm. Wadą CsI jest wysoki gradient temperatury i niewielka higroskopijność .
Jodek cezu jest stosowany jako rozdzielacz wiązki w spektrometrach podczerwieni z transformacją Fouriera (FTIR). Ma szerszy zakres transmisji niż bardziej powszechne rozdzielacze wiązek bromku potasu , działając w dalekiej podczerwieni. Jednak kryształy CsI o jakości optycznej są bardzo miękkie i trudne do rozszczepienia lub wypolerowania. Powinny być również pokryte (zazwyczaj germanem) i przechowywane w eksykatorze, aby zminimalizować interakcję z atmosferycznymi oparami wody.
Oprócz luminoforów wejściowych do wzmacniaczy obrazu jodek cezu jest często stosowany w medycynie jako materiał scyntylacyjny w płaskich detektorach promieniowania rentgenowskiego .
Bibliografia
Cytowane źródła
- Haynes, William M., wyd. (2011). Podręcznik chemii i fizyki CRC (wyd. 92). Boca Raton, FL: CRC Press . ISBN 1439855110 .
