Kwas węglowy - Carbonic acid
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Nazwa IUPAC
Kwas węglowy
|
|||
| Inne nazwy
Kwas
hydroksymrówkowy Kwas hydroksymetanowy Dihydroksykarbonyl |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| CZEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Karta informacyjna ECHA |
100.133.015 |
||
| Numer WE | |||
| 25554 | |||
| KEGG | |||
|
Identyfikator klienta PubChem
|
|||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| H 2 CO 3 | |||
| Temperatura topnienia | -80 ° C (-112 ° F; 193 K) (rozkłada się) | ||
| Podstawa sprzężona | wodorowęglan , węglan | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
W chemii kwas węglowy jest kwasem dwuzasadowym o wzorze chemicznym H 2 CO 3. Czysty związek rozkłada się w temperaturach wyższych niż ca. -80 °C.
W Biochemistry, nazwę „kwas karboksylowy” jest często stosowane do roztworów wodnych w dwutlenku węgla , które odgrywają ważną rolę w wodorowęglanu układu buforowego stosowane w celu utrzymania kwasowo-zasadowej homeostazy .
Równowagi chemiczne
Wartości stałej równowagi
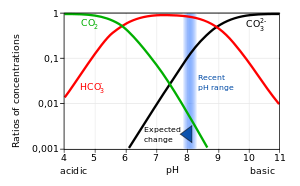
W roztworze wodnym kwas węglowy zachowuje się jak kwas dwuzasadowy. W Bjerrum działka zawiera typowe stężenia w stanie równowagi, w roztworze, w wodzie morskiej , dwutlenku węgla i różnych gatunków pochodzących z niego, w zależności od pH. Zakwaszenie wód naturalnych spowodowane jest rosnącym stężeniem dwutlenku węgla w atmosferze, co jest spowodowane spalaniem coraz większej ilości węgla i węglowodorów .
Oczekiwana zmiana dotyczy przewidywanego efektu dalszego zakwaszania oceanów . Szacuje się, że wzrost rozpuszczonego dwutlenku węgla spowodował spadek średniego pH powierzchni oceanu o około 0,1 w stosunku do poziomu sprzed epoki przemysłowej.
Baza danych stałych stabilności zawiera 136 wpisów z wartościami dla ogólnych stałych protonacji β 1 i β 2 jonu węglanowego. W poniższych wyrażeniach [H + ] przedstawia stężenie w równowadze związku chemicznego H + , itd.
Wartość log β 1 maleje wraz ze wzrostem siły jonowej , . W 25 °C:
- :
- (wybrane dane z bazy danych SC)
Wartość log β 2 również maleje wraz ze wzrostem siły jonowej.
- :
Przy =0 i 25 °C wartości pK stopniowych stałych dysocjacji wynoszą
- pK 1 = logβ 2 - logβ 1 = 6,77.
- pKa 2 = logβ 1 = 9,93.
Gdy pH = pK, dwa związki chemiczne w równowadze mają to samo stężenie.
Uwaga 1 : Istnieje pozornie sprzecznych wartości w literaturze pK a . Pines i in. przytocz wartość „pK app ” wynoszącą 6,35, zgodną z wartością 6,77 wspomnianą powyżej. Podają również wartość „pK a ” wynoszącą 3,49 i stwierdzają, że
- pK a = pK app − log K D (równanie 5)
gdzie K D = [CO 2 ] / [H 2 CO 3 ]. (przykład 3) Sytuacja wynika ze sposobu, w jaki stałe dysocjacji są nazwane i zdefiniowane, co jest jasno określone w tekście pracy Pines, ale nie w abstrakcie.
Uwaga 2 : Numeracja stałych dysocjacji jest odwrotnością numeracji stałych asocjacji , więc pK 2 (dysocjacja) = log β 1 (asocjacja). Wartość stałej krokowej dla równowagi
jest dany przez
- pK 1 (dysocjacja) 1 = log β 2 − log β 1 (asocjacja)
W rozwiązaniach niebiologicznych
Uwodnienie stała równowagi w temperaturze 25 ° C jest nazywana K h , która w przypadku kwasu węglowego [H 2 CO 3 ] / [CO 2 ] ≈ 1,7 x 10 -3 w czystej wodzie i ≈ 1,2 x 10 -3 w wodzie morskiej . Stąd, większość dwutlenku węgla, nie przekształca się do kwasu karboksylowego, a pozostałe CO 2 cząsteczek. W przypadku braku katalizatora równowaga osiągana jest dość powoli. Te stałe szybkości są 0,039 s -1 do reakcji do przodu i 23 sek -1 do reakcji odwrotnej.
W naturze wapień może reagować z wodą deszczową , tworząc roztwór wodorowęglanu wapnia ; odparowanie takiego roztworu spowoduje ponowne wytworzenie stałego węglanu wapnia. Procesy te zachodzą przy tworzeniu stalaktytów i stalagmitów .
W rozwiązaniach biologicznych
Gdy enzym anhydraza węglanowa jest również obecny w roztworze, pierwszeństwo ma następująca reakcja.
Gdy ilość dwutlenku węgla wytworzonego w reakcji postępującej przekracza jego rozpuszczalność, wydziela się gaz i trzecia równowaga
należy również wziąć pod uwagę. Stałą równowagi dla tej reakcji określa prawo Henry'ego . Obie reakcje można połączyć w celu uzyskania równowagi w roztworze.
- :
Gdy prawo Henry'ego jest używane do obliczenia wartości terminu w mianowniku, należy zachować ostrożność w odniesieniu do wymiarowości.
W fizjologii dwutlenek węgla wydalany przez płuca można nazwać kwasem lotnym lub kwasem oddechowym .
Użycie terminu kwas węglowy
Mówiąc ściśle, termin „kwas węglowy” odnosi się do związku chemicznego o wzorze .
Ponieważ pK a1 ma wartość ca. 6.8, w równowadze kwas węglowy będzie prawie w 50% zdysocjowany w płynie pozakomórkowym ( cytozolu ), który ma pH około 7,2. Należy zauważyć, że rozpuszczony dwutlenek węgla w płynie pozakomórkowym jest często nazywany „kwasem węglowym” w literaturze biochemicznej ze względów historycznych. Reakcja, w której powstaje
- HCO 3 − + H + ⇌ CO 2 + H 2 O
jest szybki w systemach biologicznych. Dwutlenek węgla można opisać jako bezwodnik kwasu węglowego.
Czysty kwas węglowy
Kwas węglowy, H 2 CO 3 , jest stabilny w temperaturze otoczenia w ściśle bezwodnych warunkach. Rozkłada się, tworząc dwutlenek węgla w obecności cząsteczek wody.
Kwas węglowy powstaje jako produkt uboczny napromieniania CO 2 /H 2 O, obok tlenku węgla i rodników (HCO i CO 3 ). Inną drogą tworzenia kwasu węglowego jest protonowanie wodorowęglanów (HCO 3 − ) wodnym roztworem HCl lub HBr. Należy to zrobić w warunkach kriogenicznych , aby uniknąć natychmiastowego rozkładu H 2 CO 3 na CO 2 i H 2 O. Amorficzny H 2 CO 3 tworzy się powyżej 120 K, a krystalizacja zachodzi powyżej 200 K, dając „β-H 2 CO 3 ”, jak określono za pomocą spektroskopii w podczerwieni . Widmo P-H 2 CO 3 zgadza się dobrze z produktem ubocznym CO 2 / H 2 O napromieniowanie. β-H 2 CO 3 sublimuje w temperaturze 230-260 K w dużej mierze bez rozkładu. Spektroskopia w podczerwieni z izolacją matrycy pozwala na rejestrację pojedynczych cząsteczek H 2 CO 3 .
Fakt, że kwas węglowy może powstać przez napromieniowanie stałej mieszaniny H 2 O + CO 2 lub nawet przez implantację protonu samego suchego lodu , dał podstawy do sugestii, że H 2 CO 3 można znaleźć w przestrzeni kosmicznej lub na Marsie , gdzie znaleziono zamarznięte lody H 2 O i CO 2 , a także promienie kosmiczne . Zaskakująca trwałość sublimowanego H 2 CO 3 aż do raczej wysokich temperaturach od 260 K umożliwia nawet w fazie gazowej H 2 CO 3 , to znaczy powyżej biegunowych czapki Mars. Obliczenia ab initio wykazały, że pojedyncza cząsteczka wody katalizuje rozkład cząsteczki kwasu węglowego w fazie gazowej na dwutlenek węgla i wodę. Przewiduje się, że przy braku wody dysocjacja gazowego kwasu węglowego będzie bardzo powolna, z okresem półtrwania w fazie gazowej wynoszącym 180 000 lat w temperaturze 300 K. Dotyczy to tylko przypadków, gdy cząsteczek jest niewiele i są od siebie oddalone, ponieważ Przewiduje się również, że kwas węglowy w fazie gazowej katalizuje swój własny rozkład poprzez tworzenie dimerów , które następnie rozpadają się na dwie cząsteczki: wodę i dwutlenek węgla.
Stwierdzono, że stały „kwas α-węglowy” jest wytwarzany w kriogenicznej reakcji wodorowęglanu potasu i roztworu HCl w metanolu . Twierdzenie to zostało zakwestionowane w pracy doktorskiej złożonej w styczniu 2014 r. Zamiast tego eksperymenty znakowania izotopów wskazują na udział estru monometylowego kwasu węglowego (CAME). Ponadto sublimowany osad je zawierają PRZYCHODZIŁ monomery i dimery nie oznacza H 2 CO 3 monomery i dimery wyżej zastrzeżeniach. Kolejne widma w podczerwieni z izolacją matrycy potwierdziły, że CAME zamiast kwasu węglowego znajduje się w fazie gazowej powyżej „kwasu α-węglowego”. Przypisanie jako CAME jest dodatkowo potwierdzane przez izolację matrycy substancji wytworzonej w fazie gazowej przez pirolizę.
Pomimo swojej skomplikowanej historii kwas węglowy może nadal występować jako odrębne polimorfy . Kwas węglowy tworzy się po utlenieniu CO rodnikami OH. Nie jest jasne czy jest to kwas karboksylowy wytwarza się w ten sposób, należy wziąć pod uwagę jako γ-H 2 CO 3 . Struktury β-H 2 CO 3 i γ-H 2 CO 3 nie zostały scharakteryzowane krystalograficznie.
Pod wysokim ciśnieniem
Chociaż cząsteczki H 2 CO 3 nie stanowią znaczącej części rozpuszczonego węgla w wodnym „kwasie węglowym” w warunkach otoczenia, znaczne ilości cząsteczkowego H 2 CO 3 mogą występować w roztworach wodnych poddanych ciśnieniu wielu gigapaskali (dziesiątki tysięcy atmosfer), jakie mogą wystąpić we wnętrzach planet.
Kwas węglowy powinien być stabilizowany pod ciśnieniem 0,6-1,6 GPa w 100 K i 0,75-1,75 GPa w 300 K. Ciśnienia te są osiągane w rdzeniach dużych lodowych satelitów, takich jak Ganimedes , Callisto i Titan , gdzie woda i dwutlenek węgla są obecni. Czysty kwas węglowy, będąc gęstszy, zatapiałby się następnie pod warstwami lodu i oddzielał je od skalistych jąder tych księżyców.
Bibliografia
Dalsza lektura
-
 „ Klimat i kwas węglowy ” w miesięczniku popularnonaukowym 59, lipiec 1901
„ Klimat i kwas węglowy ” w miesięczniku popularnonaukowym 59, lipiec 1901 - Welcha, MJ; Lifton, JF; Seck, JA (1969). „Badania śladowe z radioaktywnym tlenem-15. Wymiana między dwutlenkiem węgla a wodą”. J. Fiz. Chem. 73 (335): 3351. doi : 10.1021/j100844a033 .
- Wesoły, WL (1991). Nowoczesna Chemia Nieorganiczna (II wyd.) . Nowy Jork: McGraw-Hill. Numer ISBN 978-0-07-112651-9.
- Moore, MH; Channa, R. (1991). „Badania spektralne w podczerwieni i masowe napromieniowanego protonem lodu H2O + Co2: Dowód na kwas węglowy Ice: Dowód na kwas węglowy” . Spectrochimica Acta . 47A (2): 255–262. Kod bib : 1991AcSpA..47..255M . doi : 10.1016/0584-8539(91)80097-3 .
- W. Hage, KR Liedl; Liedl, E.; Hallbrucker, A; Mayer, E (1998). „Kwas węglowy w fazie gazowej i jego astrofizyczne znaczenie”. Nauka . 279 (5355): 1332-1335. Kod Bibcode : 1998Sci...279.1332H . doi : 10.1126/science.279.5355.1332 . PMID 9478889 .
- Hage, W.; Hallbrucker, A.; Mayer, E. (1995). „Polimorf kwasu węglowego i jego możliwe znaczenie astrofizyczne”. J.Chem. Soc. Faradaya przeł. 91 (17): 2823-2826. Kod bib : 1995JCSFT..91.2823H . doi : 10.1039/ft9959102823 .




![{\ Displaystyle \ beta _ {1} = {\ Frac {[{\ tekst {HCO}} _ {3} ^ {-}] {[{\ tekst {H}} ^ {+}][ {\ tekst {CO}}_{3}^{2-}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/170497229ff9169a1bf46ef141b7f8f0e4156143)


![{\ Displaystyle \ beta _ {2} = {\ Frac {[{\ tekst {H}} _ {2} {\ tekst {CO}} _ {3}] {[{\ tekst {H}} ^ { +}]^{2}[{\text{CO}}_{3}^{2-}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b8c36da403b35d01cd677b5d8be799b358f2736a)





![{\ Displaystyle {\ ce {K_3 = {\ Frac {[H ^ +][HCO_3 ^ {-}]} {[CO_2 (soln)]}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/728be989d8b5ded1f0cf378c3ebe5f6532b00c8f)

