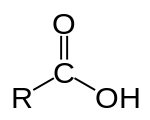
Kwas karboksylowy - Carboxylic acid
Kwasu karboksylowego jest kwas organiczny , który zawiera grupę karboksylową (-C (= O) OH), przyłączone do grupy R. Ogólny wzór kwasu karboksylowego R -COOH lub R-CO 2 H , a R odnosi się do alkilu , alkenylu , arylu , lub inne grupy. Kwasy karboksylowe występują powszechnie. Ważnymi przykładami są aminokwasy i kwasy tłuszczowe . Deprotonowanie kwasu karboksylowego daje anion karboksylanowy .
Przykłady i nazewnictwo
Kwasy karboksylowe są powszechnie identyfikowane przez ich trywialne nazwy . Często mają przyrostek -ic kwas .IUPAC -zalecane nazwy również istnieją; w tym układzie kwasy karboksylowe mają przyrostek -oic . Na przykład kwas masłowy (C 3 H 7 CO 2 H) jest kwasem masłowym według wytycznych IUPAC. W przypadku nomenklatury złożonych cząsteczek zawierających kwas karboksylowy, karboksyl może być uważany za pozycję jeden w łańcuchu macierzystym, nawet jeśli istnieją inne podstawniki , takie jak kwas 3-chloropropanowy . Alternatywnie, można go nazwać podstawnikiem „karboksylowym” lub „kwasem karboksylowym” w innej strukturze macierzystej, takiej jak 2-karboksyfuran .
Anion karboksylanowy (R-COO - lub RCO 2 - ) kwasu karboksylowego jest zwykle nazywany przyrostkiem -ate , zgodnie z ogólnym wzorem kwasu -ic i -ate odpowiednio dla sprzężonego kwasu i jego sprzężonej zasady. Na przykład, sprzężoną zasadą kwasu octowego jest octan .
Kwas węglowy , który w przyrodzie występuje w układach buforowych wodorowęglanów , nie jest generalnie klasyfikowany jako jeden z kwasów karboksylowych, mimo że ma ugrupowanie, które wygląda jak grupa COOH.
| atomów węgla, |
Nazwa zwyczajowa | Nazwa IUPAC | Wzór chemiczny | Wspólna lokalizacja lub użytkowanie |
|---|---|---|---|---|
| 1 | Kwas mrówkowy | Kwas metanowy | HCOOH | Użądlenia owadów |
| 2 | Kwas octowy | Kwas etanowy | CH 3 COOH | Ocet winny |
| 3 | Kwas propionowy | Kwas propanowy | CH 3 CH 2 COOH | Środek konserwujący do przechowywanych zbóż, zapachu ciała , mleka, masła, sera |
| 4 | Kwas masłowy | Kwas butanowy | CH 3 (CH 2 ) 2 COOH | Masło |
| 5 | Kwas walerianowy | Kwas pentanowy | CH 3 (CH 2 ) 3 COOH | Roślina waleriany |
| 6 | Kwas kapronowy | Kwas heksanowy | CH 3 (CH 2 ) 4 COOH | Tłuszcz kozi |
| 7 | Kwas enantowy | Kwas heptanowy | CH 3 (CH 2 ) 5 COOH | Zapach |
| 8 | Kwas kaprylowy | Kwas oktanowy | CH 3 (CH 2 ) 6 COOH | Kokosy |
| 9 | Kwas pelargonowy | Kwas nonanowy | CH 3 (CH 2 ) 7 COOH | Roślina pelargonii |
| 10 | Kwas kaprynowy | Kwas dekanowy | CH 3 (CH 2 ) 8 COOH | Olej kokosowy i z pestek palmy |
| 11 | Kwas undecylowy | Kwas undekanowy | CH 3 (CH 2 ) 9 COOH | Środek przeciwgrzybiczy |
| 12 | Kwas laurynowy | Kwas dodekanowy | CH 3 (CH 2 ) 10 COOH | Olej kokosowy i mydła do mycia rąk |
| 13 | Kwas tridecylowy | Kwas tridekanowy | CH 3 (CH 2 ) 11 COOH | Metabolit roślinny |
| 14 | Kwas mirystynowy | Kwas tetradekanowy | CH 3 (CH 2 ) 12 COOH | Gałka muszkatołowa |
| 15 | Kwas pentadecylowy | Kwas pentadekanowy | CH 3 (CH 2 ) 13 COOH | Tłuszcz mleczny |
| 16 | Kwas palmitynowy | Kwas heksadekanowy | CH 3 (CH 2 ) 14 COOH | olej palmowy |
| 17 | Kwas margarowy | Kwas heptadekanowy | CH 3 (CH 2 ) 15 COOH | Feromony u różnych zwierząt |
| 18 | Kwas stearynowy | Kwas oktadekanowy | CH 3 (CH 2 ) 16 COOH | Czekolada , woski, mydła i olejki |
| 19 | Kwas nonadecylowy | Kwas nonadekanowy | CH 3 (CH 2 ) 17 COOH | Tłuszcze, oleje roślinne, feromon |
| 20 | Kwas arachidowy | Kwas ikozanowy | CH 3 (CH 2 ) 18 COOH | Olej z orzechów |
| Klasa złożona | Członkowie |
|---|---|
| nienasycone kwasy monokarboksylowe | kwas akrylowy ( kwas 2-propenowy) – CH 2 =CHCOOH, stosowany w syntezie polimerów |
| Kwasy tłuszczowe | kwasy monokarboksylowe nasycone i nienasycone średnio- i długołańcuchowe, o parzystej liczbie atomów węgla; przykłady: kwas dokozaheksaenowy i kwas eikozapentaenowy (suplementy diety) |
| Aminokwasy | elementy budulcowe białek |
| Ketokwasy | kwasy o znaczeniu biochemicznym, które zawierają grupę ketonową ; przykłady: kwas acetooctowy i kwas pirogronowy |
| Aromatyczne kwasy karboksylowe | zawierające co najmniej jeden pierścień aromatyczny; przykłady: kwas benzoesowy – sól sodowa kwasu benzoesowego stosowana jest jako konserwant żywności, kwas salicylowy – typ beta-hydroksylowy występujący w wielu produktach do pielęgnacji skóry, kwasy fenyloalkanowe – klasa związków, w których grupa fenylowa jest przyłączona do kwas karboksylowy |
| Kwasy dikarboksylowe | zawierające dwie grupy karboksylowe; przykłady: kwas adypinowy monomer używany do produkcji nylonu i kwas aldarowy – rodzina kwasów cukrowych |
| Kwasy trikarboksylowe | zawierające trzy grupy karboksylowe; przykłady: kwas cytrynowy – występujący w owocach cytrusowych i kwasie izocytrynowym |
| alfa-hydroksykwasy | zawierające grupę hydroksylową w pierwszej pozycji; przykłady: kwas glicerynowy , glikolowy i mlekowy ( kwas 2-hydroksypropanowy) – występujący w kwaśnym mleku, kwas winowy – występujący w winie |
| Kwasy beta-hydroksylowe | zawierające grupę hydroksylową w drugiej pozycji |
| hydroksykwasy omega | zawierające grupę hydroksylową poza pierwszą lub drugą pozycją |
| Kwasy tłuszczowe eteru diwinylowego | zawierający podwójnie nienasycony łańcuch węglowy połączony wiązaniem eterowym z kwasem tłuszczowym, występujący w niektórych roślinach |
Właściwości fizyczne
Rozpuszczalność
Kwasy karboksylowe są polarne . Ponieważ są one zarówno akceptorami wiązań wodorowych (karbonyl –C=O), jak i donorami wiązań wodorowych (hydroksyl –OH), biorą również udział w tworzeniu wiązań wodorowych . Grupa hydroksylowa i karbonylowa tworzą razem grupę funkcyjną karboksylową. Kwasy karboksylowe zwykle występują jako dimery w ośrodkach niepolarnych ze względu na ich tendencję do „asocjacji”. Mniejsze kwasy karboksylowe (1 do 5 atomów węgla) są rozpuszczalne w wodzie, podczas gdy większe kwasy karboksylowe mają ograniczoną rozpuszczalność ze względu na rosnący hydrofobowy charakter łańcucha alkilowego. Te kwasy o dłuższych łańcuchach wydają się być rozpuszczalne w mniej polarnych rozpuszczalnikach, takich jak etery i alkohole. Wodny wodorotlenek sodu i kwasy karboksylowe, nawet hydrofobowe, reagują dając rozpuszczalne w wodzie sole sodowe. Na przykład kwas enatowy ma niską rozpuszczalność w wodzie (0,2 g/l), ale jego sól sodowa jest bardzo dobrze rozpuszczalna w wodzie.
Punkty wrzenia
Kwasy karboksylowe mają zwykle wyższe temperatury wrzenia niż woda, ze względu na ich większą powierzchnię i tendencję do tworzenia stabilizowanych dimerów przez wiązania wodorowe . Aby nastąpiło wrzenie, albo wiązania dimerowe muszą zostać zerwane, albo cały układ dimerów musi zostać odparowany, co znacznie zwiększa wymagania dotyczące entalpii parowania .
Kwasowość
Kwasy karboksylowe to kwasy Brønsteda-Lowry'ego, ponieważ są donorami protonów (H + ). Są najczęstszym rodzajem kwasu organicznego .
Kwasy karboksylowe są zazwyczaj słabymi kwasami , co oznacza, że tylko częściowo dysocjują na kationy H 3 O + i aniony RCOO − w obojętnym roztworze wodnym . Na przykład w temperaturze pokojowej w 1- molowym roztworze kwasu octowego dysocjuje tylko 0,4% kwasu. Podstawnikami odciągającymi elektrony, takimi jak -CF 3 grupy , mocniej kwasu (pKa kwasu mrówkowego wynosi 3,75, podczas gdy kwas trifluorooctowy z podstawnikiem trifluorometylo ma pKa w 0,23). Podstawniki będące donorami elektronów daje słabszego kwasu (pKa kwasu mrówkowego wynosi 3,75, podczas gdy kwas octowy, z podstawnikiem metylowym , ma pKa 4,76)
| Kwas karboksylowy | P K |
|---|---|
| Kwas octowy (CH 3 CO 2 H) | 4,76 |
| Kwas benzoesowy (C 6 H 5 CO 2 H) | 4.2 |
| Kwas mrówkowy (HCOOH) | 3,75 |
| Kwas chlorooctowy (CH 2 ClCO 2 H) | 2.86 |
| Kwas dichlorooctowy (CHCl 2 CO 2 H) | 1,29 |
|
Kwas szczawiowy (HO 2 CCO 2 H)
(pierwsza dysocjacja) |
1,27 |
|
Kwas szczawiowy (HO 2 CCO 2 − )
(druga dysocjacja) |
4.14 |
| Kwas trójchlorooctowy (Cl 3 CO 2 H) | 0,65 |
| Kwas trifluorooctowy (CF 3 CO 2 H) | 0,23 |
Deprotonowanie kwasów karboksylowych daje aniony karboksylanowe; są one stabilizowane rezonansowo , ponieważ ładunek ujemny jest zdelokalizowany nad dwoma atomami tlenu, zwiększając stabilność anionu. Każde z wiązań węgiel-tlen w anionie karboksylanowym ma charakter częściowego wiązania podwójnego. Częściowy ładunek dodatni węgla karbonylowego jest również osłabiony przez -1 / 2 ładunki ujemne na 2 atomach tlenu.
Zapach
Kwasy karboksylowe często mają silny kwaśny zapach. Estry kwasów karboksylowych mają zwykle przyjemny zapach i wiele z nich jest używanych w perfumach .
Charakteryzacja
Kwasy karboksylowe są łatwo identyfikowane jako takie za pomocą spektroskopii w podczerwieni . Wykazują ostre pasmo związane z drganiem wiązania wibracyjnego C–O ( ν C=O ) między 1680 a 1725 cm- 1 . Charakterystyczne pasmo ν O–H pojawia się jako szeroki pik w obszarze 2500 do 3000 cm- 1 . W spektrometrii 1 H NMR hydroksylowy wodór pojawia się w obszarze 10-13 ppm, chociaż często jest albo poszerzony, albo nie obserwowany z powodu wymiany ze śladami wody.
Występowanie i zastosowania
Wiele kwasów karboksylowych jest produkowanych przemysłowo na dużą skalę. Są również często spotykane w naturze. Estry kwasów tłuszczowych są głównymi składnikami lipidów, a poliamidy kwasów aminokarboksylowych są głównymi składnikami białek .
Kwasy karboksylowe są wykorzystywane do produkcji polimerów, farmaceutyków, rozpuszczalników i dodatków do żywności. Ważnymi przemysłowo kwasami karboksylowymi są kwas octowy (składnik octu, prekursor rozpuszczalników i powłok), kwas akrylowy i metakrylowy (prekursory polimerów, spoiw), kwas adypinowy (polimery), kwas cytrynowy (smak i środek konserwujący w żywności i napojach), kwas etylenodiaminotetraoctowy (środek chelatujący), kwasy tłuszczowe (powłoki), kwas maleinowy (polimery), kwas propionowy (konserwant żywności), kwas tereftalowy (polimery). Ważnymi solami karboksylanowymi są mydła.
Synteza
Szlaki przemysłowe
Ogólnie rzecz biorąc, przemysłowe drogi do kwasów karboksylowych różnią się od tych stosowanych na mniejszą skalę, ponieważ wymagają specjalistycznego sprzętu.
- Karbonylowanie alkoholi na przykładzie procesu Cativa do produkcji kwasu octowego. Kwas mrówkowy wytwarzany jest inną drogą karbonylowania, również rozpoczynającą się od metanolu.
- Utlenianie aldehydów powietrzem za pomocą katalizatorów kobaltowych i manganowych. Wymagane aldehydy są łatwo otrzymywane z alkenów przez hydroformylowanie .
- Utlenianie węglowodorów powietrzem. W przypadku prostych alkanów metoda ta jest niedroga, ale niewystarczająco selektywna, aby była użyteczna. Związki allilowe i benzylowe ulegają bardziej selektywnemu utlenianiu. Grupy alkilowe na pierścieniu benzenowym są utleniane do kwasu karboksylowego, niezależnie od długości jego łańcucha. Kwas benzoesowy z toluenu , kwas tereftalowy z para - ksylenu i kwas ftalowy z orto - ksylenu są przykładowymi konwersjami na dużą skalę. Kwas akrylowy powstaje z propenu .
- Utlenianie etenu za pomocą katalizatora kwasu krzemowolframowego .
- Katalizowane zasadą odwodornienie alkoholi.
- Karbonylacja połączona z dodaniem wody. Metoda ta jest skuteczna i wszechstronna w przypadku alkenów generujących drugorzędowe i trzeciorzędowe karbokationy , np. od izobutylenu do kwasu piwalinowego . W reakcji Kocha dodanie wody i tlenku węgla do alkenów jest katalizowane przez mocne kwasy. Hydrokarboksylacje obejmują jednoczesne dodawanie wody i CO . Takie reakcje są czasami nazywane „ chemią Reppe ”.
- HCCH + CO + H 2 O → CH 2 = CHCO 2 H
- Hydroliza triglicerydów otrzymanych z olejów roślinnych lub zwierzęcych. Te metody syntezy niektórych długołańcuchowych kwasów karboksylowych są związane z wytwarzaniem mydła .
- Fermentacja etanolu. Metoda ta stosowana jest przy produkcji octu .
- Reakcja Kolbego zapewnia drogę do kwasu salicylowego , prekursor kwas acetylosalicylowy .
Metody laboratoryjne
Metody preparatywne w reakcjach na małą skalę do badań lub do produkcji chemikaliów wysokowartościowych często wykorzystują drogie zużywalne odczynniki.
- Utlenianie pierwszorzędowych alkoholi lub aldehydów silnymi utleniaczami, takimi jak dwuchromian potasu , odczynnik Jonesa , nadmanganian potasu lub chloryn sodu . Metoda jest bardziej odpowiednia do warunków laboratoryjnych niż przemysłowe zastosowanie powietrza, które jest „bardziej ekologiczne”, ponieważ daje mniej nieorganicznych produktów ubocznych, takich jak tlenki chromu lub manganu.
- Utleniające rozszczepienie olefin przez ozonolizę , nadmanganian potasu lub dichromian potasu .
- Hydroliza nitryli , estrów lub amidów , zwykle z katalizą kwasową lub zasadową.
- Karbonatyzacja odczynnika Grignarda i odczynników litoorganicznych :
- RLi + CO 2 → RCO 2 Li
- RCO 2 Li + HCI → RCO 2 H + LiCI
- Halogenacja, a następnie hydroliza ketonów metylowych w reakcji haloformowej
- Katalizowane zasadą rozszczepienie nieenolizujących ketonów, zwłaszcza ketonów arylowych:
- RC(O)Ar + H 2 O → RCO 2 H + ArH
Rzadsze reakcje
W wielu reakcjach powstają kwasy karboksylowe, ale są one stosowane tylko w określonych przypadkach lub mają głównie znaczenie akademickie.
- Dysproporcjonowanie aldehydu w reakcji Cannizzaro
- Przegrupowanie diketonów w przegrupowaniu kwasu benzoesowego polegające na wytwarzaniu kwasów benzoesowych to reakcja von Richtera z nitrobenzenów i reakcja Kolbe-Schmitta z fenoli .
Reakcje
Najczęściej praktykowane reakcje przekształcają kwasy karboksylowe w estry, amidy, sole karboksylanowe, chlorki kwasowe i alkohole. Kwasy karboksylowe reagują z zasadami tworząc sole karboksylanowe, w których wodór grupy hydroksylowej (–OH) jest zastąpiony kationem metalu . Na przykład kwas octowy znajdujący się w occie reaguje z wodorowęglanem sodu (sodą oczyszczoną), tworząc octan sodu, dwutlenek węgla i wodę:
- CH 3 COOH + NaHCO 3 → CH 3 COO − Na + + CO 2 + H 2 O
Kwasy karboksylowe również reagują z alkoholami dając estry . Proces ten znajduje szerokie zastosowanie np. w produkcji poliestrów . Podobnie kwasy karboksylowe są przekształcane w amidy , ale ta konwersja zazwyczaj nie zachodzi w bezpośredniej reakcji kwasu karboksylowego i aminy. Zamiast tego estry są typowymi prekursorami amidów. Przekształcenie aminokwasów w peptydy to istotny proces biochemiczny, który wymaga ATP .
Grupę hydroksylową na kwasach karboksylowych można zastąpić atomem chloru, stosując chlorek tionylu, otrzymując chlorki acylu . W naturze kwasy karboksylowe są przekształcane w tioestry .
Zmniejszenie
Podobnie jak estry , większość kwasów karboksylowych można zredukować do alkoholi przez uwodornienie lub przy użyciu wodorków lub środków przenoszących alkil (ponieważ zamiast tego odprotonują kwasy bez przenoszenia), takich jak wodorek litowo-glinowy lub odczynniki Grignarda ( związki litoorganiczne ).
Chlorek N , N- dimetylo(chlorometyleno)amoniowy (ClHC=N + (CH 3 ) 2 Cl − ) jest wysoce chemoselektywnym środkiem do redukcji kwasu karboksylowego. Selektywnie aktywuje kwas karboksylowy, dając sól karboksymetylenoamonową, którą można zredukować łagodnym środkiem redukującym, takim jak tris( t- butoksy)glinowy wodorek litu, z wytworzeniem aldehydu w procedurze jednogarnkowej. Wiadomo, że procedura ta toleruje reaktywne grupy funkcyjne karbonylowe, takie jak ketony, jak również umiarkowanie reaktywne grupy estrowe, olefinowe, nitrylowe i halogenkowe.
Reakcje specjalistyczne
- Jak w przypadku wszystkich związków karbonylowych, protony na węglu α są nietrwałe z powodu tautomeryzacji keto-enolowej . Tak więc α-węgiel jest łatwo halogenowany w halogenowaniu Hell-Volhard-Zelinsky .
- Reakcja Schmidta przekształca kwasów karboksylowych amin .
- Kwasy karboksylowe ulegają dekarboksylacji w reakcji Hunsdieckera .
- Reakcji Dakin-West przekształca aminokwasu odpowiednią aminoketonową.
- W degradacji Barbiera-Wielanda kwas karboksylowy w łańcuchu alifatycznym posiadający prosty mostek metylenowy w pozycji alfa może mieć łańcuch skrócony o jeden węgiel. Procedura odwrotna to synteza Arndta-Eisterta , w której kwas przekształca się w halogenek acylu, który następnie poddaje się reakcji z diazometanem, aby uzyskać jeden dodatkowy metylen w łańcuchu alifatycznym.
- Wiele kwasów ulega dekarboksylacji oksydacyjnej . Enzymy katalizujące te reakcje są znane jako karboksylazy ( EC 6.4.1) i dekarboksylazy (EC 4.1.1).
- Kwasy karboksylowe są redukowane do aldehydów poprzez ester i DIBAL , poprzez chlorek kwasowy w redukcji Rosenmunda oraz poprzez tioester w redukcji Fukuyamy .
- W dekarboksylacji ketonowej kwasy karboksylowe są przekształcane w ketony.
- Odczynniki litoorganiczne (>2 równ.) reagują z kwasami karboksylowymi z wytworzeniem 1,1-diolanu dilitu, trwałego tetraedrycznego związku pośredniego, który rozkłada się z wytworzeniem ketonu po obróbce kwasowej.
- Kolbe elektrolizy jest elektrolityczna decarboxylative reakcji dimeryzacji. Pozbywa się grup karboksylowych dwóch cząsteczek kwasu i łączy ze sobą pozostałe fragmenty.
Rodnik karboksylowy
Rodnik karboksylowy , •COOH, istnieje tylko przez krótki czas. Moc kwasu o • COOH została zmierzona za pomocą elektronowego rezonansu paramagnetycznego spektroskopii. Grupa karboksylowa ma tendencję do dimeryzacji, tworząc kwas szczawiowy .
Zobacz też
- Bezwodnik kwasowy
- Chlorek kwasowy
- Amid
- Aminokwas
- Ester
- Lista kwasów karboksylowych
- Kwas dikarboksylowy
- Kwas polihydroksykarboksylowy (PHC).
- Pseudokwas
- Tiokarboksy
Bibliografia
Zewnętrzne linki
- Kwasy karboksylowe pH i miareczkowanie – darmowe oprogramowanie do obliczeń, analizy danych, symulacji i generowania wykresów rozkładu
- POZ.