Karotenoid - Carotenoid
Karotenoidy ( / K ə R ɒ t ɪ n ɔɪ d / ), zwany również tetraterpenoids są żółty, pomarańczowy, czerwony i organiczne pigmenty , które są wytwarzane przez rośliny i glony , jak również kilku bakterii i grzybów . Karotenoidy nadają charakterystyczny kolor dyniom , marchwi , kukurydzy , pomidorom , kanarkom , flamingom , łososiowi , homarowi , krewetkom i żonkilom . Wszystkie te organizmy mogą wytwarzać karotenoidy z tłuszczów i innych podstawowych organicznych elementów budulcowych metabolizmu. Jedynymi stawonogami żyjącymi na lądzie, o których wiadomo, że wytwarzają karotenoidy, są mszyce i przędziorków , które nabyły zdolności i geny od grzybów. Jest również wytwarzany przez bakterie endosymbiotyczne u mączlików . Karotenoidy z pożywienia są magazynowane w tkankach tłuszczowych zwierząt, a wyłącznie zwierzęta mięsożerne pozyskują je z tłuszczu zwierzęcego. W diecie człowieka wchłanianie karotenoidów ulega poprawie, gdy są spożywane z tłuszczem w posiłku. Gotowanie warzyw zawierających karotenoidy w oleju i szatkowanie warzyw zwiększają biodostępność karotenoidów .
Istnieje ponad 1100 znanych karotenoidów, które można podzielić na dwie klasy: ksantofile (zawierające tlen) i karoteny (które są wyłącznie węglowodorami i nie zawierają tlenu). Wszystkie są pochodnymi z tetraterpeny , co oznacza, że wytwarza się z 8 izoprenu cząsteczek i zawiera 40 atomów węgla. Ogólnie rzecz biorąc, karotenoidy pochłaniają fale o długości od 400 do 550 nanometrów (światło fioletowe do zielonego). Powoduje to, że związki są głęboko zabarwione na żółto, pomarańczowo lub czerwono. Karotenoidy są dominującym barwnikiem w jesiennym wybarwieniu liści około 15-30% gatunków drzew, ale wiele kolorów roślin, zwłaszcza czerwonych i fioletowych, zawdzięczamy polifenolom .
Karotenoidy pełnią dwie kluczowe role w roślinach i algach: absorbują energię świetlną do wykorzystania w fotosyntezie i zapewniają fotoochronę poprzez gaszenie niefotochemiczne . Karotenoidy zawierające niepodstawione pierścienie beta-jononowe (w tym β-karoten , α-karoten , β-kryptoksantyna i γ-karoten ) wykazują aktywność witaminy A (co oznacza, że mogą zostać przekształcone w retinol ). W oka, luteina , mezo -zeaxanthin i zeaksantyna występują jako pigmentów plamki , których znaczenie w funkcji wzroku, jak od 2016 roku pozostaje pod badań klinicznych .
Biosynteza
Podstawowymi budulcami karotenoidów są difosforan izopentenylu (IPP) i difosforan dimetyloallilu (DMAPP). Te dwa izomery izoprenowe są wykorzystywane do tworzenia różnych związków w zależności od ścieżki biologicznej zastosowanej do syntezy izomerów. Wiadomo, że rośliny wykorzystują dwa różne szlaki wytwarzania IPP: szlak cytozolowego kwasu mewalonowego (MVA) i plastydowy 4-fosforan metyloerytrytolu (MEP). U zwierząt produkcja cholesterolu zaczyna się od tworzenia IPP i DMPP przy użyciu MVA. W przypadku zakładów produkujących karotenoidy stosuj MEP do generowania IPP i DMPP. Szlak MEP skutkuje mieszaniną 5:1 IPP:DMAPP. IPP i DMAPP przechodzą kilka reakcji, w wyniku których powstaje główny prekursor karotenoidów, difosforan geranylogeranylu (GGPP). GGPP można przekształcić w karoteny lub ksantofile, przechodząc szereg różnych etapów szlaku biosyntezy karotenoidów.
Ścieżka posła do PE
3-fosforan aldehydu glicerynowego i pirogronian , produkty pośrednie fotosyntezy , są przekształcane w dezoksy-D-ksylulozo-5-fosforan (DXP) przy użyciu katalizatora syntazy DXP (DXS). Reduktoizomeraza DXP redukuje i przekształca cząsteczki w DXP w obecności NADPH , tworząc MEP. Następnie MEP jest przekształcany w 4-(cytydyno-5'-difosfo)-2-C-metylo-D-erytrytol (CDP-ME) w obecności CTP przez enzym cytydylilotransferazę MEP. CDP-ME jest następnie przekształcany, w obecności ATP , do 2-fosfo-4-(cytydyno-5'-difosfo)-2-C-metylo-D-erytrytolu (CDP-ME2P). Konwersja do CDP-ME2P jest katalizowana przez enzym kinazę CDP-ME . Następnie CDP-ME2P jest przekształcany w 2,4-cyklodifosforan 2-C-metylo-D-erytrytolu (MECDP). Ta reakcja zachodzi, gdy syntaza MECDP katalizuje reakcję, a CMP jest eliminowany z cząsteczki CDP-ME2P. MECDP jest następnie przekształcany w difosforan (e)-4-hydroksy-3-metylobut-2-en-1-ylu (HMBDP) przez syntazę HMBDP w obecności flawodoksyny i NADPH. HMBDP jest redukowany do IPP w obecności ferredoksyny i NADPH przez enzym reduktazę HMBDP . Ostatnie dwa etapy obejmujące syntazę i reduktazę HMBPD mogą wystąpić tylko w środowiskach całkowicie beztlenowych . IPP jest następnie zdolny do izomeryzacji do DMAPP przez izomerazę IPP.
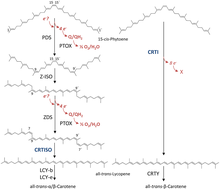
Szlak biosyntezy karotenoidów
Dwie cząsteczki GGPP skroplona przez syntazę fitoenu (PSY), tworząc 15-cis- izomer z fitoenu . Późniejsza konwersja do całkowicie translikopenu zależy od organizmu. Bakterie i grzyby wykorzystują do katalizy jeden enzym, bakteryjną desaturazę fitoenu (CRTI). Jednak rośliny i sinice wykorzystują w tym procesie cztery enzymy. Pierwszym z tych enzymów jest roślinna desaturaza fitoenu, która poprzez odwodornienie wprowadza dwa dodatkowe wiązania podwójne do 15-cis-fitoenu i izomeryzuje dwa z istniejących wiązań podwójnych z trans do cis, wytwarzając 9,15,9'-tri-cis- ζ-karoten. Centralne wiązanie podwójne tego tri-cis-ζ-karotenu jest izomeryzowane przez izomerazę zeta-karotenu Z-ISO, a powstały 9,9'-di-cis-ζ-karoten jest ponownie odwodorniany przez desaturazę ζ-karotenu (ZDS ) . To ponownie wprowadza dwa podwójne wiązania, w wyniku czego powstaje 7,9,7',9'-tetra-cis-likopen. CRTISO , karotenoidy izomeraza jest potrzebna do przekształcenia cis -lycopene się z all-trans likopenu w obecności ograniczonej FAD .
Ten całkowicie trans likopen jest cyklizowany; cyklizacja powoduje zróżnicowanie karotenoidów, które można rozróżnić na podstawie grup końcowych. Może istnieć pierścień beta lub pierścień epsilon, każdy generowany przez inny enzym ( beta-cyklaza likopenu [beta-LCY] lub epsilon-cyklaza likopenu [epsilon-LCY]). α-karoten jest wytwarzany, gdy all-trans likopen najpierw poddaje się reakcji z epsilon-LCY, a następnie drugiej reakcji z beta-LCY; podczas gdy β-karoten jest wytwarzany w dwóch reakcjach z beta-LCY. α- i β-karoten są najczęstszymi karotenoidami w fotosystemach roślin, ale nadal można je przekształcić w ksantofile za pomocą beta-hydrolazy i epsilon-hydrolazy, co prowadzi do powstania różnych ksantofilów.
Rozporządzenie
Uważa się, że zarówno DXS, jak i DXR są enzymami determinującymi szybkość, co pozwala im regulować poziom karotenoidów. Zostało to odkryte w eksperymencie, w którym DXS i DXR ulegały nadekspresji genetycznej, co prowadziło do zwiększonej ekspresji karotenoidów w powstałych sadzonkach. Uważa się również, że białka opiekuńcze białka J (J20) i białka szoku cieplnego 70 (Hsp70) są zaangażowane w posttranskrypcyjną regulację aktywności DXS, tak że mutanty z wadliwą aktywnością J20 wykazują zmniejszoną aktywność enzymu DXS podczas gromadzenia nieaktywnego białka DXS. Regulacja może być również spowodowana przez zewnętrzne toksyny, które wpływają na enzymy i białka wymagane do syntezy. Ketoklomazon pochodzi z herbicydów stosowanych do gleby i wiąże się z syntazą DXP. Hamuje to syntazę DXP, zapobiegając syntezie DXP i zatrzymując szlak MEP. Stosowanie tej toksyny prowadzi do obniżenia poziomu karotenoidów w roślinach uprawianych w skażonej glebie. Fosmidomycyna , antybiotyk , jest konkurencyjnym inhibitorem reduktoizomerazy DXP ze względu na swoją strukturę podobną do enzymu. Zastosowanie tego antybiotyku zapobiega redukcji DXP, ponownie zatrzymując szlak MEP.
Struktura i funkcja
Struktura karotenoidów pozwala na zdolności biologiczne, w tym fotosyntezę , fotoprotekcję , zabarwienie roślin i sygnalizację komórkową .
Ogólna struktura karotenoidu to łańcuch polienowy składający się z 9-11 podwójnych wiązań i ewentualnie zakończony pierścieniami. Ta struktura sprzężonych wiązań podwójnych prowadzi do wysokiego potencjału redukcyjnego, czyli zdolności do przenoszenia elektronów w cząsteczce. Karotenoidy mogą przenosić energię wzbudzenia na dwa sposoby: 1) transfer energii singlet-singlet z karotenoidu do chlorofilu oraz 2) transfer energii triplet-triplet z chlorofilu do karotenoidu. Transfer energii singlet-singlet jest transferem stanu o niższej energii i jest wykorzystywany podczas fotosyntezy. Długość ogona polienowego umożliwia absorbcję światła w zakresie fotosyntezy; po pochłonięciu energii staje się wzbudzony, a następnie przenosi wzbudzone elektrony do chlorofilu w celu fotosyntezy. Transfer tryplet-tryplet jest wyższym stanem energetycznym i jest niezbędny w fotoochronie. Światło wytwarza szkodliwe gatunki podczas fotosyntezy, przy czym najbardziej szkodliwe są reaktywne formy tlenu (ROS). Ponieważ te wysokoenergetyczne ROS są wytwarzane w chlorofilu, energia jest przekazywana do polienowego ogona karotenoidu i przechodzi szereg reakcji, w których elektrony przemieszczają się między wiązaniami karotenoidowymi, aby znaleźć najbardziej zrównoważony stan (najniższy stan energetyczny) dla karotenoidu.
Długość karotenoidów ma również wpływ na ubarwienie rośliny, ponieważ długość ogona polienowego określa, jakie długości fal światła będzie absorbowana przez roślinę. Długości fal, które nie są pochłaniane, są odbijane i są tym, co widzimy jako kolor rośliny. W związku z tym różne gatunki będą zawierać karotenoidy o różnej długości ogona, co pozwoli im wchłaniać i odbijać różne kolory.
Karotenoidy biorą również udział w różnych typach sygnalizacji komórkowej. Są w stanie sygnalizować produkcję kwasu absycynowego , który reguluje wzrost roślin, spoczynek nasion , dojrzewanie i kiełkowanie zarodków , podział i wydłużanie komórek , wzrost kwiatów i reakcje na stres.
Nieruchomości
Karotenoidy należą do kategorii tetraterpenoidów (tzn. zawierają 40 atomów węgla, są zbudowane z czterech jednostek terpenowych , z których każda zawiera 10 atomów węgla). Strukturalnie karotenoidy przyjmują postać polienowego łańcucha węglowodorowego, który czasami jest zakończony pierścieniami i może, ale nie musi, mieć przyłączone dodatkowe atomy tlenu.
- Karotenoidy z cząsteczkami zawierającymi tlen, takie jak luteina i zeaksantyna , są znane jako ksantofile .
- Karotenoidy bez tlenu (bez tlenu), takie jak α-karoten , β-karoten i likopen , są znane jako karoteny . Karoteny zazwyczaj zawierają tylko węgiel i wodór (tj. są węglowodorami ) i należą do podklasy węglowodorów nienasyconych .
Ich barwa, od jasnożółtej, przez jasnopomarańczową, po głęboką czerwień, jest bezpośrednio związana z ich strukturą. Ksantofile są często żółte, stąd ich nazwa klasy. Do podwójnych wiązań węgiel-węgiel współdziałają ze sobą w procesie zwanym sprzęgania , która pozwala na elektrony cząsteczki swobodnie poruszać się po drugiej stronie tych obszarów w cząsteczce. Wraz ze wzrostem liczby sprzężonych wiązań podwójnych elektrony związane z układami sprzężonymi mają więcej miejsca do poruszania się i wymagają mniej energii do zmiany stanów. Powoduje to zmniejszenie zakresu energii światła pochłanianego przez cząsteczkę. Ponieważ więcej długości fal światła jest absorbowanych z dłuższego końca widma widzialnego, związki nabierają coraz bardziej czerwonego wyglądu.
Karotenoidy są zazwyczaj lipofilowe ze względu na obecność długich nienasyconych łańcuchów alifatycznych , jak w niektórych kwasach tłuszczowych . Fizjologiczne wchłanianie tych rozpuszczalnych w tłuszczach witamin u ludzi i innych organizmów zależy bezpośrednio od obecności tłuszczów i soli żółciowych .
Żywność
Za ich pomarańczowo-żółty kolor odpowiada beta-karoten , występujący w dyniach , słodkich ziemniakach , marchwi i dyni zimowej . Suszona marchewka ma największą ilość karotenu ze wszystkich pokarmów na 100-gramową porcję, mierzoną w ekwiwalentach aktywności retinolu (ekwiwalenty prowitaminy A). Owoc wietnamski gac zawiera najwyższe znane stężenie likopenu karotenoidowego . Chociaż zielony, jarmuż , szpinak , kapusta włoska i rzepa zawierają znaczne ilości beta-karotenu. Dieta flamingów jest bogata w karotenoidy, które nadają tym ptakom pomarańczowe pióra.
Morfologia
Karotenoidy są zlokalizowane głównie poza jądrem komórkowym w różnych organellach cytoplazmy, kropelkach lipidów , cytosomach i ziarnistościach. Zostały one zwizualizowane i określone ilościowo za pomocą spektroskopii ramanowskiej w komórce alg .
Wraz z rozwojem przeciwciał monoklonalnych do trans likopen możliwe było zlokalizować ten karotenoid w różnych komórkach ludzi i zwierząt.
Natlenianie
Karotenoidy odgrywają ważną rolę w biologicznym natlenianiu. W komórkach roślinnych biorą udział w kontroli transportu przezbłonowego tlenu cząsteczkowego uwalnianego w fotosyntezie .
U zwierząt karotenoidy odgrywają ważną rolę we wspieraniu tlenu w jego transporcie, magazynowaniu i metabolizmie.
Transport
Karotenoidy są hydrofobowe i są zazwyczaj obecne w lipoproteinach osocza i strukturach lipidów komórkowych. Ponieważ tlen cząsteczkowy jest również cząsteczką hydrofobową , lipidy zapewniają bardziej korzystne środowisko dla rozpuszczalności O 2 niż w środowiskach wodnych. Chroniąc lipidy przed uszkodzeniem przez wolne rodniki, które generują naładowane nadtlenki lipidów i inne utlenione pochodne, karotenoidy wspierają architekturę krystaliczną i hydrofobowość lipoproteiny i struktury lipidów komórkowych, a więc rozpuszczalność tlenu i jego dyfuzja do nich.
Składowanie
Po raz pierwszy VN Karnaukhov zasugerował, że karotenoidy mogą być zaangażowane w wewnątrzkomórkowy magazyn tlenu w 1973 roku. Później odkryto, że karotenoidy mogą również stymulować tworzenie wewnątrzkomórkowych kropelek lipidowych, które mogą magazynować dodatkowy tlen cząsteczkowy. Te właściwości karotenoidów pomagają zwierzętom przystosować się do stresów środowiskowych, dużej wysokości , infekcji wewnątrzkomórkowych i innych stanów niedotlenienia .
Oddychanie
Karotenoidy, zwiększając dyfuzję tlenu i zdolność lipoprotein osocza do przenoszenia tlenu, mogą stymulować dostarczanie tlenu do tkanek organizmu. Poprawia to dotlenienie tkanek i komórek oraz stymuluje wzrost i oddychanie mitochondriów .
Modalność synergiczna
Tlen jest niezbędny w wielu reakcjach wewnątrzkomórkowych, w tym hydroksylacji, która jest ważna dla aktywacji metabolicznej proleków i prohormonów , takich jak witamina D3. Karotenoidy nie tylko wspierają wewnątrzkomórkowe natlenianie, ale mogą również poprawiać skuteczność tych cząsteczek.
Karotenoidy mogą tworzyć fizyczne kompleksy z różnymi cząsteczkami. W przypadku cząsteczek hydrofobowych może to być samoorganizacja. Z amfifilowych lub hydrofilowych związków stosowanie lycosome lub nadkrytycznym CO 2 technologii, lub innych metod są wymagane. ] Karotenoidy w tych kompleksów stanowią nową modalność wspierania i zwiększenia utlenowanie tkanek, które mogą być synergiczne korzystne dla celów terapeutycznych w różnym nutraceutycznych lub w farmaceutycznych cząsteczek.
Efekty fizjologiczne
Przeglądy badań epidemiologicznych poszukujących korelacji między spożyciem karotenoidów w żywności a wynikami klinicznymi doprowadziły do różnych wniosków:
- Przegląd z 2015 r. wykazał, że pokarmy bogate w karotenoidy wydają się chronić przed nowotworami głowy i szyi .
- W innym przeglądzie z 2015 r. dotyczącym tego, czy kartenoidy mogą zapobiegać rakowi prostaty, stwierdzono, że chociaż kilka badań wykazało, że korelacje między dietami bogatymi w karotenoidy wydają się mieć działanie ochronne, brakuje dowodów, aby ustalić, czy jest to spowodowane karotenoidami jako takimi.
- Przegląd z 2014 r. nie wykazał korelacji między spożywaniem pokarmów bogatych w karotenoidy i witaminę A a ryzykiem zachorowania na chorobę Parkinsona .
- W innym przeglądzie z 2014 r. nie znaleziono sprzecznych wyników w badaniach nad spożyciem karotenoidów i ryzykiem zachorowania na raka piersi .
Karotenoidy są również ważnymi składnikami ciemnobrązowego pigmentu melaniny , który znajduje się we włosach, skórze i oczach. Melanina pochłania wysokoenergetyczne światło i chroni te narządy przed uszkodzeniami wewnątrzkomórkowymi.
- W kilku badaniach zaobserwowano pozytywny wpływ diety bogatej w karotenoidy na teksturę, przejrzystość, kolor, siłę i elastyczność skóry.
- W badaniu z 1994 r. zauważono, że dieta bogata w karotenoidy pomogła zmniejszyć objawy zmęczenia oczu (suchość oka, bóle głowy i niewyraźne widzenie) oraz poprawić widzenie w nocy.
Ludzie i inne zwierzęta są w większości niezdolne do syntezy karotenoidów i muszą je pozyskiwać poprzez dietę. Karotenoidy są powszechną i często ozdobną cechą zwierząt. Na przykład różowy kolor łososia i czerwony kolor gotowanych homarów i łusek żółtej odmiany jaszczurek pospolitych są spowodowane karotenoidami. Zaproponowano, aby karotenoidy były wykorzystywane w cechach ozdobnych (do skrajnych przykładów patrz ptaki maskonurów ), ponieważ ze względu na ich właściwości fizjologiczne i chemiczne mogą być wykorzystywane jako widoczne wskaźniki indywidualnego zdrowia, a co za tym idzie są wykorzystywane przez zwierzęta przy doborze potencjalnych partnerów.
Kolory roślin

Najczęstsze karotenoidy to likopen i prekursor witaminy A β-karoten. W roślinach ksantofil luteina jest najpowszechniejszym karotenoidem, a jej rola w zapobieganiu chorobom oczu związanym z wiekiem jest obecnie badana. Luteina i inne barwniki karotenoidowe znajdujące się w dojrzałych liściach często nie są oczywiste ze względu na maskującą obecność chlorofilu . Gdy chlorofil nie jest obecny, jak w jesiennych liściach, przeważają żółcie i pomarańcze karotenoidów. Z tego samego powodu barwy karotenoidów często dominują w dojrzałych owocach po zdemaskowaniu ich przez zniknięcie chlorofilu.
Karotenoidy są odpowiedzialne za jaskrawe żółcie i pomarańcze, które zabarwiają liście liściaste (takie jak zamierające jesienne liście ) niektórych gatunków twardego drewna, takich jak hikory , jesion , klon , żółta topola , osika , brzoza , czereśnia , jawor , topolia , sasafras i olcha . Karotenoidy są dominującym barwnikiem w jesiennym wybarwieniu liści około 15-30% gatunków drzew. Jednak czerwienie, fiolety i ich mieszane kombinacje, które zdobią jesienne liście, zwykle pochodzą z innej grupy pigmentów w komórkach zwanych antocyjanów . W przeciwieństwie do karotenoidów pigmenty te nie są obecne w liściach przez cały sezon wegetacyjny, ale są aktywnie produkowane pod koniec lata.
Chemikalia zapachowe
Produkty degradacji karotenoidów, takie jak jony , damaskony i damascenony, są również ważnymi substancjami zapachowymi, które są szeroko stosowane w perfumerii i przemyśle perfumeryjnym . Zarówno β-damascenon, jak i β-jonon, chociaż w destylatach z róży są niskie, są kluczowymi związkami zapachowymi w kwiatach. W rzeczywistości słodkie kwiatowe zapachy obecne w czarnej herbacie , dojrzałym tytoniu , winogronach i wielu owocach wynikają ze związków aromatycznych powstających w wyniku rozpadu karotenoidów.
Choroba
Niektóre karotenoidy są produkowane przez bakterie w celu ochrony przed oksydacyjnym atakiem odpornościowym. Aureus (Golden) pigment, który nadaje niektóre szczepy Staphylococcus aureus ich nazwa karotenoid zwany staphyloxanthin . Ten karotenoid jest czynnikiem zjadliwości o działaniu przeciwutleniającym, który pomaga drobnoustrojowi uniknąć śmierci przez reaktywne formy tlenu wykorzystywane przez układ odpornościowy gospodarza.
Naturalnie występujące karotenoidy
- Węglowodory
- Lycopersene 7,8,11,12,15,7' , 8' , 11' , 12' , 15'-dekahydro-γ, γ-karoten
- Fitofluen
- Likopen
- Heksahydrolikopen 15- cis -7,8,11,12,7',8'-Heksahydro-γ,γ-karoten
- Torulen 3',4'-didehydro-β,γ-karoten
- α-zeakaroten 7',8'-dihydro-ε,γ-karoten
- α-karoten
- β-karoten
- γ-karoten
- δ-karoten
- ε-karoten
- ζ-karoten
- Alkohole
- Alloksantyna
- Bacterioruberin 2,2'-bis(3-hydroksy-3-metylobutylo)-3,4,3',4'-tetradehydro-1,2,1',2'-tetrahydro-γ,γ-karoten-1,1 „-diol”
- Cyntiaksantyna
- Pektenoksantyna
- Kryptomonaksantyna (3R,3'R)-7,8,7',8'-tetradehydro-β,β-karoten-3,3'-diol
- Krustaksantyna β,-karoten-3,4,3',4'-tetrol
- Gazaniaksantyna (3R)-5'-cis-β,γ-karoten-3-ol
- OH-chlorobakten 1',2'-dihydro-f,γ-karoten-1'-ol
- Loroksantyna β,ε-karoten-3,19,3'-triol
- Luteina (3R,3′R,6′R)-β,ε-karoten-3,3′-diol
- Lycoxanthin γ, γ-karoten-16-ol
- Rodopina 1,2-dihydro-γ,γ-karoten-l-ol
- Rodopinol aka Warmingol 13- cis -1,2-dihydro-γ,γ-karoten-1,20-diol
- Saproksantyna 3',4'-didehydro-1',2'-dihydro-β,γ-karoten-3,1'-diol
- Zeaksantyna
- Glikozydy
- Oscylaksantyna 2,2'-bis(β-L-ramnopiranozyloksy)-3,4,3',4'-tetradehydro-1,2,1',2'-tetrahydro-γ,γ-karoten-1,1'- diol
- Fleiksantofil 1'-(β-D-glukopiranozyloksy)-3',4'-didehydro-1',2'-dihydro-β,γ-karoten-2'-ol
- Etery
- Rodowibryna 1'-metoksy-3',4'-didehydro-1,2,1',2'-tetrahydro-γ,γ-karoten-1-ol
- Sferoiden 1-metoksy-3,4-didehydro-1,2,7',8'-tetrahydro-γ,γ-karoten
- Epoksydy
- Diadinoksantyna 5,6-epoksy-7',8'-didehydro-5,6-dihydro-karoten-3,3-diol
- Luteoksantyna 5,6:5',8'-Diepoksy-5,6,5',8'-tetrahydro-β,β-karoten-3,3'-diol
- Mutatoksantyna
- Cytroksantyna
- Furanotlenek zeaksantyny 5,8-epoksy-5,8-dihydro-β,β-karoten-3,3'-diol
- Neochrom 5',8'-epoksy-6,7-didehydro-5,6,5',8'-tetrahydro-β,β-karoten-3,5,3'-triol
- Foliachrome
- Trollichrome
- Vaucheriaksantyna 5',6'-epoksy-6,7-didehydro-5,6,5',6'-tetrahydro-β,β-karoten-3,5,19,3'-tetrol
- Aldehydy
- rodopina
- Warmingone 13-cis-1-hydroksy-1,2-dihydro-γ,γ-karoten-20-al
- Aldehyd tolarodynowy 3',4'-didehydro-β,γ-karoten-16'-al
- Kwasy i estry kwasów
- Torularhodin kwas 3',4'-didehydro-β,γ-karoten-16'-owy
- Ester metylowy toularodyny 3',4'-didehydro-β,γ-karoten-16'-onian metylu
- Ketony
- Astacen
- Astaksantyna
- Kantaksantyny aka Aphanicin, Chlorellaxanthin β, β-karoten-4,4-dionu
- Kapsantyna (3R,3'S,5'R)-3,3'-Dihydroksy-β,κ-karoten-6'-on
- Kapsorubina (3S,5R,3'S,5'R)-3,3'-dihydroksy-κ,κ-karoten-6,6'-dion
- Kryptokapsyna (3'R,5'R)-3'-hydroksy-β,κ-karoten-6'-on
- 2,2'-diketospirilloksantyna 1,1'-dimetoksy-3,4,3',4'-tetradehydro-1,2,1',2'-tetrahydro-γ,γ-karoten-2,2'-dion
- Echinenon β,β-karoten-4-on
- 3'-hydroksyechinenon
- Flexiksantyna 3,1'-dihydroksy-3',4'-didehydro-1',2'-dihydro-β,γ-karoten-4-on
- 3-OH Kantaksantyna vel Adonirubin vel Phoenicoxanthin 3-hydroksy-β, β-karotenu-4,4-dion,
- Hydroksysferiodenon 1'-hydroksy-1-metoksy-3,4-didehydro-1,2,1',2',7',8'-heksahydro-γ,γ-karoten-2-on
- Okenon 1'-metoksy-1',2'-dihydro-c,γ-karoten-4'-on
- Pektenolon 3,3'-Dihydroksy-7',8'-didehydro-β,β-karoten-4-on
- Phoeniconone aka Dehydroadonirubina 3-hydroksy-2,3-didehydro-β,β-karoten-4,4'-dion
- Fenikopteron β,ε-karoten-4-on
- Rubiksanton 3-hydroksy-β,γ-karoten-4'-on
- Sifonaksantyna 3,19,3'-trihydroksy-7,8-dihydro-β,ε-karoten-8-on
- Estry alkoholi
- Astaceina 3,3'-bispalmitoiloksy-2,3,2',3'-tetradehydro-β,β-karoten-4,4'-dion lub 3,3'-dihydroksy-2,3,2',3'- dipalmitynian tetradehydro-β,β-karoten-4,4'-dionu
- Fukoksantyna 3'-acetoksy-5,6-epoksy-3,5'-dihydroksy-6' , 7'-didehydro-5,6,7,8,5' , 6'-heksahydro-β, β-karotenu-8 -jeden
- Izofukoksantyna 3'-acetoksy-3,5,5'-trihydroksy-6',7'-didehydro-5,8,5',6'-tetrahydro-β,β-karoten-8-on
- Fisalien
- Syfonina 3,3'-dihydroksy-19-lauroiloksy-7,8-dihydro-β,ε-karoten-8-on lub 3,19,3'-trihydroksy-7,8-dihydro-β,ε-karoten-8 -jeden 19-laureat
-
Apokarotenoidy
- β-Apo-2'-karotenal 3',4'-Didehydro-2'-apo-b-karoten-2'-al
- Apo-2-likopenal
- Apo-6'-likopenal 6'-Apo-y-karoten-6'-al
- Aldehyd azafrynowy 5,6-Dihydroksy-5,6-dihydro-10'-apo-β-karoten-10'-al
- Biksynę 6'-laktonu cis-9'-6,6'-diapocarotene-6,6'-dikarboksylan
- cytranaksantyna 5',6'-dihydro-5'-apo-β-karoten-6'-on lub 5',6'-dihydro-5'-apo-18'-nor-β-karoten-6'-on lub 6'-metylo-6'-apo-β-karoten-6'-on
- Krocetyna Kwas 8,8'-Diapo-8,8'-karotenodiowy
- Crocetinsemialdehyde Kwas 8'-okso-8,8'-diapo-8-karotenowy
- Crocin Digentiobiosyl 8,8'-diapo-8,8'-karotenodiian
- Hopkinsiaksantyna 3-hydroksy-7,8-didehydro-7',8'-dihydro-7'-apo-b-karoten-4,8'-dion lub 3-hydroksy-8'-metylo-7,8-didehydro- 8'-apo-b-karoten-4,8'-dion
- Apo-6'-likopenian metylu 6'-apo-y-karoten-6'-onian metylu
- Paracentrone 3,5-dihydroksy-6,7-didehydro-5,6,7',8'-tetrahydro-7'-apo-b-karoten-8'-on lub 3,5-dihydroksy-8'-metylo- 6,7-didehydro-5,6-dihydro-8'-apo-b-karoten-8'-on
- Sintaksantyna 7',8'-Dihydro-7'-apo-b-karoten-8'-on lub 8'-metylo-8'-apo-b-karoten-8'-on
- Nor- i seco-karotenoidy
- Aktinoerytryna 3,3'-Bisacyloksy-2,2'-dinor-b,b-karoten-4,4'-dion
- β-karotenon 5,6:5',6'-Diseco-b,b-karoten-5,6,5',6'-tetron
- Perydynina 3'-acetoksy-5,6-epoksy-3,5'-dihydroksy-6',7'-didehydro-5,6,5',6'-tetrahydro-12',13',20'-trinor- b,b-karoten-19,11-olid
- Pirroksantyninol 5,6-epoksy-3,3'-dihydroksy-7',8'-didehydro-5,6-dihydro-12',13',20'-trinor-b,b-karoten-19,11-olid
- Semi-α-karotenon 5,6-Seco-b,e-karoten-5,6-dion
- Semi-β-karotenon 5,6-seco-b,b-karoten-5,6-dion lub 5',6'-seco-b,b-karoten-5',6'-dion
- Trifazjaksantyna 3-Hydroksysemi-b-karotenon 3'-Hydroksy-5,6-seco-b,b-karoten-5,6-dion lub 3-hydroksy-5',6'-seco-b,b-karoten-5 ',6'-dione
- Retro-karotenoidy i retro-apo-karotenoidy
- Eschscholtzksantyna 4',5'-didehydro-4,5'-retro-b,b-karoten-3,3'-diol
- Eschscholtzxantone 3'-hydroksy-4',5'-didehydro-4,5'-retro-b,b-karoten-3-on
- Rodoksantyna 4',5'-didehydro-4,5'-retro-b,b-karoten-3,3'-dion
- Tangeraksantyna 3-hydroksy-5'-metylo-4,5'-retro-5'-apo-b-karoten-5'-on lub 3-hydroksy-4,5'-retro-5'-apo-b-karoten -5'-jeden
- Wyższe karotenoidy
- Nonaprenoksantyna 2-(4-hydroksy-3-metylo-2-butenylo)-7',8',11',12'-tetrahydro-e,y-karoten
- Dekaprenoksantyna 2,2'-bis(4-hydroksy-3-metylo-2-butenylo)-e,e-karoten
- Cp 450 2-[4-hydroksy-3-(hydroksymetylo)-2-butenylo]-2'-(3-metylo-2-butenylo)-b,b-karoten
- Cp 473 2'-(4-hydroksy-3-metylo-2-butenylo)-2-(3-metylo-2-butenylo)-3',4'-didehydro-1',2'-dihydro-β,γ -karoten-1'-ol
- Bacterioruberin 2,2'-bis(3-hydroksy-3-metylobutylo)-3,4,3',4'-tetradehydro-1,2,1',2'-tetrahydro-γ,γ-karoten-1,1 „-diol”
Zobacz też
- Lista fitochemikaliów w żywności
- CRT (genetyka) , klaster genów odpowiedzialny za biosyntezę karotenoidów
- Numer E#E100–E199 (kolory)
- Fitochemia
Bibliografia
Zewnętrzne linki
- Terpenoidy karotenoidowe
- Karotenoidy jako prekursory smaku i zapachu
- Gen karotenoidowy u mszyc
- Międzynarodowe Towarzystwo Karotenoidów
- Karotenoidy w amerykańskiej National Library of Medicine Medical Subject Headings (MeSH)