Eter koronowy - Crown ether
Etery koronowe to cykliczne związki chemiczne, które składają się z pierścienia zawierającego kilka grup eterowych . Najczęstszym Etery koronowe są cyklicznymi oligomerami z tlenkiem etylenu , powtarzająca się jednostka jest oksyetylenowych, czyli CH 2 CH 2 O-. Ważnymi członkami tej serii są tetramer ( n = 4), pentamer ( n = 5) i heksamer ( n = 6). Termin „korona” odnosi się do podobieństwa między strukturą eteru korony związanego z kationem , a koroną osadzoną na głowie osoby. Pierwsza liczba w nazwie eteru koronowego odnosi się do liczby atomów w cyklu, a druga liczba odnosi się do liczby tych atomów, które są tlenem . Etery koronowe są znacznie szersze niż oligomery tlenku etylenu; ważną grupę wywodzą się od katecholi .
Etery koronowe silnie wiążą określone kationy, tworząc kompleksy . Atomy tlenu są dobrze usytuowane, aby koordynować z kationem znajdującym się we wnętrzu pierścienia, podczas gdy zewnętrzna część pierścienia jest hydrofobowa. Powstałe kationy często tworzą sole, które są rozpuszczalne w rozpuszczalnikach niepolarnych iz tego powodu etery koronowe są przydatne w katalizie przeniesienia fazowego . Denticity polieteru wpływa na powinowactwo eteru koronowego dla różnych kationów. Na przykład 18-korona-6 ma wysokie powinowactwo do kationu potasu, 15-korona-5 do kationu sodu, a 12-korona-4 do kationu litu. Wysokie powinowactwo 18-korona-6 do jonów potasu przyczynia się do jego toksyczności. Najmniejszy eter koronowy wciąż zdolny do wiązania kationów to 8-korona-4, a największy potwierdzony eksperymentalnie eter koronowy to 81-korona-27. Etery koronowe nie są jedynymi ligandami makrocyklicznymi, które wykazują powinowactwo do kationu potasu. Jonofory, takie jak walinomycyna, również wykazują wyraźną preferencję dla kationu potasu w stosunku do innych kationów.
Wykazano, że etery koronowe koordynują się z kwasami Lewisa poprzez oddziaływania elektrostatyczne, σ-dziurowe (patrz wiązanie halogenowe ), między zasadowymi atomami tlenu Lewisa w eterze koronowym i elektrofilowym centrum kwasu Lewisa.
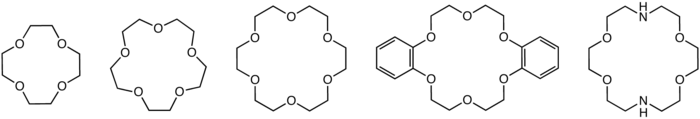 Struktury zwykłych eterów koronowych: 12-korona-4 , 15-korona-5 , 18-korona-6 , dibenzo-18-korona-6 , eter aza-korona
Struktury zwykłych eterów koronowych: 12-korona-4 , 15-korona-5 , 18-korona-6 , dibenzo-18-korona-6 , eter aza-korona
Historia
W 1967 Charles Pedersen , chemik pracujący w DuPont , odkrył prostą metodę syntezy eteru koronowego, gdy próbował przygotować środek kompleksujący dla kationów dwuwartościowych . Jego strategia polegała na połączeniu dwóch grup katecholowych przez jeden hydroksyl w każdej cząsteczce. To wiązanie definiuje ligand wielokleszczowy, który może częściowo otaczać kation i, poprzez jonizację hydroksyli fenolowych, neutralizować związane wskazanie. Był zaskoczony wyizolowaniem produktu ubocznego, który silnie skompleksował kationy potasu . Powołując się na wcześniejsze prace nad rozpuszczaniem potasu w 16-korona-4, zdał sobie sprawę, że cykliczne polietery reprezentują nową klasę czynników kompleksujących, które są zdolne do wiązania kationów metali alkalicznych . Następnie w przełomowej serii artykułów przedstawił systematyczne badania syntezy i właściwości wiążących eterów koronowych. Odkrycie eterów koronowych przyniosło korzyści w dziedzinie syntezy organicznej , katalizatorów przeniesienia fazowego i innych wschodzących dyscyplin. Pedersen szczególnie spopularyzował dibenzo etery koronowe.

Pedersen otrzymał Nagrodę Nobla w dziedzinie chemii z 1987 r. za odkrycie dróg syntezy i właściwości wiążących eterów koronowych.
Powinowactwo do kationów
Ze względu na efekt chelatowy i efekt makrocykliczny , etery koronowe wykazują silniejsze powinowactwo do różnych kationów niż ich podzielone lub acykliczne analogi. W tym przypadku selektywność kationowa dla jonów metali alkalicznych zależy głównie od wielkości i gęstości ładunku jonu oraz wielkości wnęki eteru koronowego.
| Korona Eter | Rozmiar wnęki/Å | Ulubione jony alkaliczne | Efektywne promienie jonów/Å |
|---|---|---|---|
| 12-korona-4 | 0,6-0,75 | Li + | 0,76 |
| 15-korona-5 | 0,86-0,92 | Na + | 1,02 |
| 18-korona-6 | 1,34-1,55 | K + | 1,38 |
| 21-korona-7 | 1,7-2,1 | CS + | 1,67 |
Powinowactwo danego eteru koronowego do kationów litu , sodu i potasu może zmieniać się wielokrotnie, co przypisuje się dużym różnicom w ich gęstości ładunku. Pomiędzy kationami potasu, rubidu i cezu zmiany powinowactwa są mniej zauważalne, ponieważ ich gęstość ładunku różni się mniej niż w przypadku metali alkalicznych we wcześniejszych okresach.
Oprócz wysokiego powinowactwa do kationów potasu, 18-korona-6 może również wiązać się z protonowanymi aminami i tworzyć bardzo stabilne kompleksy zarówno w roztworze, jak iw fazie gazowej. Niektóre aminokwasy , takie jak lizyna , zawierają pierwszorzędową aminę w swoich łańcuchach bocznych. Te protonowane grupy aminowe mogą wiązać się z wnęką 18-korony-6 i tworzyć stabilne kompleksy w fazie gazowej. Wiązania wodorowe powstają między trzema atomami wodoru protonowanych amin i trzema atomami tlenu 18-korona-6. Te wiązania wodorowe sprawiają, że kompleks jest stabilnym adduktem. Dzięki wprowadzeniu luminescencyjnych podstawników do ich szkieletu, związki te okazały się być czułymi sondami jonowymi, ponieważ zmiany w absorpcji lub fluorescencji grup fotoaktywnych można mierzyć dla bardzo niskich stężeń obecnego metalu. Niektóre atrakcyjne przykłady obejmują makrocykle zawierające donory tlenu i/lub azotu, które są przyłączone do związków poliaromatycznych, takich jak antracen (poprzez pozycje 9 i/lub 10) lub naftaleny (poprzez pozycje 2 i 3). Niektóre modyfikacje jonoforów barwnikowych przez etery koronowe wykazują współczynniki ekstynkcji zależne od długości łańcucha kationów w łańcuchu.
Zobacz też
Bibliografia
Zewnętrzne linki
- Pedersen, Karol (1987). „Wykład Nobla” (PDF) . Nagroda Nobla .
- Korona molekularna

