Wychwytywanie elektronów - Electron capture

Wychwytywanie elektronów ( wychwytywanie K-elektronów , również K-capture , lub wychwytywanie L-elektronów , L-capture ) to proces, w którym bogate w protony jądro elektrycznie obojętnego atomu pochłania wewnętrzny elektron atomowy , zwykle z K lub L powłoki elektronowe . Proces ten w ten sposób zmienia jądrowy proton w neutron i jednocześnie powoduje emisję neutrina elektronowego .
Ponieważ to pojedyncze emitowane neutrino niesie całą energię rozpadu , ma tę jedną charakterystyczną energię. Podobnie pęd emisji neutrin powoduje, że atom potomny odrzuca się z jednym charakterystycznym pędem.
Powstały nuklid potomny , jeśli jest w stanie wzbudzonym , przechodzi do stanu podstawowego . Zwykle podczas tego przejścia emitowane jest promieniowanie gamma , ale dewzbudzenie jądrowe może również zachodzić w wyniku konwersji wewnętrznej .
Po wychwyceniu wewnętrznego elektronu z atomu, zewnętrzny elektron zastępuje elektron, który został wychwycony iw tym procesie emitowany jest jeden lub więcej charakterystycznych fotonów promieniowania rentgenowskiego . Wychwytywanie elektronów czasami powoduje również efekt Augera , w którym elektron jest wyrzucany z powłoki elektronowej atomu w wyniku interakcji między elektronami atomu w procesie poszukiwania stanu elektronowego o niższej energii.
Po wychwytywaniu elektronów liczba atomowa zmniejsza się o jeden, liczba neutronów zwiększa się o jeden, a liczba masowa nie ulega zmianie . Proste wychwytywanie elektronów samo w sobie skutkuje powstaniem neutralnego atomu, ponieważ utrata elektronu w powłoce elektronowej jest równoważona utratą dodatniego ładunku jądrowego. Jednak dodatni jon atomowy może wynikać z dalszej emisji elektronów Augera.
Wychwytywanie elektronów jest przykładem słabego oddziaływania , jednej z czterech podstawowych sił.
Wychwytu elektronów jest podstawowym trybie zaniku dla izotopów przy względnej obfitości protonów w jądrze , ale niewystarczającą różnicy energii pomiędzy izotopu i jej przyszłego pochodny (na Isobar jednego mniej ładunek dodatni ) dla izotopu do rozpadu przez emitujące pozytrony . Wychwytywanie elektronów jest zawsze alternatywnym trybem rozpadu dla izotopów radioaktywnych , które mają wystarczającą energię do rozpadu poprzez emisję pozytonów . Wychwytywanie elektronów jest czasami zaliczane do rodzaju rozpadu beta , ponieważ podstawowy proces jądrowy, w którym pośredniczy siła słaba, jest taki sam. W fizyce jądrowej rozpad beta jest rodzajem rozpadu radioaktywnego, w którym promień beta (szybki energetyczny elektron lub pozyton) i neutrino są emitowane z jądra atomowego. Wychwytywanie elektronów jest czasami nazywane odwrotnym rozpadem beta , chociaż termin ten zwykle odnosi się do interakcji antyneutrina elektronowego z protonem.
Jeśli różnica energii między atomem macierzystym a atomem potomnym jest mniejsza niż 1,022 MeV , emisja pozytonów jest zabroniona, ponieważ energia rozpadu jest niewystarczająca, aby na to pozwolić, a zatem przechwytywanie elektronów jest jedynym trybem rozpadu. Na przykład rubid-83 (37 protonów, 46 neutronów) rozpadnie się na krypton-83 (36 protonów, 47 neutronów) wyłącznie przez wychwytywanie elektronów (różnica energii lub energia rozpadu wynosi około 0,9 MeV).
Historia
Teoria wychwytywania elektronów została po raz pierwszy omówiona przez Gian-Carlo Wick w artykule z 1934 roku, a następnie rozwinięta przez Hideki Yukawę i innych. Wychwytywanie elektronów K po raz pierwszy zaobserwował Luis Alvarez w Vanadium ,48
V
, o czym poinformował w 1937 roku. Alvarez kontynuował badania wychwytywania elektronów w galu (67
Ga
) i inne nuklidy.
Szczegóły reakcji
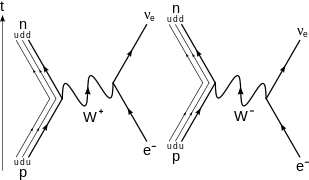
Przechwycony elektron jest jednym z własnych elektronów atomu, a nie nowym, nadchodzącym elektronem, jak mogłoby sugerować sposób zapisu powyższych reakcji. Kilka przykładów wychwytywania elektronów to:
Izotopy radioaktywne, które rozpadają się przez wychwytywanie czystego elektronu, mogą zostać powstrzymane przed rozpadem radioaktywnym, jeśli są w pełni zjonizowane (czasami do opisu takich jonów stosuje się określenie „odarte”). Przypuszcza się, że takie pierwiastki, jeśli zostaną utworzone w procesie r w wybuchających supernowych , są wyrzucane w pełni zjonizowane, a zatem nie ulegają rozpadowi radioaktywnemu, dopóki nie napotkają elektronów w przestrzeni kosmicznej. Uważa się, że anomalie w rozkładzie pierwiastków są częściowo wynikiem tego efektu wychwytywania elektronów. Rozpady odwrotne mogą być również indukowane przez pełną jonizację; na przykład,163
Ho
rozpada się w 163
Dy
przez wychwytywanie elektronów; jednak w pełni zjonizowany163
Dy
rozpada się w stan związany 163
Ho
przez proces zaniku stanu związanego β − .
Wiązania chemiczne mogą również w niewielkim stopniu wpływać na szybkość wychwytywania elektronów (na ogół mniej niż 1%) w zależności od bliskości elektronów do jądra. Na przykład w 7 Be zaobserwowano różnicę 0,9% między okresami półtrwania w środowisku metalicznym i izolacyjnym. Ten stosunkowo duży efekt wynika z faktu, że beryl jest małym atomem wykorzystującym elektrony walencyjne znajdujące się blisko jądra, a także na orbitalach bez orbitalnego momentu pędu. Elektrony na orbitalach s (niezależnie od powłoki lub pierwotnej liczby kwantowej) mają anty-węzeł prawdopodobieństwa w jądrze, a zatem są znacznie bardziej podatne na wychwytywanie elektronów niż elektrony p lub d , które mają węzeł prawdopodobieństwa w jądrze.
Wokół pierwiastków znajdujących się w środku układu okresowego , izotopy lżejsze od stabilnych izotopów tego samego pierwiastka mają tendencję do rozpadu poprzez wychwytywanie elektronów , podczas gdy izotopy cięższe od stabilnych rozpadają się poprzez emisję elektronów . Wychwytywanie elektronów ma miejsce najczęściej w cięższych pierwiastkach z niedoborem neutronów, gdzie zmiana masy jest najmniejsza i emisja pozytonów nie zawsze jest możliwa. Gdy ubytek masy w reakcji jądrowej jest większy od zera, ale mniejszy niż 2m[0-1e-], proces ten nie może zachodzić przez emisję pozytonów, ale zachodzi spontanicznie w celu wychwytu elektronów.
Typowe przykłady
Niektóre typowe radioizotopy, które rozpadają się wyłącznie przez wychwytywanie elektronów, obejmują:
|
|
|
Pełna lista znajduje się w tabeli nuklidów .
Bibliografia
Zewnętrzne linki
- „Wykres na żywo nuklidów” . Sekcja Danych Jądrowych MAEA. Wiedeń, Austria: Międzynarodowa Agencja Energii Atomowej . Źródło 16 sierpnia 2020 . z filtrem na wychwytywanie elektronów
