Jonizacja przez elektrorozpylanie - Electrospray ionization
Jonizacja przez elektrorozpylanie ( ESI ) to technika wykorzystywana w spektrometrii masowej do wytwarzania jonów za pomocą elektrorozpylania, w której wysokie napięcie jest przykładane do cieczy w celu wytworzenia aerozolu . Jest szczególnie przydatny do wytwarzania jonów z makrocząsteczek, ponieważ przezwycięża skłonność tych cząsteczek do fragmentacji podczas jonizacji. ESI różni się od innych procesów jonizacji (np. desorpcji/jonizacji laserowej wspomaganej matrycą (MALDI)) ponieważ może wytwarzać jony o wielu ładunkach, skutecznie rozszerzając zakres mas analizatora, aby pomieścić rzędy wielkości kDa-MDa obserwowane w białkach i związane z nimi fragmenty polipeptydowe.
Spektrometria masowa wykorzystująca ESI nazywana jest spektrometrią mas z jonizacją przez elektrorozpylanie (ESI-MS) lub, rzadziej, spektrometrią mas z elektrorozpylaniem (ES-MS). ESI to tak zwana technika „miękkiej jonizacji”, ponieważ fragmentacja jest bardzo niewielka. Może to być korzystne w tym sensie, że jon cząsteczkowy (a dokładniej jon pseudocząsteczkowy) jest prawie zawsze obserwowany, jednak z otrzymanego prostego widma masowego można uzyskać bardzo niewiele informacji strukturalnych. Wadę tę można przezwyciężyć, łącząc ESI z tandemową spektrometrią mas (ESI-MS/MS). Inną ważną zaletą ESI jest to, że informacje o fazie roztworu można zachować w fazie gazowej.
Technika jonizacją została po raz pierwszy opisana przez Masamichi Yamashita i John Fenn w roku 1984. Rozwój jonizacji elektrorozpylania do analizy makrocząsteczek biologicznych został nagrodzony do przyznania nagrody Nobla w dziedzinie chemii do John Bennett Fenn w roku 2002. Jednym z oryginalnych instrumentów używany przez dr. Fenna jest wystawiony w Science History Institute w Filadelfii w Pensylwanii.
Historia

W 1882 r. Lord Rayleigh teoretycznie oszacował maksymalny ładunek, jaki kropelka cieczy może przenosić, zanim wyrzuci drobne strumienie cieczy. Jest to obecnie znane jako limit Rayleigha.
W 1914 John Zeleny opublikował pracę na temat zachowania kropel płynu na końcach szklanych kapilar i przedstawił dowody na różne tryby elektrorozpylania. Wilson i Taylor i Nolan badali elektrorozpylanie w latach dwudziestych XX wieku, a Macky w 1931 roku. Stożek elektrorozpylania (obecnie znany jako stożek Taylora ) został opisany przez Sir Geoffreya Ingrama Taylora .
Pierwsze użycie jonizacji przez elektrorozpylanie ze spektrometrią mas zostało opisane przez Malcolma Dole'a w 1968 roku. John Bennett Fenn otrzymał w 2002 roku Nagrodę Nobla w dziedzinie chemii za opracowanie spektrometrii mas z jonizacją przez elektrorozpylanie pod koniec lat 80-tych.
Mechanizm jonizacji
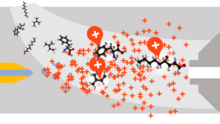
Ciecz zawierająca interesujące anality jest rozpraszana przez elektrorozpylanie w drobny aerozol. Ponieważ tworzenie jonów wiąże się z intensywnym odparowaniem rozpuszczalnika (nazywanym również desolwatacją), typowe rozpuszczalniki do jonizacji metodą elektrorozpylania wytwarza się przez zmieszanie wody z lotnymi związkami organicznymi (np. metanol acetonitryl). Aby zmniejszyć początkową wielkość kropelek, do roztworu zwykle dodaje się związki zwiększające przewodność (np. kwas octowy). Gatunki te działają również jako źródło protonów ułatwiające proces jonizacji. Elektrospray o dużym przepływie może skorzystać z nebulizacji ogrzanego gazu obojętnego, takiego jak azot lub dwutlenek węgla, oprócz wysokiej temperatury źródła ESI. Aerozol jest pobierany do pierwszego stopnia próżniowego spektrometru mas przez kapilarę przenoszącą różnicę potencjałów około 3000 V, która może być podgrzewana, aby wspomóc dalsze odparowywanie rozpuszczalnika z naładowanych kropelek. Rozpuszczalnik odparowuje z naładowanej kropli, aż stanie się niestabilny po osiągnięciu granicy Rayleigha . W tym momencie kropla odkształca się, gdy elektrostatyczne odpychanie podobnych ładunków, o stale malejącym rozmiarze, staje się silniejsze niż napięcie powierzchniowe utrzymujące kroplę razem. W tym momencie kropelka ulega rozszczepieniu kulombowskiemu, w którym pierwotna kropelka "eksploduje", tworząc wiele mniejszych, bardziej stabilnych kropelek. Nowe kropelki ulegają desolwatacji, a następnie dalszym rozszczepieniom kulombowskim. Podczas rozszczepienia kropla traci niewielki procent swojej masy (1,0–2,3%) wraz ze stosunkowo dużym procentem ładunku (10–18%).
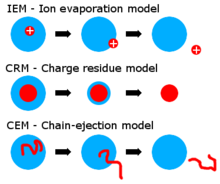
Istnieją dwie główne teorie, które wyjaśniają ostateczną produkcję jonów w fazie gazowej: model parowania jonów (IEM) i model pozostałości ładunku (CRM). IEM sugeruje, że gdy kropla osiąga pewien promień, natężenie pola na powierzchni kropli staje się wystarczająco duże, aby wspomóc desorpcję pola solwatowanych jonów. CRM sugeruje, że kropelki elektrorozpylania przechodzą cykle odparowywania i rozszczepiania, prowadząc ostatecznie do kropelek potomnych, które zawierają średnio jeden jon analitu lub mniej. Jony w fazie gazowej tworzą się po odparowaniu pozostałych cząsteczek rozpuszczalnika, pozostawiając analit z ładunkami przenoszonymi przez kropelkę.
Wiele dowodów wskazuje bezpośrednio lub pośrednio, że małe jony (z małych cząsteczek ) są uwalniane do fazy gazowej poprzez mechanizm parowania jonów, podczas gdy większe jony (na przykład z pofałdowanych białek) tworzą się przez mechanizm naładowanych pozostałości.
Zaproponowano trzeci model wykorzystujący łączną naładowaną emisję z pola pozostałości. Dla nieuporządkowanych polimerów (niesfałdowanych białek) zaproponowano inny model, zwany modelem wyrzutu łańcucha (CEM).
Jony obserwowane przez spektrometrię mas mogą być jonami quasimolekularnymi utworzonymi przez dodanie kationu wodorowego i oznaczone jako [ M + H] + lub innego kationu, takiego jak jon sodu , [ M + Na] + , lub usunięcie jądra wodoru , [ M -H] - . Często obserwuje się wielokrotnie naładowane jony, takie jak [ M + n H] n + . W przypadku dużych makrocząsteczek może występować wiele stanów ładunku, co skutkuje charakterystyczną obwiednią stanu ładunku. Wszystko to są rodzaje jonów parzystych elektronów: elektrony (same) nie są dodawane ani usuwane, w przeciwieństwie do niektórych innych źródeł jonizacji. Anality są czasami zaangażowane w procesy elektrochemiczne , co prowadzi do przesunięć odpowiednich pików w widmie masowym . Efekt ten przejawia się w bezpośredniej jonizacji metali szlachetnych, takich jak miedź, srebro i złoto, przy użyciu elektrorozpylania.
Wydajność generowania jonów fazy gazowej dla małych cząsteczek w ESI różni się w zależności od struktury związku, użytego rozpuszczalnika i parametrów instrumentalnych. Różnice w wydajności jonizacji sięgają ponad 1 milion razy.
Warianty
Elektrorozpylacze pracujące przy niskich natężeniach przepływu generują znacznie mniejsze początkowe kropelki, co zapewnia lepszą wydajność jonizacji . W 1993 Gale i Richard D. Smith donieśli, że znaczny wzrost czułości można osiągnąć przy niższych prędkościach przepływu, aż do 200 nl/min. W 1994 roku dwie grupy badawcze ukuły nazwę micro-electrospray (mikrospray) dla elektrorozpylaczy pracujących przy niskich natężeniach przepływu. Emmett i Caprioli wykazali lepszą wydajność analiz HPLC-MS, gdy elektrorozpylanie pracowało z prędkością 300–800 nl/min. Wilm i Mann wykazali, że przepływ kapilarny ~ 25 nL/min może podtrzymać elektrorozpylanie na końcówkach emiterów wytwarzanych przez przyciąganie szklanych kapilar do kilku mikrometrów. Ten ostatni został przemianowany na nano-elektrorozpylanie (nanospray) w 1996 roku. Obecnie nazwa nanospray jest również używana do elektrorozpylania zasilanego przez pompy przy niskich natężeniach przepływu, nie tylko do elektrorozpylaczy samozasilających. Chociaż może nie istnieć dobrze zdefiniowany zakres natężenia przepływu dla elektrorozpylania, mikrorozpylania i nanoelektrorozpylania, zbadali „zmiany w podziale analitu podczas rozszczepiania kropel przed uwolnieniem jonów”. W niniejszej pracy porównują wyniki uzyskane przez trzy inne grupy. a następnie zmierzyć stosunek natężenia sygnału [Ba 2+ + Ba + ]/[BaBr + ] przy różnych natężeniach przepływu.
Jonizacja na zimno jest formą elektrorozpylania, w której roztwór zawierający próbkę jest wtłaczany przez małą zimną kapilarę (10–80 °C) do pola elektrycznego w celu wytworzenia delikatnej mgiełki zimnych naładowanych kropelek. Zastosowania tej metody obejmują analizę delikatnych cząsteczek i interakcji gość-gospodarz, których nie można badać za pomocą zwykłej jonizacji elektrorozpylania.
Jonizację przez elektrorozpylanie osiągnięto również przy ciśnieniu tak niskim jak 25 tor i nazwano ją jonizacją pod ciśnieniem pod ciśnieniem atmosferycznym za pomocą nanoelektrorozpylania (SPIN) w oparciu o dwustopniowy interfejs lejka jonowego opracowany przez Richarda D. Smitha i współpracowników. Implementacja SPIN zapewniła zwiększoną czułość dzięki zastosowaniu lejków jonowych, które pomogły ograniczyć i przenieść jony do obszaru o niższym ciśnieniu spektrometru mas. Emiter nanoelektrorozpylania zbudowany jest z cienkiej kapilary o małym otworze około 1–3 mikrometrów. Aby zapewnić wystarczającą przewodność, kapilara ta jest zwykle pokryta materiałem przewodzącym, np. złotem. Jonizacja nanoelektrorozpylaniem zużywa tylko kilka mikrolitrów próbki i tworzy mniejsze kropelki. Praca przy niskim ciśnieniu była szczególnie skuteczna w przypadku niskich prędkości przepływu, gdzie mniejsza wielkość kropelek elektrorozpylania umożliwiała skuteczną desolwatację i tworzenie jonów. W rezultacie naukowcom udało się później wykazać osiągnięcie ponad 50% ogólnej wydajności wykorzystania jonizacji do przenoszenia jonów z fazy ciekłej do fazy gazowej w postaci jonów oraz przez interfejs podwójnego lejka jonowego do spektrometru mas.
Jonizacja otoczenia
W przypadku jonizacji otoczenia tworzenie jonów następuje poza spektrometrem mas bez przygotowania próbki. Elektrospray jest używany do tworzenia jonów w wielu źródłach jonów otoczenia.
Desorpcyjna jonizacja przez elektrorozpylanie (DESI) to technika jonizacji w otoczeniu , w której elektrorozpylanie rozpuszczalnika jest kierowane na próbkę. Elektrorozpylanie jest przyciągane do powierzchni przez przyłożenie napięcia do próbki. Związki próbki są ekstrahowane do rozpuszczalnika, który jest ponownie aerozolowany jako silnie naładowane kropelki, które odparowują, tworząc wysoce naładowane jony. Po jonizacji jony wchodzą do interfejsu ciśnienia atmosferycznego spektrometru mas. DESI pozwala na jonizację próbek w otoczeniu pod ciśnieniem atmosferycznym, przy niewielkim przygotowaniu próbki.
Ekstrakcyjna jonizacja elektrorozpylania to metoda jonizacji w otoczeniu typu spray, która wykorzystuje dwa połączone rozpylenia, z których jeden jest generowany przez elektrorozpylanie.
Oparta na laserze jonizacja otoczenia oparta na elektrorozpylaniu to dwuetapowy proces, w którym impulsowy laser jest używany do desorbowania lub usuwania materiału z próbki, a chmura materiału oddziałuje z elektrorozpylaniem, tworząc jony. W przypadku jonizacji w otoczeniu materiał próbki jest osadzany na tarczy w pobliżu elektrorozpylania. Laser desorbuje lub usuwa materiał z próbki, która jest wyrzucana z powierzchni do elektrosprayu, który wytwarza silnie naładowane jony. Przykładami są elektrorozpylanie jonizacja przez desorpcję promieniowaniem laserowym , matryca z desorpcją laserową z jonizacją przez elektrorozpylanie , i ablacja laserowa z jonizacją przez elektrorozpylanie .
Jonizacja elektrostatyczna (ESTASI) obejmowała analizę próbek znajdujących się na płaskiej lub porowatej powierzchni lub wewnątrz mikrokanału. Kropelka zawierająca anality jest osadzana na obszarze próbki, do którego przykłada się pulsacyjne wysokie napięcie. Gdy ciśnienie elektrostatyczne jest większe niż napięcie powierzchniowe, rozpylane są kropelki i jony.
Wtórna jonizacja przez elektrorozpylanie (SESI) to metoda natryskowa, jonizacja otoczenia, w której jony ładujące są wytwarzane za pomocą elektrorozpylania. Jony te następnie ładują cząsteczki pary w fazie gazowej, gdy się z nimi zderzają.
W przypadku jonizacji w sprayu papierowym próbka jest nakładana na kawałek papieru, dodawany jest rozpuszczalnik, a na papier przykładane jest wysokie napięcie, tworząc jony.
Aplikacje
Elektrospray służy do badania fałdowania białek .
Chromatografia cieczowa – spektrometria mas
Jonizacja przez elektrorozpylanie jest preferowanym źródłem jonów do sprzężenia chromatografii cieczowej ze spektrometrią mas (LC-MS). Analizę można przeprowadzić w trybie online, wprowadzając ciecz eluowaną z kolumny LC bezpośrednio do elektrorozpylania, lub w trybie offline, zbierając frakcje do późniejszej analizy w klasycznej konfiguracji z nanoelektrorozpylaniem i spektrometrią mas. Wśród wielu parametrów operacyjnych w ESI-MS dla białek, napięcie elektrorozpylania zostało zidentyfikowane jako ważny parametr do rozważenia w elucji gradientowej ESI LC/MS. Wpływ różnych kompozycji rozpuszczalników (takich jak TFA lub octan amonu, odczynniki doładowujące lub grupy derywatyzujące) lub warunki rozpylania na widma elektrorozpylania-LCMS i/lub widma nanoESI-MS. Zostały zbadane.
Elektroforeza kapilarna-spektrometria mas (CE-MS)
Elektroforeza kapilarna-spektrometria mas została umożliwiona przez interfejs ESI, który został opracowany i opatentowany przez Richarda D. Smitha i współpracowników z Pacific Northwest National Laboratory i okazał się mieć szerokie zastosowanie do analizy bardzo małych mieszanin związków biologicznych i chemicznych, a nawet rozszerzania do pojedynczej komórki biologicznej.
Niekowalencyjne oddziaływania w fazie gazowej
Jonizacja przez elektrorozpylanie jest również wykorzystywana do badania niekowalencyjnych interakcji w fazie gazowej. Uważa się, że proces elektrorozpylania umożliwia przenoszenie niekowalencyjnych kompleksów fazy ciekłej do fazy gazowej bez zakłócania oddziaływania niekowalencyjnego. Problemy, takie jak niespecyficzne interakcje, zostały zidentyfikowane podczas badania kompleksów ligand-substrat metodą ESI-MS lub nanoESI-MS. Ciekawym tego przykładem jest badanie interakcji między enzymami a lekami będącymi inhibitorami enzymu. Badania konkurencji między STAT6 a inhibitorami wykorzystały ESI jako sposób na przeszukiwanie potencjalnych nowych kandydatów na leki.
Zobacz też
- Sonda jonizacji elektrorozpylania
- Ablacja laserowa jonizacja elektrorozpylania
- Sonic spray jonizacja
Bibliografia
Dalsza lektura
- Cole, Richard (1997). Spektrometria mas z jonizacją przez elektrorozpylanie: podstawy, oprzyrządowanie i zastosowania . Nowy Jork: Wiley. Numer ISBN 978-0-471-14564-6.
- Gross, Michael; Pramanik, Birendra N.; Ganguly, AK (2002). Stosowana spektrometria mas z elektrorozpylaniem . Nowy Jork, NY: Marcel Dekker. Numer ISBN 978-0-8247-0618-0.
- Snyder, A. Peter (1996). Biochemiczne i biotechnologiczne zastosowania spektrometrii masowej z jonizacją przez elektrorozpylanie . Columbus, Ohio: Amerykańskie Towarzystwo Chemiczne. Numer ISBN 978-0-8412-3378-2.
- Aleksandrow, ML; LN gal; NV Krasnov; VI Nikołajew; WA Pawlenko; VA Shkurov (lipiec 1984). Экстракция ионов из растворов при атмосферном давлении – Метод масс-спектрометрического анализа биорганиещески[Ekstrakcja jonów z roztworów pod ciśnieniem atmosferycznym - Metoda analizy spektrometrii masowej substancji bioorganicznych]. Doklady Akademii Nauk SSSR (po rosyjsku). 277 (2): 379-383.
- Aleksandrow, ML; LN gal; NV Krasnov; VI Nikołajew; WA Pawlenko; VA Shkurov (2008) [lipiec 1984]. „Ekstrakcja jonów z roztworów pod ciśnieniem atmosferycznym jako metoda analizy spektrometrii masowej związków bioorganicznych”. Szybka komunikacja w spektrometrii masowej . 22 (3): 267–270. Kod bib : 2008RCMS...22..267A . doi : 10.1002/rcm.3113 . PMID 18181250 .
Zewnętrzne linki
- Elektrorozpylanie podkładu jonizującego Krajowe laboratorium wysokiego pola magnetycznego
- Elektrorozpylanie + jonizacja + spektrometria masowa + w Narodowej Bibliotece Medycznej USA Medical Subject Headings (MeSH)