Rozszerzony układ okresowy - Extended periodic table
| Część serii na |
| Układ okresowy |
|---|
An wydłużone Okresowego przypuszcza o pierwiastków innych niż te obecnie znane ze okresowego i sprawdzony, do oganesson , który uzupełnia siódmego okresu (wiersz) w okresowym z liczbą atomową ( Z ), 118. 2021, brak elementów z powodzeniem zsyntetyzowano wyższą liczbę atomową niż oganesson; wszystkie elementy w ósmym okresie i później pozostają więc czysto hipotetyczne.
W przypadku odkrycia kolejnych pierwiastków o wyższych niż ta liczbach atomowych, zostaną one umieszczone w dodatkowych okresach, ułożonych (jak w okresach istniejących) w celu zilustrowania okresowo powtarzających się tendencji we właściwościach danych pierwiastków. Oczekuje się, że wszelkie dodatkowe okresy będą zawierać większą liczbę pierwiastków niż okres siódmy, ponieważ oblicza się, że mają dodatkowy tzw. blok g , zawierający co najmniej 18 pierwiastków z częściowo wypełnionymi orbitalami g w każdym okresie. Ośmiookresowa tablica zawierająca ten blok została zasugerowana przez Glenna T. Seaborga w 1969 roku. Pierwszy element g-bloku może mieć liczbę atomową 121, a zatem miałby systematyczną nazwę unbiunium . Mimo wielu poszukiwań żadne pierwiastki z tego regionu nie zostały zsyntetyzowane ani odkryte w przyrodzie.
Zgodnie z przybliżeniem orbitalnym w opisach mechaniki kwantowej struktury atomowej, blok g odpowiadałby pierwiastkom z częściowo wypełnionymi orbitami g, ale efekty sprzężenia spinowo- orbitalnego znacznie zmniejszają wiarygodność przybliżenia orbitalnego dla pierwiastków o dużej liczbie atomowej. Podczas gdy wersja Seaborga przedłużonego okresu zawierała cięższe elementy na wzór lżejszych elementów, ponieważ nie uwzględniała efektów relatywistycznych , modele uwzględniające efekty relatywistyczne nie. Pekka Pyykkö i Burkhard Fricke wykorzystali modelowanie komputerowe do obliczenia pozycji elementów do Z = 172 i stwierdzili, że kilka z nich zostało przesuniętych z reguły Madelunga . Ze względu na niepewność i zmienność przewidywań właściwości chemicznych i fizycznych pierwiastków powyżej 120, obecnie nie ma zgody co do ich umieszczenia w rozszerzonym układzie okresowym.
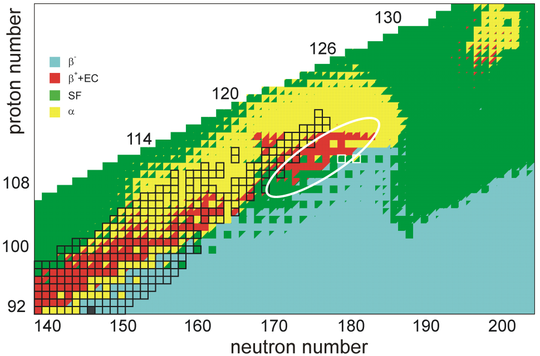
Pierwiastki w tym regionie prawdopodobnie są wysoce niestabilne w odniesieniu do rozpadu radioaktywnego i ulegają rozpadowi alfa lub spontanicznemu rozszczepieniu z wyjątkowo krótkim okresem półtrwania , chociaż przypuszcza się , że pierwiastek 126 znajduje się na wyspie stabilności, która jest odporna na rozszczepienie, ale nie na alfa rozkład. Możliwe są również inne wyspy stabilności poza znanymi elementami, w tym jedna teoretycznie wokół elementu 164, chociaż zakres efektów stabilizujących z zamkniętych powłok jądrowych jest niepewny. Nie jest jasne, ile pierwiastków poza oczekiwaną wyspą stabilności jest fizycznie możliwych, czy okres 8 jest zakończony, czy też jest okres 9. Międzynarodowa Unia Chemii Czystej i Stosowanej (IUPAC) definiuje pierwiastek, który ma istnieć, jeśli jego żywotność jest dłuższy niż 10-14 sekund (0,01 pikosekundy lub 10 femtosekund), czyli czas, w którym jądro utworzy chmurę elektronów .
Już w 1940 r. zauważono, że uproszczona interpretacja relatywistycznego równania Diraca natrafia na problemy z orbitalami elektronowymi przy Z > 1/α ≈ 137, co sugeruje, że neutralne atomy nie mogą istnieć poza pierwiastkiem 137, oraz że układ okresowy pierwiastków oparty na na orbitalach elektronowych zatem załamuje się w tym miejscu. Z drugiej strony, bardziej rygorystyczna analiza oblicza analogiczną granicę jako Z ≈ 173, gdzie podpowłoka 1s zanurza się w morzu Diraca , i że zamiast tego to nie neutralne atomy nie mogą istnieć poza pierwiastkiem 173, ale gołe jądra, co oznacza, że nie przeszkoda w dalszej rozbudowie systemu okresowego. Atomy przekraczające tę krytyczną liczbę atomową nazywane są atomami nadkrytycznymi .
Historia
Po raz pierwszy zaproponowano istnienie cięższych pierwiastków poza aktynowcami już w 1895 roku, kiedy duński chemik Hans Peter Jørgen Julius Thomsen przewidział, że tor i uran tworzą część okresu 32 pierwiastków, który kończy się na nieaktywnym chemicznie pierwiastku o masie atomowej 292 ( niedaleko od 294 znanego dzisiaj pierwszego i jedynego odkrytego izotopu oganessonu ). W 1913 szwedzki fizyk Johannes Rydberg podobnie przewidział, że następny po radonie gaz szlachetny będzie miał liczbę atomową 118 i czysto formalnie wyprowadzi jeszcze cięższe kongenery radonu przy Z = 168, 218, 290, 362 i 460, dokładnie tam, gdzie Aufbau zasada przewidziała, że tak będzie. Niels Bohr przewidział w 1922 r. strukturę elektronową tego kolejnego gazu szlachetnego przy Z = 118 i zasugerował, że powodem, dla którego pierwiastki poza uranem nie były widoczne w naturze, było to, że były zbyt niestabilne. Niemiecki fizyk i inżynier Richard Swinne opublikował w 1926 r. artykuł przeglądowy zawierający przewidywania dotyczące pierwiastków transuranowych (być może ukuł ten termin), w którym przewidział współczesne przewidywania wyspy stabilności : od 1914 r. zakładał, że okresy półtrwania nie powinny zmniejszać się ściśle wraz z liczbą atomową, ale zamiast tego zasugerowali, że mogą istnieć pewne dłużej żyjące pierwiastki przy Z = 98-102 i Z = 108-110 i spekulowali, że takie pierwiastki mogą istnieć w jądrze Ziemi , w meteorytach żelaznych lub w lodowych czap Grenlandii, gdzie zostali zamknięci przed ich domniemanym kosmicznym pochodzeniem. Do 1955 elementy te zostały nazwane elementami superciężkimi .
Pierwsze przewidywania dotyczące właściwości nieodkrytych pierwiastków superciężkich zostały wykonane w 1957 roku, kiedy po raz pierwszy zbadano koncepcję powłok jądrowych i wysunięto teorię, że wokół pierwiastka 126 istnieje wyspa stabilności. W 1967 roku przeprowadzono bardziej rygorystyczne obliczenia i wyspę stabilności teoretycznie miał być wyśrodkowany na nieodkrytym wówczas flerowu (element 114); te i inne późniejsze badania zmotywowały wielu badaczy do poszukiwania superciężkich pierwiastków w przyrodzie lub próby ich syntezy w akceleratorach. W latach 70. przeprowadzono wiele poszukiwań superciężkich pierwiastków, wszystkie z negatywnymi wynikami. Od grudnia 2018 r. podjęto próbę syntezy dla każdego pierwiastka aż do unbiseptium ( Z = 127), z wyjątkiem unbitrium ( Z = 123), przy czym najcięższym z powodzeniem zsyntetyzowanym pierwiastkiem był oganesson w 2002 r., a najnowszym odkryciem jest tennessine w 2010.
Ponieważ przewidywano, że niektóre superciężkie pierwiastki leżą poza siedmiookresowym układem okresowym, dodatkowy ósmy okres zawierający te pierwiastki został po raz pierwszy zaproponowany przez Glenna T. Seaborga w 1969 roku. Model ten kontynuował wzór w ustalonych pierwiastkach i wprowadził nowy g-blok i szereg superaktynowców rozpoczynający się od pierwiastka 121, zwiększając liczbę pierwiastków w okresie 8 w porównaniu do znanych okresów. Te wczesne obliczenia nie uwzględniały jednak efektów relatywistycznych, które przełamują okresowe trendy i uniemożliwiają prostą ekstrapolację. W 1971 Fricke obliczył układ okresowy do Z = 172 i odkrył, że niektóre pierwiastki rzeczywiście mają inne właściwości, które łamią ustalony wzorzec, a obliczenia Pekki Pyykkö z 2010 r. również wykazały , że kilka pierwiastków może zachowywać się inaczej niż oczekiwano. Nie wiadomo, jak daleko układ okresowy może wykraczać poza znane 118 pierwiastków, ponieważ przewiduje się, że cięższe pierwiastki będą coraz bardziej niestabilne. Glenn T. Seaborg zasugerował, że praktycznie rzecz biorąc, koniec układu okresowego może nastąpić już w okolicach Z =120 z powodu niestabilności jądrowej.
Przewidywane struktury rozszerzonego układu okresowego
Obecnie nie ma zgody co do umieszczania pierwiastków powyżej liczby atomowej 120 w układzie okresowym pierwiastków.
Wszystkie te hipotetyczne nieodkryte pierwiastki są nazwane przez Międzynarodową Unię Chemii Czystej i Stosowanej (IUPAC) standard nazewnictwa pierwiastków systematycznych, który tworzy ogólną nazwę do użytku do czasu odkrycia, potwierdzenia i oficjalnej nazwy pierwiastka. Nazwy te zazwyczaj nie są używane w literaturze i są określane przez ich liczby atomowe; stąd element 164 nie byłby zwykle nazywany „unhexquadium” lub „Uhq” (systematyczna nazwa i symbol IUPAC), ale raczej „element 164” z symbolem „164”, „(164)” lub „E164”.
Zasada Aufbau
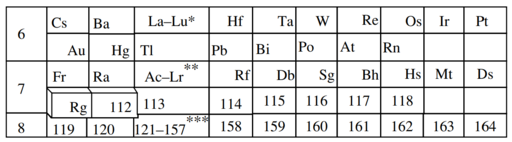
W elemencie 118 orbitale 1s, 2s, 2p, 3s, 3p, 3d, 4s, 4p, 4d, 4f, 5s, 5p, 5d, 5f, 6s, 6p, 6d, 7s i 7p są wypełnione pozostałe orbitale niewypełnione. Prosta ekstrapolacja z zasady Aufbau przewidziałaby, że ósmy rząd wypełni orbitale w kolejności 8s, 5g, 6f, 7d, 8p; ale po elemencie 120 bliskość powłok elektronowych sprawia, że umieszczenie w prostym stole jest problematyczne.
| 1 | 1 godz |
2 On |
||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2 | 3 Li |
4 Be |
5 Ł |
6 stopni |
7 N |
8 O |
9 F |
10 Ne |
||||||||||||||||||||||||||||||||||||||||||
| 3 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 godz |
16 S |
17 Cl |
18 Ar |
||||||||||||||||||||||||||||||||||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 kr |
25 mln |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 Jako |
34 Se |
35 Br |
36 kr |
||||||||||||||||||||||||||||||||
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 mies |
43 Tc |
44 Ruy |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 cali |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe |
||||||||||||||||||||||||||||||||
| 6 | 55 Cs |
56 Ba |
57 La |
58 Ce |
59 Pr |
60 Nd |
61 po południu |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 dyń |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 pkt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 pkt |
85 At |
86 Rn |
||||||||||||||||||
| 7 | 87 Fr |
88 Ra |
89 Ac |
90 Th |
91 Pa |
92 godz |
93 Np |
94 Pu |
95 rano |
96 cm² |
97 Bk |
98 Por |
99 Es |
100 FM |
101 Md |
102 Nie |
103 Lr |
104 Rf |
105 db |
106 Sg |
107 Bh |
108 godz |
109 mln ton |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 mc |
116 Lwów |
117 Ts |
118 Og |
||||||||||||||||||
| 8 | 119 Uue |
120 Ubn |
121 Ubu |
122 Ubb |
123 Ubt |
124 Ubq |
125 Ubp |
126 UBH |
127 Ubs |
128 Ubo |
129 Ube |
130 Ut |
131 Utu |
132 Utb |
133 Utt |
134 Utq |
135 UTP |
136 Uth |
137 UTS |
138 Uto |
139 Ute |
140 Uqn |
141 Uqu |
142 Uqb |
143 Uqt |
144 Uqq |
145 Uqp |
146 Uqh |
147 Uqs |
148 Uqo |
149 Uqe |
150 Upn |
151 Upu |
152 Upb |
153 Upt |
154 Upq |
155 Upp |
156 UPH |
157 wzlotów |
158 Upo |
159 Upe |
160 Uhn |
161 Uhu |
162 Uhb |
163 UHT |
164 UHQ |
165 Uhp |
166 Uhh |
167 UHS |
168 Uho |
Pyykkö
Nie wszystkie modele pokazują wyższe elementy na wzór lżejszych elementów. Pekka Pyykkö , na przykład, zastosował modelowanie komputerowe do obliczenia pozycji pierwiastków do Z = 172 i ich możliwych właściwości chemicznych w artykule opublikowanym w 2011 roku. Odkrył, że kilka pierwiastków zostało przesuniętych z zasady porządkowania energii Madelunga w wyniku nakładające się orbitale; jest to spowodowane rosnącą rolą efektów relatywistycznych w ciężkich pierwiastkach.
Fricke
Burkhard Fricke i in., którzy przeprowadzili obliczenia do pierwiastka 184 w artykule opublikowanym w 1971, również stwierdzili, że pewne elementy zostały przesunięte z zasady Aufbaua jako konsekwencja efektów relatywistycznych.
| h | On | |||||||||||||||||||||||||||||||
| Li | Być | b | C | n | O | F | Ne | |||||||||||||||||||||||||
| Na | Mg | Glin | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Współ | Ni | Cu | Zn | Ga | Ge | Jak | Se | Br | Kr | |||||||||||||||
| Rb | Sr | Tak | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Płyta CD | w | Sn | Sb | Te | i | Xe | |||||||||||||||
| Cs | Ba | La | Ce | Pr | NS | Po południu | Sm | Eu | Bóg | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Odnośnie | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | Na | Rn | |
| Fr | Ra | Ac | NS | Rocznie | U | Np | Pu | Jestem | Cm | Bk | cf | Es | Fm | Md | Nie | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 119 | 120 | 121 | 122–141 | 142 | 143 | 144 | 145 | 146 | 147 | 148 | 149 | 150 | 151 | 152 | 153 | 154 | 155 | 156 | 157 | 158 | 159 | 160 | 161 | 162 | 163 | 164 | ||||||
| 165 | 166 | 167 | 168 | 169 | 170 | 171 | 172 |
Nefiedov
Nefedov , Trzhaskovskaya i Yarzhemskii przeprowadzili obliczenia do 164 (wyniki opublikowane w 2006 roku). W przeciwieństwie do Pyykkö, a także Fricke et al., uważali pierwiastki od 158 do 164 za homologi grup od 4 do 10, a nie od 6 do 12, zauważając podobieństwa konfiguracji elektronów do metali przejściowych okresu piątego. Elementy 111 i 112 są odsunięte od płaszczyzny, aby odzwierciedlić różne konfiguracje od Au i Hg.
Kulsza
Chemik obliczeniowy Andrey Kulsha zaproponował dwie formy rozszerzonego układu okresowego. Na podstawie ich prawdopodobnych właściwości chemicznych, pierwiastki 157-172 są umieszczane jako kongenery ósmego okresu od itru do ksenonu w piątym okresie; jest to zgodne z obliczeniami Nefedova i in. z 2006 roku. W pierwszej sugestii Kulshy (2011, po publikacji artykułu Pyykkö), pierwiastki 121–138 i 139–156 są umieszczone w dwóch oddzielnych rzędach (razem nazywanych „elementami przejścia”), połączonych dodaniem podpowłoki 5g 18 do rdzenia, ponieważ odpowiednio naśladują lantanowce i aktynowce. W jego drugiej propozycji (2016) pierwiastki 121–142 tworzą blok g (ponieważ mają aktywność 5 g), podczas gdy pierwiastki 143–156 tworzą blok f umieszczony pod aktynem przez nobel.
Wyszukiwanie nieodkrytych elementów
Próby syntezy
Podejmowano nieudane próby syntezy pierwiastków z okresu 8 aż do unbiseptium, z wyjątkiem unbitrium. Próby syntezy ununennium, pierwszego okresu 8 elementu, trwają od 2021 roku.
Ununennium
Syntezę ununennium podjęto po raz pierwszy w 1985 roku, bombardując cel einsteinium-254 jonami wapnia -48 w akceleratorze superHILAC w Berkeley w Kalifornii:
-
254
99Es
+ 48
20Ca
→ 302
119Uue
* → brak atomów
Nie zidentyfikowano żadnych atomów, co doprowadziło do granicznego przekroju 300 nb . Późniejsze obliczenia sugerują, że przekrój poprzeczny reakcji 3n (która dałaby 299 Uue i trzy neutrony jako produkty) byłby w rzeczywistości sześćset tysięcy razy mniejszy niż górna granica, przy 0,5 pb.
Ponieważ ununennium jest najlżejszym nieodkrytym pierwiastkiem, w ostatnich latach było celem eksperymentów syntezy zarówno niemieckich, jak i rosyjskich zespołów. Rosyjskie eksperymenty przeprowadzono w 2011 roku i nie opublikowano żadnych wyników, co wyraźnie sugeruje, że nie zidentyfikowano atomów ununennium. Od kwietnia do września 2012 r. podjęto próbę syntezy izotopów 295 Uue i 296 Uue, bombardując cel z berkelu -249 tytanem -50 w GSI Helmholtz Center for Heavy Ion Research w Darmstadt w Niemczech. Na podstawie przewidywanego teoretycznie przekroju oczekiwano, że atom unennium zostanie zsyntetyzowany w ciągu pięciu miesięcy od rozpoczęcia eksperymentu.
-
249
97Bk
+ 50
22Ti
→ 299
119Uue
* → 296
119Uue
+ 3 1
0
n
-
249
97Bk
+ 50
22Ti
→ 299
119Uue
* → 295
119Uue
+ 4 1
0
n
Eksperyment planowano początkowo kontynuować do listopada 2012 r., ale przerwano go wcześniej, aby wykorzystać cel 249 Bk do potwierdzenia syntezy tennessine (w ten sposób zmieniając pociski na 48 Ca). Przewiduje się, że ta reakcja pomiędzy 249 Bk i 50 Ti jest najbardziej korzystną praktyczną reakcją dla powstania unennium, ponieważ jest raczej asymetryczna, choć również nieco zimna. (Reakcja pomiędzy 254 Es i 48 Ca byłaby lepsza, ale przygotowanie miligramowych ilości 254 Es dla celu jest trudne.) Niemniej jednak konieczna zmiana ze „srebrnego pocisku” 48 Ca na 50 Ti dzieli oczekiwany plon z unennium o około dwudziestu, ponieważ wydajność silnie zależy od asymetrii reakcji fuzji.
Ze względu na przewidywane krótkie okresy półtrwania zespół GSI zastosował nową „szybką” elektronikę zdolną do rejestrowania zdarzeń rozpadu w ciągu mikrosekund. Nie zidentyfikowano atomów ununennium, co oznacza graniczny przekrój 70 fb. Przewidywany rzeczywisty przekrój wynosi około 40 fb, co jest na granicy obecnej technologii.
Zespół Wspólnego Instytutu Badań Jądrowych w Dubnej w Rosji planował rozpoczęcie eksperymentów nad syntezą ununennium i unbinilium przy użyciu reakcji 249 Bk+ 50 Ti i 249 Cf+ 50 Ti w 2019 roku przy użyciu nowego kompleksu doświadczalnego. Zespół RIKEN w Japonii planował również wykonanie prób na tych elementach począwszy od 2018 roku z celami 248 Cm przy użyciu reakcji 248 Cm+ 51 V i 248 Cm+ 54 Cr. Ta pierwsza działa od czerwca 2018 roku.
Unbinilium
Po sukcesie w uzyskaniu oganessonu w wyniku reakcji między 249 Cf a 48 Ca w 2006 roku, zespół Wspólnego Instytutu Badań Jądrowych (ZIBJ) w Dubnej rozpoczął podobne eksperymenty w marcu-kwietniu 2007 roku, mając nadzieję na stworzenie unbinilium (pierwiastek 120). z jąder 58 Fe i 244 Pu . Przewiduje się, że izotopy unbinilium mają okresy połowicznego rozpadu alfa rzędu mikrosekund . Wstępna analiza wykazała, że nie wytworzono żadnych atomów unbinilium, co zapewnia granicę 400 fb dla przekroju poprzecznego przy badanej energii.
-
244
94Pu
+ 58
26Fe
→ 302
120Ubn
* → brak atomów
Rosyjski zespół planował zmodernizować swoje obiekty przed ponowną próbą reakcji.
W kwietniu 2007 r. zespół w GSI Helmholtz Center for Heavy Jon Research w Darmstadt w Niemczech podjął próbę stworzenia unbinilium przy użyciu uranu -238 i niklu -64:
-
238
92U
+ 64
28Ni
→ 302
120Ubn
* → brak atomów
Nie wykryto żadnych atomów, co zapewnia granicę 1,6 pb dla przekroju poprzecznego przy dostarczonej energii. GSI powtórzył eksperyment z wyższą czułością w trzech oddzielnych seriach w okresie kwiecień-maj 2007, styczeń-marzec 2008 i wrzesień-październik 2008, wszystkie z negatywnymi wynikami, osiągając granicę przekroju poprzecznego 90 fb.
W czerwcu-lipcu 2010 r. i ponownie w 2011 r., po unowocześnieniu swojego sprzętu, aby umożliwić stosowanie bardziej radioaktywnych celów, naukowcy z GSI podjęli próbę bardziej asymetrycznej reakcji fuzji:
-
248
96Cm
+ 54
24Cr
→ 302
120Ubn
* → brak atomów
Spodziewano się, że zmiana reakcji pięciokrotnie zwiększy prawdopodobieństwo syntezy unbinilium, ponieważ wydajność takich reakcji silnie zależy od ich asymetrii. Zaobserwowano trzy skorelowane sygnały, które pasowały do przewidywanych energii rozpadu alfa 299 Ubn i jej córki 295 Og, a także eksperymentalnie znanej energii rozpadu jej wnuczki 291 Lv . Jednak czas życia tych możliwych rozpadów był znacznie dłuższy niż oczekiwano, a wyników nie można było potwierdzić.
W sierpniu i październiku 2011 r. inny zespół w GSI korzystający z obiektu TASCA wypróbował nową, jeszcze bardziej asymetryczną reakcję:
-
249
98cf
+ 50
22Ti
→ 299
120Ubn
* → brak atomów
Ze względu na asymetrię przewidywano , że reakcja pomiędzy 249 Cf i 50 Ti jest najbardziej korzystną praktyczną reakcją do syntezy unbinilium, chociaż jest również nieco zimna. Nie zidentyfikowano atomów unbinilium, co oznacza graniczny przekrój 200 fb. Jens Volker Kratz przewidział, że rzeczywisty maksymalny przekrój do wytwarzania unbinilium w którejkolwiek z tych reakcji wynosi około 0,1 fb; dla porównania rekord świata dla najmniejszego przekroju udanej reakcji wyniósł 30 fb dla reakcji 209 Bi( 70 Zn,n) 278 Nh , a Kratz przewidział maksymalny przekrój 20 fb dla wytworzenia sąsiedniego unennium. Jeśli te przewidywania są trafne, synteza ununennium byłaby na granicy obecnej technologii, a synteza unbinilium wymagałaby nowych metod.
Unbinium
Syntezę unbiunium została pierwsza próba w 1977 roku przez bombardowanie docelową uran-238 z miedzi -65 jonów w Gesellschaft für Schwerionenforschung w Darmstadt , Niemcy:
-
238
92U
+ 65
29Cu
→ 303
121Ubu
* → brak atomów
Nie zidentyfikowano żadnych atomów.
Unbib
Pierwsze próby syntezy unbibium podjęli w 1972 roku Flerov i in. we Wspólnym Instytucie Badań Jądrowych (ZIBJ), wykorzystując reakcje termojądrowe indukowane ciężkimi jonami:
-
238
92U
+ 66,68
30Zn
→ 304, 306
122Ubb
* → brak atomów
Eksperymenty te były motywowane wczesnymi przewidywaniami istnienia wyspy stabilności przy N = 184 i Z > 120. Nie wykryto żadnych atomów i zmierzono granicę plastyczności 5 nb (5000 pb ). Aktualne wyniki (patrz flerow ) wykazały, że czułość tych eksperymentów była zbyt niska o co najmniej 3 rzędy wielkości.
W 2000 roku Gesellschaft für Schwerionenforschung (GSI) Helmholtz Center for Heavy Ion Research przeprowadziło bardzo podobny eksperyment ze znacznie wyższą czułością:
-
238
92U
+ 70
30Zn
→ 308
122Ubb
* → brak atomów
Wyniki te wskazują, że synteza tak cięższych pierwiastków pozostaje poważnym wyzwaniem i wymagana jest dalsza poprawa natężenia wiązki i wydajności eksperymentalnej. W przyszłości czułość powinna zostać zwiększona do 1 fb, aby uzyskać lepsze wyniki.
Kolejna nieudana próba syntezy unbibu została przeprowadzona w 1978 roku w GSI Helmholtz Center, gdzie naturalny cel erbowy został zbombardowany jonami ksenonu-136 :
-
nago
68Er
+ 136
54Xe
→ 298, 300, 302, 303, 304, 306
Ubb
* → brak atomów
W szczególności oczekiwano, że reakcja między 170 Er a 136 Xe da emitery alfa o czasie półtrwania wynoszącym mikrosekundy, które rozpadną się na izotopy flerowu, których okres półtrwania może wydłużyć się do kilku godzin, ponieważ przewiduje się, że flerow znajduje się w pobliżu centrum wyspy stabilności . Po dwunastu godzinach naświetlania nic nie znaleziono w tej reakcji. Po podobnej nieudanej próbie syntezy unbinu z 238 U i 65 Cu stwierdzono, że okresy półtrwania superciężkich jąder muszą być mniejsze niż jedna mikrosekunda lub przekroje poprzeczne są bardzo małe. Nowsze badania nad syntezą superciężkich pierwiastków sugerują, że oba wnioski są prawdziwe. Dwie próby syntezy unbibium w latach 70. były napędzane przez badania sprawdzające, czy superciężkie pierwiastki mogą potencjalnie występować w naturze.
W latach 2000-2004 w Laboratorium Reakcji Jądrowych we Flerowie przeprowadzono kilka eksperymentów badających charakterystykę rozszczepienia różnych superciężkich jąder złożonych, takich jak 306 Ubb . Zastosowano dwie reakcje jądrowe, a mianowicie 248 Cm + 58 Fe i 242 Pu + 64 Ni. Wyniki pokazują, w jaki sposób superciężkie jądra rozszczepiają się głównie poprzez wyrzucanie jąder o zamkniętej powłoce, takich jak 132 Sn (Z=50, N=82). Stwierdzono również, że wydajność szlaku rozszczepienia jądrowego była podobna dla pocisków 48 Ca i 58 Fe, co sugeruje możliwe przyszłe użycie pocisków 58 Fe w formowaniu superciężkich pierwiastków.
Unbikwadium
Naukowcy z GANIL (Grand Accélérateur National d'Ions Lourds) próbowali zmierzyć bezpośrednie i opóźnione rozszczepienie jąder złożonych pierwiastków o Z = 114, 120 i 124, aby zbadać efekty powłoki w tym regionie i wskazać kolejny sferyczny proton powłoka. To dlatego, że mając kompletne pociski jądrowe (lub, równoważnie, mający liczbę magiczną z protonów i neutronów ) dawałoby większą stabilność na jądrach superciężkich takich elementów, a tym samym zbliżając się do wyspy stabilności . W 2006 roku, z pełnymi wynikami opublikowanymi w 2008 roku, zespół przedstawił wyniki reakcji polegającej na bombardowaniu naturalnej tarczy germanowej jonami uranu:
-
238
92U
+ na
32Ge
→ 308, 310, 311, 312, 314
Ubq
* → rozszczepienie
Zespół poinformował, że był w stanie zidentyfikować rozszczepienie jąder złożonych z okresami półtrwania > 10-18 s. Wynik ten sugeruje silny efekt stabilizujący przy Z = 124 i wskazuje na następną powłokę protonową przy Z > 120, a nie przy Z = 114, jak wcześniej sądzono. Jądro złożone to luźna kombinacja nukleonów, które jeszcze nie ułożyły się w otoczki jądrowe. Nie ma struktury wewnętrznej i jest utrzymywany razem tylko przez siły zderzenia między jądrem tarczy i pocisku. Szacuje się, że nukleony potrzebują około 10-14 s, aby ułożyć się w otoczki jądrowe, w którym to momencie złożone jądro staje się nuklidem , a liczba ta jest używana przez IUPAC jako minimalny okres półtrwania , jaki musi mieć deklarowany izotop potencjalnie zostać rozpoznane jako odkryte. Zatem eksperymenty GANIL nie liczą się jako odkrycie pierwiastka 124 .
Rozszczepienie jądra złożonego 312 124 badano również w 2006 r. w tandemowym akceleratorze ciężkich jonów ALPI w Laboratori Nazionali di Legnaro (Legnaro National Laboratories) we Włoszech:
-
232
90NS
+ 80
34Se
→ 312
Ubq
* → rozszczepienie
Podobnie jak w poprzednich eksperymentach przeprowadzonych w JINR ( Joint Institute for Nuclear Research ), fragmenty rozszczepienia skupione wokół podwójnie magicznych jąder, takich jak 132 Sn ( Z = 50, N = 82), ujawniają tendencję superciężkich jąder do wyrzucania takich podwójnie magicznych jąder w rozszczepienie. Stwierdzono również wzrost średniej liczby neutronów na rozszczepienie z jądra złożonego 312 124 (w stosunku do lżejszych układów), co potwierdza, że trend cięższych jąder emitujących więcej neutronów podczas rozszczepiania trwa nadal w obszarze superciężkiej masy.
Unbipentium
Pierwsza i jedyna próba syntezy unbipentium została przeprowadzona w Dubnej w latach 1970-1971 przy użyciu jonów cynku i celu ameryk - 243 :
-
243
95Jestem
+ 66, 68
30Zn
→ 309, 311
Ubp
* → brak atomów
Nie wykryto atomów i określono granicę przekroju na 5 nb. Eksperyment ten był motywowany możliwością większej stabilności jąder wokół Z ~ 126 i N ~ 184, chociaż nowsze badania sugerują, że wyspa stabilności może zamiast tego leżeć przy niższej liczbie atomowej (takiej jak copernicium , Z = 112), a synteza cięższych pierwiastków, takich jak unbipentium, będzie wymagała bardziej czułych eksperymentów.
Unbihexium
Pierwsza i jedyna próba syntezy unbihexium , która zakończyła się niepowodzeniem, została przeprowadzona w 1971 roku w CERN (Europejskiej Organizacji Badań Jądrowych) przez René Bimbota i Johna M. Alexandera przy użyciu reakcji gorącej fuzji:
-
232
90NS
+ 84
36Kr
→ 316
126Ubh
* → brak atomów
Zaobserwowano cząstki alfa o wysokiej energii (13-15 MeV ) i uznano je za możliwy dowód na syntezę unbiheksu. Kolejne nieudane eksperymenty z wyższą czułością sugerują, że czułość 10 mb tego eksperymentu była zbyt niska; stąd tworzenie się jąder unbihexium w tej reakcji jest wysoce nieprawdopodobne.
Unbiseptium
Pierwsza i jedyna próba syntezy unbiseptium, która zakończyła się niepowodzeniem, została przeprowadzona w 1978 roku w akceleratorze UNILAC w GSI Helmholtz Center, gdzie naturalny cel tantalowy został zbombardowany jonami ksenonu -136:
-
nat
73Ta
+ 136
54Xe
→ 316, 317
Ubs
* → brak atomów
Poszukiwania w przyrodzie
Badanie przeprowadzone w 1976 roku przez grupę amerykańskich naukowców z kilku uniwersytetach zaproponował, aby pierwotne elementy nadciężkiego, głównie liwermor , unbiquadium, unbihexium i unbiseptium, może być przyczyną niewyjaśnionego uszkodzenia promieniowania (zwłaszcza radiohalos ) w minerały. Skłoniło to wielu badaczy do poszukiwania ich w przyrodzie w latach 1976-1983. Grupa kierowana przez Toma Cahilla, profesora z Uniwersytetu Kalifornijskiego w Davis , twierdziła w 1976 roku, że wykryli cząstki alfa i promieniowanie rentgenowskie o odpowiednich energiach spowodować zaobserwowane uszkodzenia, wspierając obecność tych elementów. W szczególności, obecność długowieczne (rzędu 10 9 lat) unbiquadium i unbihexium jądra, wraz z ich produktów rozpadu, w obfitości 10 -11 w stosunku do ich ewentualnego kongenerów uranu i plutonu , został przypuszczał. Inni twierdzili, że żadnego nie wykryto, i kwestionowali proponowane cechy pierwotnych superciężkich jąder. W szczególności zacytowali, że każde takie superciężkie jądra muszą mieć zamkniętą powłokę neutronową przy N = 184 lub N = 228, a ten warunek konieczny dla zwiększonej stabilności istnieje tylko w izotopach z niedoborem neutronów z livermorium lub izotopy bogate w neutrony innych pierwiastków, które nie być beta-stabilne w przeciwieństwie do większości naturalnie występujących izotopów. Sugerowano również, że aktywność ta jest spowodowana transmutacjami jądrowymi w naturalnym ceru , co podnosi dalszą niejasność w tej rzekomej obserwacji superciężkich pierwiastków.
24 kwietnia 2008 r. grupa kierowana przez Amnona Marinova z Uniwersytetu Hebrajskiego w Jerozolimie twierdziła, że znalazła pojedyncze atomy unbibu -292 w naturalnie występujących złożach toru w ilości od 10-11 do 10-12 w stosunku do toru. Twierdzenie Marinova i in. został skrytykowany przez część środowiska naukowego. Marinov twierdził, że przesłał artykuł do czasopism „ Nature” i „ Nature Physics”, ale obaj go odrzucili, nie wysyłając go do recenzji. Twierdzono, że atomy unbibu -292 są superdeformowanymi lub hiperdeformowanymi izomerami o okresie półtrwania wynoszącym co najmniej 100 milionów lat.
Krytyka tej techniki, wcześniej używanej do rzekomego identyfikowania lżejszych izotopów toru za pomocą spektrometrii mas , została opublikowana w Physical Review C w 2008 roku. Obalenie grupy Marinov zostało opublikowane w Physical Review C po opublikowanym komentarzu.
Powtórzenie eksperymentu z torem przy użyciu lepszej metody akceleratorowej spektrometrii masowej (AMS) nie potwierdziło wyników, pomimo 100-krotnie lepszej czułości. Wynik ten poddaje w wątpliwość wyniki współpracy Marinovów w odniesieniu do ich twierdzeń o długożyciowych izotopach toru , rentgenu i unbibu . Nadal jest możliwe, że ślady unbibu mogą istnieć tylko w niektórych próbkach toru, chociaż jest to mało prawdopodobne.
Możliwy zasięg pierwotnych superciężkich pierwiastków na dzisiejszej Ziemi jest niepewny. Nawet jeśli zostanie potwierdzone, że dawno temu spowodowały uszkodzenia spowodowane promieniowaniem, mogą teraz rozpaść się na zwykłe ślady lub nawet całkowicie zniknąć. Nie jest również pewne, czy takie superciężkie jądra mogą być w ogóle wytwarzane naturalnie, ponieważ oczekuje się , że spontaniczne rozszczepienie zakończy proces r odpowiedzialny za tworzenie ciężkich pierwiastków o liczbie masowej od 270 do 290, na długo przed powstaniem pierwiastków cięższych niż unbinilium .
Niedawny hipoteza próbuje wyjaśnić spektrum Przybylskiego Gwiazdy przez naturalnie występujące flerow , unbinilium i unbihexium .
Przewidywane właściwości pierwiastków z ósmego okresu
Pierwiastek 118, oganesson , jest najcięższym zsyntetyzowanym pierwiastkiem. Następne dwa pierwiastki, pierwiastki 119 i 120 , powinny tworzyć szereg 8s i być odpowiednio metalem alkalicznym i metalem ziem alkalicznych . Poza pierwiastkiem 120 oczekuje się , że seria superaktynowców rozpocznie się, gdy elektrony 8s i wypełnienie podpowłok 8p 1/2 , 7d 3/2 , 6f i 5g określą chemię tych pierwiastków. Kompletne i dokładne obliczenia CCSD nie są dostępne dla pierwiastków powyżej 122 ze względu na ekstremalną złożoność sytuacji: orbitale 5g, 6f i 7d powinny mieć mniej więcej ten sam poziom energii, a w obszarze elementu 160 9s, 8p 3 Orbitale /2 i 9p 1/2 również powinny mieć mniej więcej taką samą energię. Spowoduje to mieszanie się powłok elektronowych, przez co koncepcja bloku nie będzie już zbyt dobrze stosowana, a także zaowocuje nowymi właściwościami chemicznymi, które bardzo utrudnią umieszczenie niektórych z tych pierwiastków w układzie okresowym.

Właściwości chemiczne i fizyczne
Elementy 119 i 120
Niektóre przewidywane właściwości pierwiastków 119 i 120 Nieruchomość 119 120 Standardowa masa atomowa [322] [325] Grupa 1 2 Konfiguracja elektronów walencyjnych 8s 1 8s 2 Stabilne stany utlenienia 1 , 3 2 , 4 Pierwsza energia jonizacji 463,1 kJ/mol 563,3 kJ/mol Promień metaliczny 260 po południu 200 po południu Gęstość 3 g / cm 3 7 g / cm 3 Temperatura topnienia 0–30 °C (32–86 °F) 680 ° C (1300 ° F) Temperatura wrzenia 630 °C (1200 °F) 1700 °C (3100 °F)
Pierwsze dwa pierwiastki okresu 8 będą ununennium i unbinilium, pierwiastkami 119 i 120. Ich konfiguracje elektronowe powinny mieć wypełniony orbital 8s. Ten orbital jest relatywistycznie ustabilizowany i skurczony; zatem pierwiastki 119 i 120 powinny być bardziej podobne do rubidu i strontu niż do ich bezpośrednich sąsiadów powyżej, fransu i radu . Innym efektem relatywistycznego skrócenia orbitalu 8s jest to, że promienie atomowe tych dwóch pierwiastków powinny być mniej więcej takie same jak promienie fransu i radu. Powinny one zachowywać się jak zwykłe alkalicznych i metali ziem alkalicznych (chociaż mniej reaktywne niż ich bezpośrednim pionowym sąsiadów), zwykle tworząc +1 do +2 utleniania stanów odpowiednio, ale relatywistycznemu destabilizacji 7p 3/2 podpowłoki i stosunkowo niskie energie jonizacji z elektrony 7p 3/2 powinny również umożliwiać wyższe stany utlenienia, takie jak +3 i +4 (odpowiednio).
Superaktynowce
Można uważać, że superaktynowce są w zakresie od pierwiastków 121 do 157, które można sklasyfikować jako pierwiastki 5g i 6f ósmego okresu, razem z pierwszym pierwiastkiem 7d. W serii superaktynowców wszystkie muszle 7d 3/2 , 8p 1/2 , 6f 5/2 i 5g 7/2 powinny wypełniać się jednocześnie. Stwarza to bardzo skomplikowane sytuacje, do tego stopnia, że pełne i dokładne obliczenia CCSD zostały wykonane tylko dla pierwiastków 121 i 122. Pierwszy superaktynid, unbiun (pierwiastek 121), powinien być podobny do lantanu i aktynu : jego główny stopień utlenienia powinien wynosić + 3, chociaż bliskość poziomów energetycznych podpowłok walencyjnych może pozwolić na wyższe stany utlenienia, podobnie jak w pierwiastkach 119 i 120. Relatywistyczna stabilizacja podpowłoki 8p powinna skutkować konfiguracją elektronów walencyjnych stanu podstawowego 8s 2 8p 1 dla pierwiastka 121, w przeciwieństwie do konfiguracji ds 2 lantanu i aktynu; niemniej jednak ta anomalna konfiguracja nie wydaje się wpływać na jej obliczoną chemię, która pozostaje podobna do aktynu. Przewiduje się, że jego pierwsza energia jonizacji wyniesie 429,4 kJ/mol, czyli będzie niższa niż w przypadku wszystkich znanych pierwiastków z wyjątkiem metali alkalicznych potasu , rubidu , cezu i fransu : ta wartość jest nawet niższa niż w przypadku metali alkalicznych z okresu 8 unennium (463,1 kJ/mol). Podobnie następny superaktynid, unbib (pierwiastek 122), może być podobny do ceru i toru , z głównym stopniem utlenienia +4, ale będzie miał konfigurację walencyjną w stanie podstawowym 7d 1 8s 2 8p 1 lub 8s 2 8p 2 , w przeciwieństwie do konfiguracji toru 6d 2 7s 2 . Stąd jego pierwsza energia jonizacji byłaby mniejsza niż energia toru (Th: 6,3 eV ; Ubb: 5,6 eV) ze względu na większą łatwość jonizacji elektronu 8p 1/2 unbibu niż elektronu 6d toru. Zapadnięcie się samego orbitala 5g jest opóźnione do około elementu 125; oczekuje się, że konfiguracje elektronowe 119-elektronowego szeregu izoelektronowego wynoszą [Og]8s 1 dla pierwiastków od 119 do 122, [Og]6f 1 dla pierwiastków 123 i 124 oraz [Og]5g 1 dla pierwiastka 125 wzwyż.
Przewiduje się, że w pierwszych kilku superaktynidach energie wiązania dodanych elektronów są na tyle małe, że mogą stracić wszystkie swoje elektrony walencyjne; na przykład, unbihexium (pierwiastek 126) może łatwo tworzyć stan utlenienia +8, a nawet wyższe stany utlenienia dla kilku następnych pierwiastków mogą być możliwe. Unbihexium przewiduje się również wykazują wiele innych stanów utlenienia : ostatnie obliczenia sugerują stabilny Fluorkowo UbhF może być możliwe, wynikające z wzajemnego oddziaływania wiążącego pomiędzy 5g orbitalnej na unbihexium i 2 p oczodołowej fluoru . Inne przewidywane stany utlenienia to +2, +4 i +6; Oczekuje się, że +4 będzie najczęstszym stanem utlenienia unbiheksu. W superactinides z unbipentium elementu (125) do unbiennium (elementu 129) przewiduje się wykazywać utlenienia +6 i utworzenia heksafluorki jednak UbpF 6 i UbhF 6 przewiduje się stosunkowo słabo wiążące. Do energii dysocjacji wiązania oczekuje się, że znacznie zwiększa się elementu 127, a tym bardziej na elemencie 129. Sugeruje to przejście z silnym charakterze jonowym w fluorki elementu 125 charakter bardziej kowalencyjne, obejmujące 8P orbitalnej w fluorki elementu 129. wiązanie w tych heksafluorkach superaktynowców znajduje się głównie między najwyższą podpowłoką 8p superaktynowca a podpowłoką 2p fluoru, w przeciwieństwie do tego, jak uran wykorzystuje swoje orbitale 5f i 6d do wiązania w sześciofluorku uranu .
Pomimo zdolności wczesnych superaktynowców do osiągania wysokich stanów utlenienia, obliczono, że elektrony o masie 5 g będą najtrudniejsze do jonizacji; oczekuje się, że jony Ubp 6+ i Ubh 7+ będą miały konfigurację 5g 1 , podobną do konfiguracji 5f 1 jonu Np 6+ . Podobne zachowanie obserwuje się w niskiej aktywności chemicznej elektronów 4f w lantanowcach ; jest to konsekwencją tego, że orbitale 5g są małe i głęboko zakopane w chmurze elektronowej. Obecność elektronów na orbitalach g, które nie istnieją w konfiguracji elektronowej stanu podstawowego żadnego obecnie znanego pierwiastka, powinna umożliwić obecnie nieznanym orbitalom hybrydowym formowanie się i wpływanie na chemię superaktynidów w nowy sposób, chociaż brak elektronów g w znanych pierwiastkach utrudnia przewidywanie chemii superaktynidów.
Niektóre przewidywane związki superaktynowców (X = halogen ) 121 122 123 124 125 126 127 128 129 132 142 143 144 145 146 148 153 154 155 156 157 Pogarszać UbuX 3 UbbX 4 UbtX 5 UbqX 6 UbpF
UbpF 6
UbpO2+
2UbhF
UbhF 6
UbhO 4UbsF 6 UboF 6 UbeF
UbeF 6UqbX 4
UqbX 6UqtF 6 UqqX 6
UqqO2+
2
UqqF 8
UqqO 4UqpF 6 UqoO 6 Analogi La X 3
Ac X 3Ce X 4
Cz X 4Np O2+
2CzF 4 UF 6
UO2+
2
Pu F 8
PuO 4UO 6 Stany utleniania 3 4 5 6 1, 6, 7 1, 2, 4, 6, 8 6 6 1, 6 6 4, 6 6, 8 3, 4, 5, 6, 8 6 8 12 3 0, 2 3, 5 2 3
W późniejszych superaktynidach stany utlenienia powinny być niższe. W przypadku pierwiastka 132 dominujący najbardziej stabilny stopień utlenienia będzie wynosił tylko +6; jest to dalej redukowane do +3 i +4 przez element 144, a na końcu serii superaktynowców będzie to tylko +2 (a być może nawet 0), ponieważ powłoka 6f, która jest wypełniana w tym momencie, znajduje się głęboko w środku chmura elektronów i elektrony 8s i 8p 1/2 są zbyt mocno związane, aby były aktywne chemicznie. Powłoka 5g powinna być wypełniona w elemencie 144, a powłoka 6f w pobliżu elementu 154, a w tym obszarze superaktynidów elektrony 8p 1/2 są tak silnie związane, że nie są już aktywne chemicznie, tak że tylko kilka elektronów może uczestniczyć w reakcjach chemicznych. Obliczenia Fricke et al. przewidzieć, że w elemencie 154 powłoka 6f jest pełna i nie ma żadnych funkcji fal elektronowych d lub innych poza chemicznie nieaktywnymi powłokami 8s i 8p 1/2 . Może to spowodować, że pierwiastek 154 będzie raczej niereaktywny z właściwościami podobnymi do gazu szlachetnego . Obliczenia Pyykkö zakładają jednak, że w pierwiastku 155 powłoka 6f jest nadal podatna na jonizację chemiczną: Upp 3+ powinien mieć pełną powłokę 6f, a czwarty potencjał jonizacyjny powinien mieścić się pomiędzy potencjałami terbu i dysprozu , które są znane w + 4 stan.
Podobnie jak w przypadku skurczów lantanowców i aktynowców , w szeregu superaktynowców powinno występować skurcz nadaktynowców, w których promienie jonowe superaktynowców są mniejsze niż oczekiwano. W lantanowcach skurcz wynosi około 4,4 pm na element; w aktynowcach jest to około 15:00 na pierwiastek. Skurcz jest większy w lantanowcach niż w aktynowcach ze względu na większą lokalizację funkcji falowej 4f w porównaniu z funkcją falową 5f. Porównania z funkcjami falowymi zewnętrznych elektronów lantanowców, aktynowców i nadaktynowców prowadzą do przewidywania skurczu około 2 µm na pierwiastek w nadaktynowcach; chociaż jest to mniejsze niż skurcze w lantanowcach i aktynowcach, jego łączny efekt jest większy ze względu na fakt, że głęboko zakopane powłoki 5g i 6f wypełnione są 32 elektronami, zamiast tylko 14 elektronami wypełnionymi w powłokach 4f i 5f w odpowiednio lantanowce i aktynowce.
Pekka Pyykkö dzieli te superaktynowce na trzy serie: serię 5g (elementy 121 do 138), serię 8p 1/2 (elementy 139 do 140) i serię 6f (elementy 141 do 155), zauważając również, że będzie duże nakładanie się poziomów energii i że orbitale 6f, 7d lub 8p 1/2 mogą być również zajęte we wczesnych atomach lub jonach superaktynowców. Spodziewa się również, że zachowywałyby się bardziej jak „super lantanowce ”, w tym sensie, że elektrony 5g byłyby w większości chemicznie nieaktywne, podobnie jak tylko jeden lub dwa elektrony 4f w każdym lantanowcach są kiedykolwiek zjonizowane w związkach chemicznych. Przewidywał również, że możliwe stany utlenienia superaktynowców mogą wzrosnąć bardzo wysoko w serii 6f, do wartości takich jak +12 w elemencie 148.
Andrey Kulsha nazwał trzydzieści sześć pierwiastków od 121 do 156 „przejściowymi” i zaproponował podzielenie ich na dwie serie po osiemnaście każdy, jeden z pierwiastków 121 do 138, a drugi z pierwiastków 139 do 156. Pierwszy byłby analogiczny do lantanowce, o stopniu utlenienia głównie od +4 do +6, ponieważ dominuje wypełnienie powłoki 5g, a sąsiednie pierwiastki są do siebie bardzo podobne, tworząc analogię do uranu , neptunu i plutonu . Druga byłaby analogiczna do aktynowców: na początku (wokół pierwiastków w latach 140.) należałoby oczekiwać bardzo wysokich stopni utlenienia, gdy powłoka 6f wznosi się ponad 7d, ale potem typowe stany utlenienia obniżą się i w pierwiastkach w 150 s później 8p 1/2 elektronów przestanie być chemicznie aktywne. Ponieważ dwa rzędy są oddzielone przez dodanie kompletnej podpowłoki 5g 18 , można je również uznać za analogi.
Jako przykład z późnych superaktynidów oczekuje się, że pierwiastek 156 będzie wykazywał głównie stopień utlenienia +2, ze względu na jego konfigurację elektronową z łatwo usuwanymi elektronami 7d 2 nad stabilnym [Og]5g 18 6f 14 8s 2 8p2
1/2rdzeń. Można zatem uznać cięższe kongener Nobelium , który również ma parę łatwo usunąć 7S 2 elektronów na stabilny [n] 5f 14 rdzenia i jest zwykle w stanie +2 (silne utleniacze są wymagane do uzyskania w Nobelium +3 stan). Jego energia pierwszej jonizacji powinna wynosić około 400 kJ/mol, a promień metaliczny około 170 pikometrów. Przy względnej masie atomowej około 445 u, powinien to być bardzo ciężki metal o gęstości około 26 g/cm 3 .
Elementy 157 do 166
Oczekuje się, że metale przejściowe 7d w okresie 8 będą pierwiastkami od 157 do 166. Chociaż elektrony 8s i 8p 1/2 są tak silnie związane z tymi pierwiastkami, że nie powinny być w stanie brać udziału w żadnych reakcjach chemicznych, 9s i 9p Oczekuje się, że 1/2 poziomów będzie łatwo dostępnych do hybrydyzacji. Te pierwiastki 7d powinny być podobne do pierwiastków 4d itru poprzez kadm . W szczególności element 164 o konfiguracji elektronowej 7d 10 9s 0 wykazuje wyraźne analogie z palladem z jego konfiguracją elektronową 4d 10 5s 0 .
Nie oczekuje się metale szlachetne z tej serii metali przejściowych się szlachetne jak ich homologów lżejszych, ze względu na nieobecność zewnętrznej s powłoki dla osłony, a także dlatego, że 7d powłoki silnie podzielona na dwie podpowłok powodu efektów relatywistycznymi. Powoduje to, że energie pierwszej jonizacji metali przejściowych 7d są mniejsze niż ich lżejsze kongenery.
Teoretyczne zainteresowanie chemią unheksquadium jest w dużej mierze motywowane przewidywaniami teoretycznymi, że on, zwłaszcza izotopy 472 Uhq i 482 Uhq (ze 164 protonami i 308 lub 318 neutronami ), znalazłyby się w centrum hipotetycznej drugiej wyspy stabilności (pierwszej koncentrując się na copernicium , szczególnie izotopach 291 Cn, 293 Cn i 296 Cn, które mają mieć okres półtrwania stuleci lub tysiącleci).
Obliczenia przewidują, że elektrony 7d pierwiastka 164 (nieheksquadowe) powinny bardzo łatwo uczestniczyć w reakcjach chemicznych, tak że unheksquadium powinno być w stanie wykazywać stabilne stany utlenienia +6 i +4 oprócz normalnego stanu +2 w roztworach wodnych z silnymi ligandami . Unhexquadium powinno zatem być w stanie, z wytworzeniem związków, takich jak UHQ ( CO ) 4 , UHQ ( PF 3 ) 4 (zarówno tetraedrycznej , jak odpowiednie związki palladu) i UHQ ( CN )2
2( liniowy ), co bardzo różni się od zachowania ołowiu , którego unhexquadium byłby cięższym homologiem, gdyby nie efekty relatywistyczne. Niemniej jednak stan dwuwartościowy byłby głównym stanem w roztworze wodnym (choć stany +4 i +6 byłyby możliwe przy silniejszych ligandach), a unhekskwad(II) powinien zachowywać się bardziej podobnie do ołowiu niż unheksquadium(IV) i unheksquadium(VI ).
Oczekuje się, że Unhexquadium będzie miękkim kwasem Lewisa i ma parametr miękkości Ahrlandsa bliski 4 eV . Unhexquadium powinien być co najwyżej umiarkowanie reaktywny, mając pierwszą energię jonizacji, która powinna wynosić około 685 kJ/mol, porównywalna do energii molibdenu . Ze względu na skurcze lantanowców, aktynowców i superaktynowców , unhexquadium powinien mieć promień metaliczny tylko 158 pm , bardzo zbliżony do znacznie lżejszego magnezu , pomimo oczekiwanej masy atomowej około 474 u, która jest około 19,5 razy większa od masy atomowej magnez. Ten mały promień i duża masa powodują, że oczekuje się, że będzie miał niezwykle wysoką gęstość około 46 g·cm- 3 , ponad dwukrotnie większą niż osm , obecnie najgęstszy znany pierwiastek, przy 22,61 g·cm- 3 ; unheksquadium powinien być drugim najgęstszym pierwiastkiem w pierwszych 172 pierwiastkach w układzie okresowym, a tylko jego sąsiad unhekstrium (pierwiastek 163) ma większą gęstość (47 g·cm -3 ). Metaliczny unheksquadium powinien mieć bardzo dużą energię kohezji ( entalpię krystalizacji) ze względu na swoje wiązania kowalencyjne , co najprawdopodobniej skutkuje wysoką temperaturą topnienia. W stanie metalicznym unheksquadium powinien być dość szlachetny i analogiczny do palladu i platyny . Fricke i in. zasugerowali pewne formalne podobieństwa do oganessonu , ponieważ oba pierwiastki mają konfiguracje zamkniętej powłoki i podobne energie jonizacji, chociaż zauważają, że chociaż oganesson byłby bardzo złym gazem szlachetnym, unhexquadium byłby dobrym metalem szlachetnym.
Pierwiastki 165 (unhekspentium) i 166 (unhekspentium), ostatnie dwa metale 7d, powinny zachowywać się podobnie do metali alkalicznych i metali ziem alkalicznych, gdy znajdują się odpowiednio na stopniach utlenienia +1 i +2. Elektrony dziewiątki powinny mieć energie jonizacji porównywalne do energii trójek elektronów sodu i magnezu , ze względu na efekty relatywistyczne powodujące, że elektrony dziewiątki są znacznie silniej związane niż przewidywałyby obliczenia nierelatywistyczne. Pierwiastki 165 i 166 powinny normalnie wykazywać odpowiednio stany utlenienia +1 i +2, chociaż energie jonizacji elektronów 7d są wystarczająco niskie, aby umożliwić wyższe stany utlenienia, takie jak +3 dla pierwiastka 165. Stopień utlenienia +4 dla pierwiastka 166 jest mniejszy prawdopodobnie tworząc sytuację podobną do lżejszych pierwiastków w grupach 11 i 12 (zwłaszcza złota i rtęci ). Ponieważ rtęć, ale nie copernicium jonizacja elementu 166, który UHH 2+ powinna doprowadzić w 7d 10 konfiguracji odpowiadającej utraty elektronów s, ale nie D-elektronów, co bardziej przypomina zapalniczki „mniej Relatywistyczna pierwiastki grupy 12 cynk, kadm i rtęć, które zasadniczo nie mają charakteru metali przejściowych.
Niektóre przewidywane właściwości pierwiastków 156-166
Promienie metaliczne i gęstości są pierwszymi przybliżeniami.
Najbardziej analogiczna grupa jest podana jako pierwsza, a następnie inne podobne grupy.Nieruchomość 156 157 158 159 160 161 162 163 164 165 166 Standardowa masa atomowa [445] [448] [452] [456] [459] [463] [466] [470] [474] [477] [481] Grupa Grupa Yb
(4)3
(5)4
(6)5
(7)6
(8)7
(9)8
(10)9
(11)10
(12, 14, 18)11
(1, 13)12
(2, 14)Konfiguracja elektronów walencyjnych 7d 2 7d 3 7d 4 7d 5 7d 6 7d 7 7d 8 7d 9 7d 10 7d 10 9s 1 7d 10 9s 2 Stabilne stany utlenienia 2 3 4 1 , 5 2 , 6 3 , 7 4 , 8 5 0 , 2 , 4 , 6 1 , 3 2 Pierwsza energia jonizacji 400 kJ/mol 450 kJ/mol 520 kJ/mol 340 kJ/mol 420 kJ/mol 470 kJ/mol 560 kJ/mol 620 kJ/mol 690 kJ/mol 520 kJ/mol 630 kJ/mol Promień metaliczny 170 po południu 163 po południu 157 po południu 152 po południu 148 po południu 148 po południu 149 po południu 152 po południu 158 po południu 250 po południu 200 po południu Gęstość 26 g / cm 3 28 g / cm 3 30 g / cm 3 33 g / cm 3 36 g / cm 3 40 g / cm 3 45 g / cm 3 47 g / cm 3 46 g / cm 3 7 g / cm 3 11 g / cm 3
Elementy 167 do 172
Oczekuje się, że następnych sześć pierwiastków w układzie okresowym będzie ostatnimi pierwiastkami z grupy głównej w swoim okresie i prawdopodobnie będzie podobnych do pierwiastków 5p od indu do ksenonu . W elementach od 167 do 172 będą wypełnione pociski 9p 1/2 i 8p 3/2 . Ich wartości własne energii są tak blisko siebie, że zachowują się jak jedna połączona podpowłoka p, podobnie jak nierelatywistyczne podpowłoki 2p i 3p. Zatem efekt pary obojętnych nie występuje i oczekuje się, że najczęstsze stopnie utlenienia pierwiastków 167 do 170 to odpowiednio +3, +4, +5 i +6. Oczekuje się, że pierwiastek 171 (unseptun) wykaże pewne podobieństwa do halogenów , wykazując różne stopnie utlenienia w zakresie od -1 do +7, chociaż oczekuje się, że jego właściwości fizyczne będą bliższe właściwościom metalu. Oczekuje się, że jego powinowactwo do elektronów wyniesie 3,0 eV , co pozwoli mu utworzyć HUsu, analogicznie do halogenowodoru . Oczekuje się, że jon Usu − będzie miękką zasadą , porównywalną do jodku (I − ). Oczekuje się, że pierwiastek 172 (unseptb) będzie gazem szlachetnym o zachowaniu chemicznym podobnym do ksenonu, ponieważ ich energie jonizacji powinny być bardzo podobne (Xe, 1170,4 kJ/mol; Usb, 1090 kJ/mol). Jedyną główną różnicą między nimi jest to, że pierwiastek 172, w przeciwieństwie do ksenonu, ma być cieczą lub ciałem stałym w standardowej temperaturze i ciśnieniu ze względu na znacznie większą masę atomową. Oczekuje się, że unseptbium będzie silnym kwasem Lewisa , tworzącym fluorki i tlenki, podobnie jak jego lżejszy kongener ksenon. Ze względu na analogię elementów 165–172 do okresów 2 i 3, Fricke i in. uważali, że tworzą dziewiąty okres układu okresowego, podczas gdy ósmy okres uznali za zakończony pierwiastkiem metalu szlachetnego 164. Ten dziewiąty okres byłby podobny do drugiego i trzeciego okresu, ponieważ oczekuje się, że nie będzie miał przejścia metale.
Niektóre przewidywane właściwości pierwiastków 167-172
Promienie metaliczne lub kowalencyjne i gęstości są pierwszymi przybliżeniami.Nieruchomość 167 168 169 170 171 172 Standardowa masa atomowa [485] [489] [493] [496] [500] [504] Grupa 13 14 15 16 17 18 Konfiguracja elektronów walencyjnych 9s 2 9p 1 9s 2 9p 2 9s 2 9p 2 8p 1 9s 2 9p 2 8p 2 9s 2 9p 2 8p 3 9s 2 9p 2 8p 4 Stabilne stany utlenienia 3 4 5 6 -1 , 3 , 7 0 , 4 , 6 , 8 Pierwsza energia jonizacji 620 kJ/mol 720 kJ/mol 800 kJ/mol 890 kJ/mol 984 kJ/mol 1090 kJ/mol Promień metaliczny lub kowalencyjny 190 po południu 180 po południu 175 po południu 170 po południu 165 po południu 220 po południu Gęstość 17 g / cm 3 19 g / cm 3 18 g / cm 3 17 g / cm 3 16 g / cm 3 9 g / cm 3
Poza elementem 172
Oczekuje się, że pierwiastek 172, ostatni pierwiastek z okresu 8, będzie pierwszym gazem szlachetnym po oganessonie (ostatni pierwiastek z okresu 7). Poza tym powinna rozpocząć się kolejna długa seria przejściowa, taka jak superaktynowce, wypełniająca co najmniej muszle 6g, 7f i 8d (z 10s, 10p 1/2 i 6h 11/2 zbyt dużą energią, aby wnieść wkład na początku serii). Elektrony te byłyby bardzo luźno związane, potencjalnie umożliwiając osiągnięcie bardzo wysokich stanów utlenienia, chociaż elektrony stałyby się ściślej związane ze wzrostem ładunku jonowego.
W elemencie 173 (unseptrium) najbardziej zewnętrzny elektron wszedłby do podpowłoki 6g 7/2 . Ponieważ interakcje spin-orbita mogłyby stworzyć bardzo dużą przerwę energetyczną między podpowłokami 8p 3/2 i 6g 7/2 , oczekuje się, że ten najbardziej zewnętrzny elektron będzie bardzo luźno związany i bardzo łatwo stracony, tworząc kation Ust + . W rezultacie oczekuje się, że pierwiastek 173 będzie zachowywał się chemicznie jak metal alkaliczny, a jeden znacznie bardziej reaktywny niż nawet cez (franc i pierwiastek 119 są mniej reaktywne niż cez ze względu na efekty relatywistyczne).
Pierwiastek 184 (unoctquadium) był istotnie celem wczesnych przewidywań, ponieważ początkowo spekulowano, że 184 będzie magiczną liczbą protonową: przewiduje się, że ma konfigurację elektronową [Usb] 6g 5 7f 4 8d 3 , z co najmniej 7f i 8d elektrony aktywne chemicznie. Oczekuje się, że jego zachowanie chemiczne będzie podobne do uranu i neptunu , ponieważ dalsza jonizacja poza stanem +6 (odpowiadającym usunięciu elektronów 6g) będzie prawdopodobnie nieopłacalna; stan +4 powinien być najbardziej powszechny w roztworze wodnym, a +5 i +6 osiągalne w związkach stałych.
Koniec układu okresowego
Liczba fizycznie możliwych elementów jest nieznana. Niskie oszacowanie jest takie, że układ okresowy może zakończyć się wkrótce po wyspie stabilności , która ma wyśrodkować na Z = 126, ponieważ rozszerzenie układu okresowego pierwiastków i nuklidów jest ograniczone przez linie kroplowania protonów i neutronów oraz stabilność w kierunku alfa. rozpad i spontaniczne rozszczepienie. Jedno obliczenie Y. Gambhira i in. , analizując energię wiązania jądra i stabilność w różnych kanałach rozpadu, sugeruje granicę istnienia jąder związanych przy Z = 146. Niektórzy, tacy jak Walter Greiner , przewidywali, że może nie być końca układu okresowego pierwiastków. Inne przewidywania końca układu okresowego to Z = 128 ( John Emsley ) i Z = 155 (Albert Khazan).
Pierwiastki powyżej liczby atomowej 137
Jest to „ludowa legenda” wśród fizyków, że Richard Feynman sugerował, że neutralne atomy nie mogą istnieć dla liczby atomowej większej niż Z = 137, na tej podstawie, że relatywistyczne równanie Diraca przewiduje, że energia stanu podstawowego najbardziej wewnętrznego elektronu w takim atom byłby liczbą urojoną . Tutaj liczba 137 powstaje jako odwrotność stałej struktury subtelnej . Zgodnie z tym argumentem, neutralne atomy nie mogą istnieć poza untriseptium, a zatem układ okresowy pierwiastków oparty na orbitalach elektronowych załamuje się w tym momencie. Argument ten zakłada jednak, że jądro atomowe jest punktowe. Dokładniejsze obliczenia muszą uwzględniać mały, ale niezerowy rozmiar jądra, co przewiduje się, że przesunie granicę dalej do Z ≈ 173.
Model Bohra
Model Bohra wykazuje trudności dla atomów o liczbie atomowej większej niż 137, ponieważ prędkość elektronu na orbicie elektronowej 1s , v , jest dana wzorem
gdzie Z jest liczbą atomową , a α jest stałą struktury subtelnej , miarą siły oddziaływań elektromagnetycznych. Zgodnie z tym przybliżeniem każdy pierwiastek o liczbie atomowej większej niż 137 wymagałby, aby elektrony 1s poruszały się z prędkością większą niż c , czyli prędkość światła . Stąd nierelatywistyczny model Bohra jest niedokładny w zastosowaniu do takiego elementu.
Relatywistyczne równanie Diraca

Relatywistyczne równanie Diraca daje energię stanu podstawowego jako
gdzie m jest masą spoczynkową elektronu. Dla Z > 137 funkcja falowa stanu podstawowego Diraca jest oscylacyjna, a nie związana, i nie ma luki między dodatnimi i ujemnymi widmami energii, jak w paradoksie Kleina . Dokładniejsze obliczenia uwzględniające wpływ skończonych rozmiarów jądra wskazują, że energia wiązania najpierw przekracza 2 mc 2 dla Z > Z cr ≈ 173. Dla Z > Z cr , jeśli najbardziej wewnętrzny orbital (1s) nie jest wypełniony, pole elektryczne jądra wyciągnie elektron z próżni , powodując spontaniczną emisję pozytonu . To zanurzenie podpowłoki 1 w ujemnym kontinuum było często uważane za „koniec” układu okresowego pierwiastków, chociaż bardziej szczegółowe zabiegi sugerują mniej ponury wynik.
Atomy o liczbie atomowej powyżej Z cr ≈ 173 nazwano atomami nadkrytycznymi . Atomy nadkrytyczne nie mogą być całkowicie zjonizowane, ponieważ ich podpowłoka 1s zostałaby wypełniona przez spontaniczne tworzenie pary, w której para elektron-pozyton jest tworzona z kontinuum ujemnego, przy czym elektron jest związany, a pozyton ucieka. Jednak silne pole wokół jądra atomowego jest ograniczone do bardzo małego obszaru przestrzeni, tak że zasada wykluczania Pauliego zabrania dalszego spontanicznego tworzenia par po wypełnieniu podpowłok, które zanurkowały w ujemne kontinuum. Pierwiastki 173-184 nazwano słabo nadkrytycznymi atomami, ponieważ dla nich tylko powłoka 1s zanurkowała w ujemne kontinuum; oczekuje się, że powłoka 2p 1/2 połączy się wokół pierwiastka 185, a powłoka 2s wokół pierwiastka 245. Dotychczasowe eksperymenty nie doprowadziły do wykrycia spontanicznego tworzenia par z asemblacji ładunków nadkrytycznych w wyniku zderzenia ciężkich jąder (np. zderzenia ołowiu z uranem do chwilowego daje efektywne Z równe 174; uran z uranem daje efektywne Z = 184, a uran z kalifornem daje efektywne Z = 190). Ponieważ oczekuje się, że atomy w stanie nadkrytycznym nie będą stwarzać trudności ze swoją strukturą elektronową, koniec układu okresowego można określić raczej niestabilnością jądrową niż niestabilnością powłoki elektronowej.
Materia kwarkowa
Przypuszcza się również, że w obszarze poza A > 300 może istnieć cały „ kontynent stabilności ” składający się z hipotetycznej fazy stabilnej materii kwarkowej , składającej się raczej z swobodnie płynących w górę i w dół kwarków niż kwarków połączonych w protony i neutrony. Teoretycznie taka forma materii jest stanem podstawowym materii barionowej z większą energią wiązania na barion niż materia jądrowa , co sprzyja rozpadowi materii jądrowej poza ten próg masy na materię kwarkową. Jeśli taki stan materii istnieje, prawdopodobnie mógłby zostać zsyntetyzowany w tych samych reakcjach syntezy, prowadzących do normalnych superciężkich jąder, i byłby ustabilizowany przed rozszczepieniem w wyniku silniejszego wiązania, które wystarcza do przezwyciężenia odpychania kulombowskiego.
Ostatnie obliczenia sugerują stabilność bryłek materii kwarkowej w górę (udQM) względem jąder konwencjonalnych poza A ~ 266, a także pokazują, że bryłki udQM stają się nadkrytyczne wcześniej ( Z cr ~ 163, A ~ 609) niż jądra konwencjonalne ( Z cr ~ 177, ~ 480).
Właściwości jądrowe
Magiczne liczby i wyspa stabilności
Stabilność jąder znacznie spada wraz ze wzrostem liczby atomowej po Curium , element 96, tak, że wszystkie izotopy o liczbie atomowej powyżej 101 rozpadu radioaktywnie z półtrwania pod dziennie, z wyjątkiem Dubnium -268. Żadne pierwiastki o liczbie atomowej powyżej 82 (po ołowiu ) nie mają stabilnych izotopów. Niemniej jednak, z przyczyn jeszcze nie do końca poznanych, istnieje nieznaczny wzrost stabilności jądrowej wokół liczb atomowych 110 – 114 , co prowadzi do pojawienia się czegoś, co w fizyce jądrowej znane jest jako „ wyspa stabilności ”. Ta koncepcja, zaproponowana przez profesora Uniwersytetu Kalifornijskiego Glenna Seaborga , wyjaśnia, dlaczego superciężkie elementy trwają dłużej niż przewidywano.
Obliczenia według metody Hartree–Fock–Bogoliubov z wykorzystaniem nierelatywistycznego oddziaływania Skyrme zaproponowały Z = 126 jako zamkniętą powłokę protonową . W tym obszarze układu okresowego zasugerowano , że N = 184, N = 196 i N = 228 jako zamknięte powłoki neutronowe. Dlatego najbardziej interesujące są izotopy 310 126, 322 126 i 354 126, ponieważ mogą one być znacznie dłużej żyjące niż inne izotopy. Element 126, mający magiczną liczbę od protonów , przewiduje się, że są bardziej stabilne niż inne elementy w tym regionie i mogą mieć izomery jądrowe o bardzo długim okresie półtrwania . Możliwe jest również, że wyspa stabilności jest wyśrodkowana na 306 122 , co może być sferyczne i podwójnie magiczne .
Biorąc pod uwagę deformację jądrową i efekty relatywistyczne, analiza poziomów pojedynczych cząstek przewiduje nowe liczby magiczne dla superciężkich jąder przy Z = 126, 138, 154 i 164 oraz N = 228, 308 i 318. wyspa stabilności ześrodkowana na 291 Cn, 293 Cn i 298 Fl, dalsze wyspy stabilności mogą istnieć wokół podwójnie magicznych 354 126 oraz 472 164 lub 482 164. Przewiduje się, że te jądra są beta-stabilne i rozpadają się przez emisję alfa lub spontaniczne rozszczepienie ze stosunkowo długimi okresami półtrwania i nadają dodatkową stabilność sąsiednim N = 228 izotonom i pierwiastkom 152–168, odpowiednio. Z drugiej strony, ta sama analiza sugeruje, że domknięcia powłoki protonowej mogą być stosunkowo słabe lub nawet nieistnieć w niektórych przypadkach, takich jak 354 126, co oznacza, że takie jądra mogą nie być podwójnie magiczne, a stabilność będzie determinowana głównie przez silne zamknięcia powłoki neutronowej. Dodatkowo, ze względu na ogromnie większe siły odpychania elektromagnetycznego, które muszą zostać pokonane przez silne siły na drugiej wyspie ( Z = 164), możliwe jest, że jądra wokół tego obszaru istnieją tylko jako rezonanse i nie mogą pozostawać razem przez znaczącą ilość czas. Możliwe jest również, że niektóre z superaktynidów między tymi seriami mogą w rzeczywistości nie istnieć, ponieważ znajdują się zbyt daleko od obu wysp, w którym to przypadku układ okresowy może zakończyć się około Z = 130.
Poza pierwiastkiem 164 linia rozszczepiania określająca granicę stabilności w odniesieniu do samorzutnego rozszczepienia może zbiegać się z linią kroplową neutronów , stanowiąc granicę dla istnienia cięższych pierwiastków. Niemniej jednak, dalsze magiczne liczby zostały przewidziane przy Z = 210, 274 i 354 oraz N = 308, 406, 524, 644 i 772, z dwoma beta-stabilnymi podwójnie magicznymi jądrami znalezionymi przy 616 210 i 798 274; ta sama metoda obliczeniowa odtworzyła przewidywania dla 298 Fl i 472 164. (Podwójnie magiczne jądra przewidziane dla Z = 354 są beta-niestabilne, przy czym 998 354 jest ubogie w neutrony, a 1126 354 bogate w neutrony). rozpad i rozszczepienie są przewidywane dla 616 210 i 798 274, z okresami połowicznego rozpadu do setek mikrosekund dla 616 210, nie będą istniały wyspy stabilności tak znaczące, jak przewidywane dla Z = 114 i 164. Ponieważ istnienie superciężkich pierwiastków jest bardzo silnie uzależniony od efektów stabilizujących z zamkniętych powłok, niestabilność jądra i rozszczepienie prawdopodobnie określą koniec układu okresowego poza tymi wyspami stabilności.
Przewidywane właściwości rozpadu nieodkrytych pierwiastków
Ponieważ uważa się, że główna wyspa stabilności leży w okolicach 291 Cn i 293 Cn, nieodkryte pierwiastki poza oganessonem mogą być bardzo niestabilne i ulegać rozpadowi alfa lub spontanicznemu rozszczepieniu w ciągu mikrosekund lub mniej. Dokładny region, w którym okresy półtrwania przekracza jedną mikrosekundę, nie jest znany, chociaż różne modele sugerują, że izotopy pierwiastków cięższych niż unbinilium, które mogą być wytwarzane w reakcjach fuzji z dostępnymi celami i pociskami, będą miały okres półtrwania poniżej jednej mikrosekundy, a zatem mogą nie być wykryto. Konsekwentnie przewiduje się, że będą istniały obszary stabilności przy N = 184 i N = 228, a być może również przy Z ~ 124 i N ~ 198. Jądra te mogą mieć okres półtrwania wynoszący kilka sekund i ulegać głównie rozpadowi alfa i samoistnemu rozszczepienia, chociaż mogą również istnieć mniejsze gałęzie rozpadu beta-plus (lub wychwytywania elektronów ). Poza tymi obszarów o zwiększonej trwałości, rozszczepienia bariery oczekuje się znacznie spaść na skutek utraty działania stabilizującego, w wyniku rozszczepienia półtrwania poniżej 10 -18 sekund, zwłaszcza w jeszcze nawet jąder na którym przeszkoda jest nawet niższa ze względu na nukleon parowania . Ogólnie rzecz biorąc, oczekuje się, że okresy połowicznego rozpadu alfa będą wzrastać wraz z liczbą neutronów, od nanosekund w najbardziej ubogich w neutrony izotopach do sekund bliżej linii stabilności beta . W przypadku jąder zawierających tylko kilka neutronów więcej niż magiczna liczba energia wiązania znacznie spada, co skutkuje załamaniem trendu i krótszym okresem półtrwania. Najbardziej ubogie w neutrony izotopy tych pierwiastków mogą również być niezwiązane i ulegać emisji protonów . Rozpad klasterowy (emisja cząstek ciężkich) został również zaproponowany jako alternatywny tryb rozpadu niektórych izotopów, co stanowi kolejną przeszkodę w identyfikacji tych pierwiastków.
Konfiguracje elektronowe
Poniżej przedstawiono oczekiwane konfiguracje elektronowe pierwiastków 119–173 i 184. Symbol [Og] wskazuje prawdopodobną konfigurację elektronową oganessonu (Z = 118), który jest obecnie ostatnim znanym pierwiastkiem. Konfiguracje elementów w tej tabeli są zapisane zaczynając od [Og], ponieważ oczekuje się, że oganesson będzie ostatnim wcześniejszym elementem z konfiguracją zamkniętej powłoki (gaz obojętny), 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 4f 14 5s 2 5p 6 5d 10 5f 14 6s 2 6p 6 6d 10 7s 2 7p 6 .
Poza elementem 123 nie są dostępne pełne obliczenia, a zatem dane w tej tabeli należy traktować jako wstępne . W przypadku pierwiastka 123, a być może także cięższych pierwiastków, przewiduje się, że kilka możliwych konfiguracji elektronów będzie mieć bardzo podobne poziomy energii, tak że bardzo trudno jest przewidzieć stan podstawowy . Uwzględniono wszystkie zaproponowane konfiguracje (odkąd zrozumiano, że reguła Madelunga prawdopodobnie przestaje tu działać).
Przewidywane przydziały bloków do 172 to Kulsha, zgodnie z oczekiwanymi dostępnymi orbitalami walencyjnymi. W literaturze nie ma jednak zgody co do tego, jak bloki powinny działać po elemencie 138.
Pierwiastek chemiczny Blok Przewidywane konfiguracje elektronów 119 Uue Ununennium s-blok [Og] 8s 1 120 Ubn Unbinilium s-blok [Og] 8s 2 121 Ubu Unbinium g-blok [Og] 8s 2 8p1
1/2122 Ubb Unbib g-blok [Og] 8s 2 8p2
1/2
[Og] 7d 1 8s 2 8p1
1/2123 Ubt Unbitrium g-blok [Og] 6f 1 8s 2 8p2
1/2
[Og] 6f 1 7d 1 8s 2 8p1
1/2
[Og] 6f 2 8s 2 8p1
1/2
[Og] 8s 2 8p2
1/2 8p1
3/2124 Ubq Unbikwadium g-blok [Og] 6f 2 8s 2 8p2
1/2
[Og] 6f 3 8s 2 8p1
1/2125 Ubp Unbipentium g-blok [Og] 6f 4 8s 2 8p1
1/2
[Og] 5g 1 6f 2 8s 2 8p2
1/2
[Og] 5g 1 6f 3 8s 2 8p1
1/2
[Og] 8s 2 0,81(5g 1 6f 2 8p2
1/2) + 0,17 (5g 1 6f 1 7d 2 8p)1
1/2) + 0,02(6f 3 7d 1 8p1
1/2)126 Ubh Unbihexium g-blok [Og] 5g 1 6f 4 8s 2 8p1
1/2
[Og] 5g 2 6f 2 8s 2 8p2
1/2
[Og] 5g 2 6f 3 8s 2 8p1
1/2
[Og] 8s 2 0,998(5g 2 6f 3 8p1
1/2) + 0,002 (5g 2 6f 2 8p)2
1/2)127 Ubs Unbiseptium g-blok [Og] 5g 2 6f 3 8s 2 8p2
1/2
[Og] 5g 3 6f 2 8s 2 8p2
1/2
[Og] 8s 2 0,88(5g 3 6f 2 8p2
1/2) + 0,12 (5g 3 6f 1 7d 2 8p)1
1/2)128 Ubo Unbioktium g-blok [Og] 5g 3 6f 3 8s 2 8p2
1/2
[Og] 5g 4 6f 2 8s 2 8p2
1/2
[Og] 8s 2 0,88(5g 4 6f 2 8p2
1/2) + 0,12 (5g 4 6f 1 7d 2 8p1
1/2)129 Ube Dwulecie g-blok [Og] 5g 4 6f 3 7d 1 8s 2 8p1
1/2
[Og] 5g 4 6f 3 8s 2 8p2
1/2
[Og] 5g 5 6f 2 8s 2 8p2
1/2
[Og] 5g 4 6f 3 7d 1 8s 2 8p1
1/2130 Nie Untrinilium g-blok [Og] 5g 5 6f 3 7d 1 8s 2 8p1
1/2
[Og] 5g 5 6f 3 8s 2 8p2
1/2
[Og] 5g 6 6f 2 8s 2 8p2
1/2
[Og] 5g 5 6f 3 7d 1 8s 2 8p1
1/2131 Utu Untriunium g-blok [Og] 5g 6 6f 3 8s 2 8p2
1/2
[Og] 5g 7 6f 2 8s 2 8p2
1/2
[Og] 8s 2 0,86(5g 6 6f 3 8p2
1/2) + 0,14 (5g 6 6f 2 7d 2 8p)1
1/2)132 UTB Untribium g-blok [Og] 5g 7 6f 3 8s 2 8p2
1/2
[Og] 5g 8 6f 2 8s 2 8p2
1/2133 Utt Untritrium g-blok [Og] 5g 8 6f 3 8s 2 8p2
1/2134 Utq Untriquadium g-blok [Og] 5g 8 6f 4 8s 2 8p2
1/2135 Utp Untrypentium g-blok [Og] 5g 9 6f 4 8s 2 8p2
1/2136 Uth Untrihexium g-blok [Og] 5g 10 6f 4 8s 2 8p2
1/2137 Uts Untriseptium g-blok [Og] 5g 11 6f 4 8s 2 8p2
1/2138 Ty też Untriokt g-blok [Og] 5g 12 6f 4 8s 2 8p2
1/2
[Og] 5g 12 6f 3 7d 1 8s 2 8p2
1/2139 Ute Untriennium g-blok [Og] 5g 13 6f 3 7d 1 8s 2 8p2
1/2
[Og] 5g 13 6f 2 7d 2 8s 2 8p2
1/2140 Uqn Unquadnilium g-blok [Og] 5g 14 6f 3 7d 1 8s 2 8p2
1/2
[Og] 5g 15 6f 1 8s 2 8p2
1/2 8p2
3/2141 Uqu niekwadun g-blok [Og] 5g 15 6f 2 7d 2 8s 2 8p2
1/2142 Uqb Niekwadb g-blok [Og] 5g 16 6f 2 7d 2 8s 2 8p2
1/2143 Uqt Niekwadrium f-blok [Og] 5g 17 6f 2 7d 2 8s 2 8p2
1/2144 Uqq Unquadquadium f-blok [Og] 5g 18 6f 2 7d 2 8s 2 8p2
1/2
[Og] 5g 18 6f 1 7d 3 8s 2 8p2
1/2
[Og] 5g 17 6f 2 7d 3 8s 2 8p2
1/2
[Og] 8s 2 0,95(5g 17 6f 2 7d 3 8p2
1/2) + 0,05 (5g 17 6f 4 7d 1 8p)2
1/2)145 Uqp Unkwadpentium f-blok [Og] 5g 18 6f 3 7d 2 8s 2 8p2
1/2146 Uqh Unquadheksyum f-blok [Og] 5g 18 6f 4 7d 2 8s 2 8p2
1/2147 Uqs Unquadseptium f-blok [Og] 5g 18 6f 5 7d 2 8s 2 8p2
1/2148 Uqo niekwadoctium f-blok [Og] 5g 18 6f 6 7d 2 8s 2 8p2
1/2149 Uqe Unquadennium f-blok [Og] 5g 18 6f 6 7d 3 8s 2 8p2
1/2150 Upn Unpentnilium f-blok [Og] 5g 18 6f 6 7d 4 8s 2 8p2
1/2
[Og] 5g 18 6f 7 7d 3 8s 2 8p2
1/2151 Upu Unpentunium f-blok [Og] 5g 18 6f 8 7d 3 8s 2 8p2
1/2152 Upb Unpentbium f-blok [Og] 5g 18 6f 9 7d 3 8s 2 8p2
1/2153 Upt Unpenttrium f-blok [Og] 5g 18 6f 10 7d 3 8s 2 8p2
1/2
[Og] 5g 18 6f 11 7d 2 8s 2 8p2
1/2154 Upq Unpentquadium f-blok [Og] 5g 18 6f 11 7d 3 8s 2 8p2
1/2
[Og] 5g 18 6f 12 7d 2 8s 2 8p2
1/2155 Upp Unpentium f-blok [Og] 5g 18 6f 12 7d 3 8s 2 8p2
1/2
[Og] 5g 18 6f 13 7d 2 8s 2 8p2
1/2156 Up Unpenthexium f-blok [Og] 5g 18 6f 13 7d 3 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 2 8s 2 8p2
1/2157 UPS Unpentseptium d-blok [Og] 5g 18 6f 14 7d 3 8s 2 8p2
1/2158 Upo Unpentoctium d-blok [Og] 5g 18 6f 14 7d 4 8s 2 8p2
1/2159 Upe Unpentennium d-blok [Og] 5g 18 6f 14 7d 5 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 4 8s 2 8p2
1/29s 1160 Uhn Unhexnilium d-blok [Og] 5g 18 6f 14 7d 6 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 5 8s 2 8p2
1/29s 1161 Uhu Unhexunium d-blok [Og] 5g 18 6f 14 7d 7 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 6 8s 2 8p2
1/29s 1162 Uhb Unhexbium d-blok [Og] 5g 18 6f 14 7d 8 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 7 8s 2 8p2
1/29s 1163 Uht Unhekstrium d-blok [Og] 5g 18 6f 14 7d 9 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 8 8s 2 8p2
1/29s 1164 Uhq Unhexquadium d-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2165 Uhp Unhekspentium d-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/29s 1166 Uhh Unheksaks d-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/29s 2167 Uhs Unheksseptium p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/29s 2 9p1
1/2
[Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p1
3/29s 2168 Uho Unheksokt p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/29s 2 9p2
1/2
[Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p2
3/29s 2169 Uhe Unheksennium p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p1
3/29s 2 9p2
1/2
[Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p3
3/29s 2170 Usn Unseptnilium p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p2
3/29s 2 9p2
1/2
[Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p4
3/29s 2171 Usu Unseptunium p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p3
3/29s 2 9p2
1/2
[Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p4
3/29s 2 9p1
1/2172 Usb Nieseptb p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p4
3/29s 2 9p2
1/2173 Ust Unsepttrium ? [Usb] 6g 1
[Usb] 9p1
3/2... ... ... ... ... 184 Uoq Unokkwadium ? [Usb] 6g 5 7f 4 8d 3
Zobacz też
Bibliografia
Dalsza lektura
- Kaldor, U. (2005). „Superciężkie pierwiastki — chemia i spektroskopia”. Encyklopedia Chemii Obliczeniowej . doi : 10.1002/0470845015.cu0044 . Numer ISBN 978-0470845011.
- Seaborg, GT (1968). „Elementy ponad 100, obecny stan i perspektywy na przyszłość” . Roczny Przegląd Nauki Jądrowej . 18 : 53–152. Kod Bibcode : 1968ARNPS..18...53S . doi : 10.1146/annurev.ns.18.120168.000413 .
- Scerri, Ericu. (2011). Bardzo krótkie wprowadzenie do układu okresowego, Oxford University Press, Oxford . Numer ISBN 978-0-19-958249-5.
Zewnętrzne linki
- Holler, Jim. „Obrazy g-orbitali” . Uniwersytet w Kentucky.
- Rihani, Jeries A. „Rozszerzony układ okresowy pierwiastków” .
- Scerri, Ericu. „Strona internetowa Erica Scerriego dotycząca pierwiastków i układu okresowego pierwiastków” .