Sfera koordynacyjna - Coordination sphere
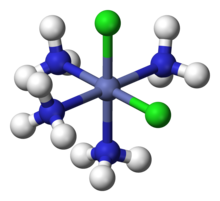
NH 3 i Cl tworzą sferę koordynacyjną wokół centralnego jonu kobaltu .
W chemii koordynacyjnej The pierwszej kuli koordynacji odnosi się do układu z cząsteczkami i jonami (na ligandy ) bezpośrednio przyłączone do centralnego atomu metalu. Sekund koordynacja kula składa się z cząsteczek i jonów przyłączone na różne sposoby do pierwszej sferze koordynacyjnej.
Pierwsza sfera koordynacji
Pierwsza sfera koordynacyjna odnosi się do cząsteczek, które są przyłączone bezpośrednio do metalu. Interakcje między pierwszą a drugą sferą koordynacyjną zwykle obejmują wiązania wodorowe. W przypadku kompleksów naładowanych ważne jest parowanie jonów .

W chlorku heksamminekobaltu (III) ([Co (NH 3 ) 6 ] Cl 3 ), kation kobaltu plus 6 ligandów amoniaku stanowią pierwszą sferę koordynacyjną. Sfera koordynacyjna tego jonu składa się zatem z centralnego rdzenia MN 6 „ozdobionego” 18 wiązaniami N-H, które promieniują na zewnątrz.
Druga sfera koordynacji

Jony metali można opisać jako składające się z serii dwóch koncentrycznych sfer koordynacyjnych, pierwszej i drugiej. Bardziej oddalone od drugiej sfery koordynacyjnej cząsteczki rozpuszczalnika zachowują się bardziej jak „ rozpuszczalnik w masie ”. Symulacja drugiej sfery koordynacji jest przedmiotem zainteresowania chemii obliczeniowej . Druga sfera koordynacyjna może składać się z jonów (zwłaszcza w naładowanych kompleksach), cząsteczek (zwłaszcza tych, które wiążą się z ligandami w pierwszej sferze koordynacyjnej) i części szkieletu liganda. W porównaniu do pierwszej sfery koordynacyjnej druga sfera koordynacyjna ma mniej bezpośredni wpływ na reaktywność i właściwości chemiczne kompleksu metalu. Niemniej jednak druga sfera koordynacyjna jest istotna dla zrozumienia reakcji kompleksu metalu, w tym mechanizmów wymiany ligandów i katalizy.
Rola w katalizie
Mechanizmy metaloprotein często wywołują modulację drugiej sfery koordynacyjnej przez białko.

Rola w mechanistycznej chemii nieorganicznej
Szybkość wymiany ligandów między pierwszą a drugą sferą koordynacyjną jest pierwszym krokiem w reakcjach podstawienia liganda. W asocjacyjnym podstawianiu ligandów wchodzący nukleofil znajduje się w drugiej sferze koordynacji. Efekty te są istotne w praktycznych zastosowaniach, takich jak środki kontrastowe stosowane w MRI .
Energetykę reakcji przenoszenia elektronów w wewnętrznej sferze omówiono w odniesieniu do drugiej sfery koordynacyjnej. Niektóre reakcje przenoszenia elektronów sprzężone z protonami obejmują przenoszenie atomów między drugimi sferami koordynacyjnymi reagentów:
- [Fe * (H 2 O) 6 ] 2+ + [Fe (H 2 O) 5 (OH)] 2+ → [Fe (H 2 O) 6 ] 3+ + [Fe * (H 2 O) 5 ( OH)] 2+
Rola w spektroskopii
Wpływ rozpuszczalnika na kolory i stabilność często można przypisać zmianom w drugiej sferze koordynacji. Takie efekty można wyrazić w kompleksach, w których ligandy w pierwszej sferze koordynacyjnej są silnymi donorami i akceptorami wiązań wodorowych, np. Odpowiednio [Co (NH 3 ) 6 ] 3+ i [Fe (CN) 6 ] 3− . Etery koronowe wiążą się z kompleksami poliamin poprzez drugą sferę koordynacyjną. Kationy poliamoniowe wiążą się z centrami azotowymi cyjanometalanów.
Rola w chemii supramolekularnej
Cząsteczki makrocykliczne, takie jak cyklodekstryny, często pełnią rolę drugiej sfery koordynacyjnej dla kompleksów metali.
Zobacz też
Dalsza lektura
Bibliografia
- ^ Zhao, Meng; Wang, Hai-Bo; Ji, Liang-Nian; Mao, Zong-Wan (2013). „Wgląd w mikrośrodowiska metaloenzymów: biomimetyczne kompleksy metali z funkcjonalną drugą sferą koordynacyjną” . Recenzje Towarzystwa Chemicznego . 42 (21): 8360. doi : 10.1039 / c3cs60162e . ISSN 0306-0012 .
- ^ Yang, JY; Chen, S .; Dougherty, WG; Kassel, WS; Bullock, RM; DuBois, DL; Raugei, S .; Rousseau, R .; Dupuis, M .; Rakowski DuBois, M. (2010). „Kataliza utleniania wodoru przez kompleks difosfiny niklu z bocznymi tert-butyloaminami”. Chem. Commun . 46 (45): 8618–8620. doi : 10.1039 / c0cc03246h . PMID 20938535 .
- ^ Bullock, RM; Helm, ML (2015). „Molekularne elektrokatalizatory do utleniania wodoru przy użyciu metali występujących w dużej ilości w ziemi: przepychanie protonów wokół przekaźników protonowych” . Acc. Chem. Res . 48 (7): 2017–2026. doi : 10.1021 / acs.accounts.5b00069 . OSTI 1582563 . PMID 26079983 .
- ^ RM Supkowski, W. DeW. Horrocks Jr. „O oznaczaniu liczby cząsteczek wody q, koordynowanych do jonów europu (III) w roztworze z czasów rozpadu luminescencji” Inorganic Chimica Acta 2002, tom 340, str. 44–48. doi : 10.1016 / S0020-1693 (02) 01022-8
- ^ Lehn, JM Supramolecular Chemistry: Concepts and Perspectives; VCH: Weinhiem, 1995.
- ^ Z. Liu, ST Schneebeli, JF Stoddart „Koordynacja drugiej sfery zrewidowana” Chimia 2014, 68, 315-320. doi : 10.2533 / chimia.2014.315
- ^ Z. Liu, M. Frasconi, J. Lei, ZJ Brown, Z. Zhu, D. Cao, J. Iehl, G. Liu, AC Fahrenbach, OK Farha, JT Hupp, CA Mirkin, YY Botros, JF Stoddart ” Selektywna izolacja złota ułatwiona przez koordynację drugiej sfery z alfa-cyklodekstryną "Nature Communications 2013, 4, 1855. doi : 10.1038 / ncomms2891
