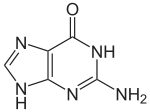
Guanina - Guanine
|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
2-Amino-1,9-dihydro- 6H -puryn-6-on |
|||
| Inne nazwy
2-amino-6-hydroksypuryna,
2-aminohipoksantyna, guanina |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| 147911 | |||
| CZEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Karta informacyjna ECHA |
100.000.727 |
||
| Numer WE | |||
| 431879 | |||
| KEGG | |||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS | |||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 5 H 5 N 5 O | |||
| Masa cząsteczkowa | 151,13 g/mol | ||
| Wygląd zewnętrzny | Białe, amorficzne ciało stałe. | ||
| Gęstość | 2,200 g / cm 3 (obliczona) | ||
| Temperatura topnienia | 360 ° C (680 ° F; 633 K) rozkłada się | ||
| Temperatura wrzenia | Wzniosłość | ||
| Nierozpuszczalny. | |||
| Kwasowość (p K a ) | 3,3 (amid), 9,2 (wtórny), 12,3 (pierwotny) | ||
| Zagrożenia | |||
| Główne zagrożenia | Drażniący | ||
| NFPA 704 (ognisty diament) | |||
| Temperatura zapłonu | Nie palne | ||
| Związki pokrewne | |||
|
Związki pokrewne
|
cytozyna ; adenina ; Tymina ; Uracyl | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
Guaniny ( / ɡ w ɑ n ɪ N / ) ( symbol G lub Gua ) jest jednym z czterech głównych nukleinowych znajdują się w kwasów nukleinowych DNA i RNA , reszta jest adenina , cytozyna i tymina ( uracyl w RNA). W DNA guanina jest sparowana z cytozyną. Nukleozyd guaniny nazywa się guanozyną .
O wzorze C 5 H 5 N 5 O guanina jest pochodną puryny , składającą się ze skondensowanego układu pierścieni pirymidyno - imidazolowych ze sprzężonymi wiązaniami podwójnymi. Ten nienasycony układ oznacza, że bicykliczna cząsteczka jest płaska.
Nieruchomości
Guanina wraz z adeniną i cytozyną jest obecna zarówno w DNA, jak i RNA, podczas gdy tymina jest zwykle widoczna tylko w DNA, a uracyl tylko w RNA. Guanina ma dwie formy tautomeryczne , główną formę ketonową (patrz rysunki) i rzadką formę enolową .
Wiąże się z cytozyną poprzez trzy wiązania wodorowe . W cytozynie grupa aminowa działa jako donor wiązania wodorowego, a karbonyl C-2 i N-3 amina jako akceptory wiązania wodorowego. Guanina ma grupę karbonylową C-6, która działa jako akceptor wiązania wodorowego, podczas gdy grupa przy N-1 i grupa aminowa przy C-2 działają jako donory wiązań wodorowych.
Guaninę można hydrolizować mocnym kwasem do glicyny , amoniaku , dwutlenku węgla i tlenku węgla . Po pierwsze, guanina ulega deaminacji i staje się ksantyną . Guanina utlenia się łatwiej niż adenina, inna zasada będąca pochodną puryny w DNA. Jego wysoka temperatura topnienia 350 °C odzwierciedla międzycząsteczkowe wiązania wodorowe między grupami okso i aminowymi w cząsteczkach kryształu. Z powodu tego międzycząsteczkowego wiązania guanina jest stosunkowo nierozpuszczalna w wodzie, ale jest rozpuszczalna w rozcieńczonych kwasach i zasadach.
Historia
Pierwsza izolacja guaniny została zgłoszona w 1844 r. przez niemieckiego chemika Juliusa Bodo Ungera (1819–1885), który pozyskał ją jako minerał powstały z odchodów ptaków morskich, znany jako guano i który był używany jako źródło nawozu; guanina została nazwana w 1846 roku. W latach 1882-1906 Hermann Emil Fischer określił strukturę i wykazał również, że kwas moczowy można przekształcić w guaninę.
Synteza
Śladowe ilości guaniny przez polimeryzację z cyjanku amonu ( NH
4CN ). Dwa eksperymenty przeprowadzone przez Levy et al. wykazali, że ogrzewanie 10 mol·L -1 NH
4CN w temperaturze 80 °C przez 24 godziny dał wydajność 0,0007%, przy użyciu 0,1 mol·L -1 NH
4CN zamrożony w temperaturze -20°C przez 25 lat dał wydajność 0,0035%. Wyniki te wskazują, że guanina może powstawać w zamarzniętych regionach prymitywnej ziemi. W 1984 r. Yuasa doniósł o wydajności 0,00017% guaniny po wyładowaniu elektrycznym NH
3, CH
4, C
2h
6i 50 ml wody, a następnie hydroliza kwasowa. Nie wiadomo jednak, czy obecność guaniny nie była po prostu wynikowym zanieczyszczeniem reakcji.
- 10NH 3 + 2CH 4 + 4C 2 H 6 + 2 H 2 O → 2C 5 H 8 N 5 O (guanina) + 25H 2
Fischera-Tropscha Syntezę można również stosować do wytwarzania guaniny oraz adenina , uracyl i tyminy . Ogrzewając równomolowe mieszaniny gazowej CO, H 2 i NH 3 do 700 ° C przez 15 do 24 minut, a następnie gwałtownego schłodzenia, po czym podtrzymująca podgrzewania 100 do 200 ° C przez 16 do 44 godzin, w obecności katalizatora tlenku glinu uzyskano guanina i uracyl:
- 10CO + H 2 + 10NH 3 → 2C 5 H 8 N 5 O (guanina) + 8 H 2 O
Inną możliwą drogę abiotyczną zbadano przez hartowanie plazmy wysokotemperaturowej mieszaniny gazów 90% N 2 –10% CO–H 2 O.
Synteza Traubego polega na ogrzewaniu 2,4,5-triamino-1,6-dihydro-6-oksypirymidyny (w postaci siarczanu) z kwasem mrówkowym przez kilka godzin.

Biosynteza
Guanina nie jest syntetyzowana de novo , zamiast tego jest oddzielana od bardziej złożonej cząsteczki, guanozyny , przez enzym fosforylazy guanozyny :
- guanozyna + fosforan guanina + alfa-D-rybozo-1-fosforan
Inne zdarzenia i zastosowania biologiczne
Słowo guanina pochodzi od hiszpańskiego zapożyczenia guano („odchody ptaków/nietoperzy”), które samo w sobie pochodzi od słowa wanu w języku keczua , co oznacza „łajno”. Jak zauważa Oxford English Dictionary , guanina to „biała bezpostaciowa substancja pozyskiwana obficie z guana, stanowiąca składnik odchodów ptaków”.
W 1656 roku w Paryżu pan Jaquin wydobył z łusek ryby Alburnus alburnus tak zwaną „esencję perłową”, czyli krystaliczną guaninę. W przemyśle kosmetycznym krystaliczną guaninę stosuje się jako dodatek do różnych produktów (np. szamponów), gdzie nadaje perłowo- opalizujący efekt. Jest również stosowany w farbach metalicznych oraz symulowanych perłach i tworzywach sztucznych. Nadaje połyskujący połysk cieniom do powiek i lakierom do paznokci . Zabiegi na twarz z użyciem odchodów lub guano japońskich słowików były stosowane w Japonii i innych krajach, ponieważ guanina w odchodach sprawia, że skóra wygląda jaśniej. Kryształy guaniny to rombowe płytki składające się z wielu przezroczystych warstw, ale mają wysoki współczynnik załamania światła, który częściowo odbija i przepuszcza światło z warstwy na warstwę, tworząc w ten sposób perłowy połysk. Może być nakładany przez natrysk, malowanie lub zanurzanie. Może podrażniać oczy. Jego alternatywą jest mika , sztuczna perła (z mielonych muszli) oraz drobinki aluminium i brązu .
Guanina ma bardzo różnorodne zastosowania biologiczne, które obejmują szereg funkcji, zarówno pod względem złożoności, jak i wszechstronności. Obejmują one między innymi kamuflaż, wyświetlanie i wizję.
Pająki, skorpiony i niektóre płazy przekształcają amoniak, jako produkt metabolizmu białek w komórkach, w guaninę, ponieważ może być wydalany przy minimalnej utracie wody.
Guanina znajduje się również w wyspecjalizowanych komórkach skóry ryb zwanych irydocytami (np. jesiotra ), a także w odblaskowych złogach oczu ryb głębinowych i niektórych gadów , takich jak krokodyle .
W dniu 8 sierpnia 2011 r. opublikowano raport, oparty na badaniach NASA z meteorytami znalezionymi na Ziemi, sugerujący, że elementy budulcowe DNA i RNA (guanina, adenina i pokrewne cząsteczki organiczne ) mogły powstawać poza Ziemią w przestrzeni kosmicznej.
Zobacz też
Bibliografia
Zewnętrzne linki
- Widmo guaniny MS
- Guanina na Chemicalland21.com