Heksan - Hexane
|
|
|

|
|

|
|

|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
Heksan |
|
| Inne nazwy
Sekstan, heksakarban
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| 1730733 | |
| CZEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| Karta informacyjna ECHA |
100.003.435 |
| Numer WE | |
| 1985 | |
| KEGG | |
| Siatka | n-heksan |
|
Identyfikator klienta PubChem
|
|
| Numer RTECS | |
| UNII | |
| Numer ONZ | 1208 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 6 H 14 | |
| Masa cząsteczkowa | 86,178 g·mol -1 |
| Wygląd zewnętrzny | Bezbarwna ciecz |
| Zapach | Benzyna |
| Gęstość | 0,6606 g ml -1 |
| Temperatura topnienia | -96 do -94°C; -141 do -137 ° F; 177 do 179 tys |
| Temperatura wrzenia | 68,5 do 69,1 °C; 155,2 do 156,3 °F; 341,6 do 342,2 K |
| 9,5 mg l- 1 | |
| log P | 3,764 |
| Ciśnienie pary | 17,60 kPa (przy 20,0 °C) |
|
Stała prawa Henry'ego ( k H ) |
7,6 nmol Pa -1 kg -1 |
| UV-vis (λ max ) | 200 nm |
| -74,6 x 10 -6 cm 3 / mol | |
|
Współczynnik załamania ( n D )
|
1,375 |
| Lepkość | 0,3 mPa·s |
| 0,08 D | |
| Termochemia | |
|
Pojemność cieplna ( C )
|
265,2 JK -1 mol -1 |
|
Standardowa
entropia molowa ( S |
296,06 JK -1 mol -1 |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-199.4–198,0 kJ mol -1 |
|
Standardowa entalpia
spalania (Δ c H ⦵ 298 ) |
-4180–-4140 kJ mol -1 |
| Zagrożenia | |
| Główne zagrożenia | Toksyczny wpływ na reprodukcję – po aspiracji , obrzęk płuc , zapalenie płuc |
| Arkusz danych dotyczących bezpieczeństwa | Zobacz: strona danych |
| Piktogramy GHS |
   
|
| Hasło ostrzegawcze GHS | Niebezpieczeństwo |
| H225 , H302 , H305 , H315 , H336 , H361fd , H373 , H411 | |
| P201 , P202 , P210 , P233 , P240 , P241 , P242 , P243 , P260 , P264 , P271 , P273 , P280 , P281 , P301 + 330 + 331 , P310 , P302 + 352 , P303 + 361 + 353 , P304 + 340 , P312 , P308 + 313 , P314 , P332 + 313 , P363 , P370 + 378 | |
| NFPA 704 (ognisty diament) | |
| Temperatura zapłonu | -26,0 ° C (-14,8 ° F; 247,2 K) |
| 234,0 ° C (453,2 ° F; 507,1 K) | |
| Granice wybuchowości | 1,2-7,7% |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
25 g kg- 1 (doustnie, szczur) 28710 mg/kg (szczur, doustnie) |
|
LD Lo ( najniższa opublikowana )
|
56137 mg/kg (szczur, doustnie) |
| NIOSH (limity ekspozycji dla zdrowia w USA): | |
|
PEL (dopuszczalne)
|
TWA 500 ppm (1800 mg/m 3 ) |
|
REL (zalecane)
|
TWA 50 ppm (180 mg/m 3 ) |
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
1100 ppm |
| Związki pokrewne | |
|
Powiązane alkany
|
|
| Strona z danymi uzupełniającymi | |
|
Współczynnik załamania ( n ), stała dielektryczna (ε r ) itp. |
|
|
Dane termodynamiczne |
Zachowanie fazowe ciało stałe-ciecz-gaz |
| UV , IR , NMR , MS | |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Heksan ( / H ɛ k s eɪ n / ) jest związek organiczny , prostołańcuchowy alkan o sześciu atomach węgla i ma wzór cząsteczkowy C 6 H 14 .
Heksan jest istotnym składnikiem benzyny . Jest to bezbarwna ciecz, bezwonna w stanie czystym, o temperaturze wrzenia około 69 °C (156 °F). Jest szeroko stosowany jako tani, stosunkowo bezpieczny, w dużej mierze niereaktywny i łatwo odparowujący niepolarny rozpuszczalnik .
Określenie heksany odnosi się do mieszaniny , składającej się głównie (> 60%) w heksanie, z różnymi ilościami związków izomerycznych 2-metylopentan i 3-metylopentanu i ewentualnie mniejszych ilości nonisomeric C 5 C 6 i C 7 (cyklo)alkany. Heksany są tańsze niż heksan i są często stosowane w operacjach na dużą skalę, niewymagających pojedynczego izomeru (np. jako rozpuszczalnik czyszczący lub do chromatografii ).
Izomery
| Nazwa zwyczajowa | Nazwa IUPAC | Formuła tekstowa | Formuła szkieletowa |
|---|---|---|---|
|
normalny heksan n -heksan |
heksan | CH 3 (CH 2 ) 4 CH 3 |
|
| izoheksan | 2-metylopentan | (CH 3 ) 2 CH(CH 2 ) 2 CH 3 |
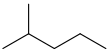
|
| 3-metylopentan | CH 3 CH 2 CH (CH 3 ) CH 2 CH 3 |
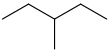
|
|
| 2,3-dimetylobutan | (CH 3 ) 2 CHCH (CH 3 ) 2 |
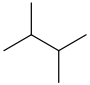
|
|
| neoheksan | 2,2-dimetylobutan | (CH 3 ) 3 CCH 2 CH 3 |
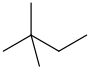
|
Zastosowania
W przemyśle heksany są wykorzystywane do produkcji klejów do butów, wyrobów skórzanych i pokryć dachowych. Są również używane do ekstrakcji olejów spożywczych (takich jak olej rzepakowy lub olej sojowy) z nasion, do czyszczenia i odtłuszczania różnych przedmiotów oraz do produkcji tekstyliów. Są one powszechnie stosowane w ekstrakcji oleju sojowego na bazie żywności w Stanach Zjednoczonych i są potencjalnie obecne jako zanieczyszczenia we wszystkich produktach spożywczych sojowych, w których stosowana jest ta technika; brak regulacji przez FDA tego zanieczyszczenia jest kwestią kontrowersji.
Typowym laboratoryjnym zastosowaniem heksanów jest ekstrakcja zanieczyszczeń olejowych i tłuszczowych z wody i gleby do analizy. Ponieważ heksan nie może być łatwo deprotonowany , jest on używany w laboratorium do reakcji, które wymagają bardzo silnych zasad, takich jak wytwarzanie litów organicznych . Na przykład butylolity są zazwyczaj dostarczane w postaci roztworu w heksanie.
Heksany są powszechnie stosowane w chromatografii jako rozpuszczalnik niepolarny. Wyższe alkany obecne jako zanieczyszczenia w heksanach mają podobne czasy retencji jak rozpuszczalnik, co oznacza, że frakcje zawierające heksan również będą zawierać te zanieczyszczenia. W chromatografii preparatywnej, stężenie dużej objętości heksanów może skutkować w próbce znacznie zanieczyszczonej alkanami. Może to skutkować otrzymaniem stałego związku w postaci oleju, a alkany mogą zakłócać analizę.
Produkcja
Heksany pozyskiwane są głównie poprzez rafinację ropy naftowej . Dokładny skład frakcji zależy w dużej mierze od źródła ropy (surowej lub reformowanej) oraz ograniczeń rafinacji. Produktem przemysłowym (zwykle około 50% wagowych izomeru o łańcuchu prostym) jest frakcja wrząca w temperaturze 65-70 ° C (149-158 ° F).
Właściwości fizyczne
Wszystkie alkany są bezbarwne. Temperatury wrzenia różnych heksanów są nieco podobne i, podobnie jak w przypadku innych alkanów, są na ogół niższe dla bardziej rozgałęzionych form. Temperatury topnienia są zupełnie inne, a tendencja nie jest widoczna.
| Izomer | MP (°C) | MP (°F) | BP (°C) | BP (°F) |
|---|---|---|---|---|
| n -heksan | -95.3 | -139,5 | 68,7 | 155,7 |
| 3-metylopentan | -118,0 | −180,4 | 63,3 | 145,9 |
| 2-metylopentan (izoheksan) | -153,7 | -244,7 | 60,3 | 140,5 |
| 2,3-dimetylobutan | -128,6 | -199,5 | 58,0 | 136,4 |
| 2,2-dimetylobutan (neoheksan) | -99.8 | −147,6 | 49,7 | 121,5 |
Heksan ma znaczną prężność pary w temperaturze pokojowej:
| Temperatura (°C) | Temperatura (°F) | Ciśnienie pary ( mmHg ) | Ciśnienie pary ( kPa ) |
|---|---|---|---|
| -40 | -40 | 3.36 | 0,448 |
| -30 | −22 | 7.12 | 0,949 |
| -20 | -4 | 14.01 | 1,868 |
| -10 | 14 | 25,91 | 3.454 |
| 0 | 32 | 45,37 | 6,049 |
| 10 | 50 | 75,74 | 10.098 |
| 20 | 68 | 121,26 | 16.167 |
| 25 | 77 | 151,28 | 20.169 |
| 30 | 86 | 187.11 | 24,946 |
| 40 | 104 | 279,42 | 37,253 |
| 50 | 122 | 405,31 | 54.037 |
| 60 | 140 | 572,76 | 76,362 |
Reaktywność
Podobnie jak większość alkanów, heksan charakteryzuje się niską reaktywnością i jest odpowiednim rozpuszczalnikiem dla związków reaktywnych. Próbki handlowe n-heksanu jednak często zawierają metylocyklopentan , który zawiera trzeciorzędowe wiązania CH, które są niekompatybilne z niektórymi reakcjami rodnikowymi.
Bezpieczeństwo
Wdychanie n -heksanu przy 5000 ppm przez 10 minut powoduje wyraźne zawroty głowy; 2500-1000 ppm przez 12 godzin powoduje senność , zmęczenie , utratę apetytu i parestezje w dystalnych kończynach; 2500–5000 ppm powoduje osłabienie mięśni , pulsację zimna w kończynach, niewyraźne widzenie, ból głowy i anoreksję . Wykazano, że przewlekła ekspozycja zawodowa na podwyższone poziomy n-heksanu jest związana z neuropatią obwodową w mechanice samochodowej w USA oraz neurotoksycznością u pracowników pras drukarskich oraz fabryk obuwia i mebli w Azji, Europie i Ameryce Północnej.
Amerykański Narodowy Instytut Zdrowia i Bezpieczeństwa Pracy (NIOSH) ustalił dopuszczalnych zalecanych ekspozycji (REL) dla izomerów heksanu (nie n-heksan), 100 ppm (350 mg / m 3 (0,15 g / stóp sześciennych)) dla 8 -godzinny dzień roboczy. Jednakże, dla n-heksanu, obecny NIOSH REL 50 ppm (180 mg / m 3 (0,079 g / stóp sześciennych)) dla 8-godzinnego dnia pracy. Limit ten został zaproponowany jako dopuszczalny limit narażenia (PEL) przez Administrację Bezpieczeństwa i Zdrowia w Pracy w 1989 roku; jednak ten PEL został uchylony w sądach amerykańskich w 1992 roku. Obecny PEL n-heksanu w USA wynosi 500 ppm (1800 mg/m 3 (0,79 gr/stopę sześcienną)).
Heksan i inne lotne węglowodory ( eter naftowy ) stwarzają ryzyko aspiracji . n- Heksan jest czasami stosowany jako denaturant alkoholu oraz jako środek czyszczący w przemyśle tekstylnym , meblarskim i skórzanym. Jest powoli zastępowany innymi rozpuszczalnikami.
Podobnie jak benzyna, heksan jest bardzo lotny i stwarza ryzyko wybuchu. Zapłon oparów heksanu, które zostały nielegalnie wyrzucone do ścieków w Louisville (Kentucky) z zakładu przetwórstwa soi należącego do Ralston-Purina, spowodował serię eksplozji, które zniszczyły ponad 21 km linii kanalizacyjnych i ulic w tym mieście.
Incydenty
Zawodowe zatrucie heksanem wystąpiło u japońskich sandałowców , włoskich szewców , tajwańskich pracowników impregnacji prasy i innych. Analiza pracowników tajwańskich wykazała narażenie zawodowe na substancje, w tym n -heksan. W latach 2010-2011 chińscy pracownicy produkujący iPhone'y doznali zatrucia heksanem.
Hexane został zidentyfikowany jako przyczyna eksplozji kanalizacji w Louisville w dniu 13 lutego 1981 roku, która zniszczyła ponad 13 mil (21 km) linii kanalizacyjnych i ulic w centrum Louisville w stanie Kentucky w Stanach Zjednoczonych
Biotransformacja
n- Heksan ulega w organizmie biotransformacji do 2-heksanolu, a następnie do 2,5-heksanodiolu . Konwersja jest katalizowana przez enzym cytochrom P450 wykorzystujący tlen z powietrza. 2,5- heksanodiol może ulegać dalszemu utlenieniu do 2,5- heksanodionu , który jest neurotoksyczny i wywołuje polineuropatię . W związku z tym zachowaniem omówiono zastąpienie n -heksanu jako rozpuszczalnika. Możliwą alternatywą jest n- heptan .
Zobacz też
Bibliografia
Linki zewnętrzne
- Międzynarodowa Karta Bezpieczeństwa Chemicznego 1262 (2-metylopentan)
- Karta charakterystyki dla heksanu
- Krajowa Inwentaryzacja Zanieczyszczeń – arkusz informacyjny n -heksanu
- Wpis do bazy fitochemicznej
- Centrum Kontroli i Zapobiegania Chorobom
- Ostrzeżenie Krajowej Rady Bezpieczeństwa „WSPÓLNY WPŁYW CHEMICZNY NA MECHANIKA SAMOCHODOWĄ”
- Australijskie krajowym wykazie substancji zanieczyszczających (NPI) strona
- „EPA nie uważa n-heksanu za czynnik rakotwórczy u ludzi”. Rejestr Federalny / tom. 66, nr 71 / czwartek, 12 kwietnia 2001 / Regulamin

