Chlorek wodoru - Hydrogen chloride
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Nazwa IUPAC
Chlorek wodoru
|
|||
| Inne nazwy
Gazowy kwas solny
Gaz chlorowodorowy |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| 1098214 | |||
| CZEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.028.723 |
||
| Numer WE | |||
| 322 | |||
| KEGG | |||
| Siatka | Kwas chlorowodorowy | ||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS | |||
| UNII | |||
| Numer ONZ | 1050 | ||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| HCl | |||
| Masa cząsteczkowa | 36,46 g/mol | ||
| Wygląd zewnętrzny | Bezbarwny gaz | ||
| Zapach | ostry; ostry i płonący | ||
| Gęstość | 1,49 g/L | ||
| Temperatura topnienia | -114,22 ° C (-173,60 ° F; 158,93 K) | ||
| Temperatura wrzenia | -85,05 ° C (-121,09 ° F; 188,10 K) | ||
| 823 g/L (0 °C) 720 g/L (20 °C) 561 g/L (60 °C) |
|||
| Rozpuszczalność | rozpuszczalny w metanolu , etanolu , eterze | ||
| Ciśnienie pary | 4352 kPa (przy 21,1 °C) | ||
| Kwasowość (p K a ) | −3,0; -5,9 (±0,4) | ||
| Zasadowość (p K b ) | 17,0 | ||
| Kwas sprzężony | Chloron | ||
| Podstawa sprzężona | Chlorek | ||
|
Współczynnik załamania ( n D )
|
1.0004456 (gaz) 1.254 (ciecz) |
||
| Lepkość | 0,311 cP (-100 °C) | ||
| Struktura | |||
| liniowy | |||
| 1,05 D | |||
| Termochemia | |||
|
Pojemność cieplna ( C )
|
0,7981 J/(Kg) | ||
|
Standardowa
entropia molowa ( S |
186.902 J/(K·mol) | ||
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-92,31 kJ/mol | ||
|
Standardowa entalpia
spalania (Δ c H ⦵ 298 ) |
-95,31 kJ/mol | ||
| Farmakologia | |||
| A09AB03 ( KTO ) B05XA13 ( KTO ) | |||
| Zagrożenia | |||
| Arkusz danych dotyczących bezpieczeństwa | Karta charakterystyki JT Baker | ||
| Piktogramy GHS |
 
|
||
| Hasło ostrzegawcze GHS | Zagrożenie | ||
| H280 , H314 , H331 | |||
| P261 , P280 , P305+351+338 , P310 , P410+403 | |||
| NFPA 704 (ognisty diament) | |||
| Dawka lub stężenie śmiertelne (LD, LC): | |||
|
LD 50 ( mediana dawki )
|
238 mg/kg (szczur, doustnie) | ||
|
LC 50 ( mediana stężenia )
|
3124 ppm (szczur, 1 godz. ) 1108 ppm (mysz, 1 godz.) |
||
|
LC Lo ( najniższa opublikowana )
|
1300 ppm (człowiek, 30 min ) 4416 ppm (królik, 30 min) 4416 ppm (świnka morska, 30 min) 3000 ppm (człowiek, 5 min) |
||
| NIOSH (limity ekspozycji dla zdrowia w USA): | |||
|
PEL (dopuszczalne)
|
C 5 ppm (7 mg/m 3 ) | ||
|
REL (zalecane)
|
C 5 ppm (7 mg/m 3 ) | ||
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
50 ppm | ||
| Związki pokrewne | |||
|
Związki pokrewne
|
Fluorowodór bromowodoru , jodowodoru astatowodór |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
Związek chlorowodór ma Wzór chemiczny HCli jako taki jest halogenowodorem . W temperaturze pokojowej jest gazem bezbarwnym , który w kontakcie z parą wodną z powietrza tworzy białe opary kwasu solnego . Gazowy chlorowodór i kwas solny są ważne w technologii i przemyśle. Kwas chlorowodorowy, wodny roztwór chlorowodoru, jest również powszechnie określany wzorem HCl.
Reakcje
Chlorowodór to dwuatomowa cząsteczka składająca się z atomu wodoru H i atomu chloru Cl połączonych polarnym wiązaniem kowalencyjnym . Atom chloru jest znacznie bardziej elektroujemny niż atom wodoru, co sprawia, że to wiązanie jest polarne. W konsekwencji cząsteczka ma duży moment dipolowy z ujemnym ładunkiem częściowym (δ−) przy atomie chloru i dodatnim ładunkiem częściowym (δ+) przy atomie wodoru. Częściowo ze względu na wysoką polarność HCl jest bardzo dobrze rozpuszczalny w wodzie (i innych rozpuszczalnikach polarnych ).
W kontakcie H 2 O i HCl łączą się, tworząc kationy hydroniowe H 3 O + i aniony chlorkowe Cl − poprzez odwracalną reakcję chemiczną :
- HCl + H 2 O → H 3 O + + Cl −
Powstały roztwór nazywa się kwasem solnym i jest mocnym kwasem . Dysocjacji kwasu lub stałe jonizacji, K , jest duża, co oznacza, że odcina HCl i jonizuje praktycznie całkowicie w wodzie. Nawet przy braku wody chlorowodór może nadal działać jak kwas. Na przykład chlorowodór może rozpuszczać się w niektórych innych rozpuszczalnikach, takich jak metanol :
- HCI + CH 3 OH → CH 3 O + H 2 + CI -
Chlorowodór może protonować cząsteczki lub jony, a także może służyć jako katalizator kwasowy w reakcjach chemicznych, w których pożądane są warunki bezwodne ( bezwodne ).
Ze względu na kwasowy charakter chlorowodór jest substancją żrącą , szczególnie w obecności wilgoci.
Struktura i właściwości
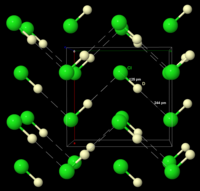
Zamrożony HCl przechodzi przemianę fazową w temperaturze 98,4 K. Rentgenowska dyfrakcja proszkowa zamrożonego materiału pokazuje, że podczas tego przejścia materiał zmienia się ze struktury rombowej na sześcienną . W obu strukturach atomy chloru znajdują się w układzie twarzocentrycznym . Nie udało się jednak zlokalizować atomów wodoru. Analiza danych spektroskopowych i dielektrycznych oraz określenie struktury DCl (chlorku deuteru) wskazuje, że HCl tworzy w ciele stałym łańcuchy zygzakowate, podobnie jak HF (patrz rysunek po prawej).
| Temperatura (°C) | 0 | 20 | 30 | 50 |
|---|---|---|---|---|
| Woda | 823 | 720 | 673 | 596 |
| Metanol | 513 | 470 | 430 | |
| Etanol | 454 | 410 | 381 | |
| Eter | 356 | 249 | 195 |
Widmo w podczerwieni z gazowego chlorowodoru, pokazanym po lewej stronie, składa się z kilku ostrych linii absorpcyjnych zgrupowane wokół 2886 cm -1 (długość fali ~ 3,47 urn). W temperaturze pokojowej prawie wszystkie cząsteczki znajdują się w podstawowym stanie wibracyjnym v = 0. Uwzględniając anharmonikę, energię wibracyjną można zapisać jako.
Aby promować cząsteczkę HCl ze stanu v = 0 do stanu v = 1, spodziewalibyśmy się absorpcji w podczerwieni około ν o = ν e + 2 x e ν e = 2880 cm −1 . Jednak ta absorpcja odpowiadająca gałęzi Q nie jest obserwowana, ponieważ jest zabroniona przez symetrię. Zamiast tego widoczne są dwa zestawy sygnałów (gałęzie P i R) z powodu jednoczesnej zmiany stanu rotacyjnego cząsteczek. Ze względu na zasady doboru mechaniki kwantowej dozwolone są tylko niektóre przejścia rotacyjne. Stany charakteryzują się rotacyjną liczbą kwantową J = 0, 1, 2, 3, ... reguły wyboru mówią, że Δ J może przyjmować tylko wartości ±1.
Wartość stałej obrotowej B jest znacznie mniejsza niż oscylacyjnej ν o , tak że do obracania cząsteczki potrzebna jest znacznie mniejsza ilość energii; dla typowej cząsteczki leży ona w obszarze mikrofalowym. Jednak energia wibracyjna cząsteczki HCl umieszcza jej absorpcję w obszarze podczerwieni, umożliwiając łatwe zebranie widma pokazującego przejścia rowibracyjne tej cząsteczki za pomocą spektrometru podczerwieni z ogniwem gazowym. Ten ostatni może być nawet wykonany z kwarcu, ponieważ absorpcja HCl znajduje się w oknie przezroczystości dla tego materiału.
Naturalnie obfity chlor składa się z dwóch izotopów, 35 Cl i 37 Cl, w stosunku około 3:1. Podczas gdy stałe sprężystości są prawie identyczne, rozbieżne zredukowane masy H 35 Cl i H 37 Cl powodują wymierne różnice w energii obrotowej, stąd dublety obserwuje się przy bliższym przyjrzeniu się każdej linii absorpcji, ważonej w tym samym stosunku 3:1.
Produkcja
Większość chlorowodoru produkowanego na skalę przemysłową jest wykorzystywana do produkcji kwasu solnego .
Trasy historyczne
W XVII wieku Johann Rudolf Glauber z Karlstadt nad Menem w Niemczech użył soli chlorkowo-sodowej i kwasu siarkowego do przygotowania siarczanu sodu w procesie Mannheima , uwalniając chlorowodór. Joseph Priestley z Leeds w Anglii wytworzył czysty chlorowodór w 1772 r., a do 1808 r. Humphry Davy z Penzance w Anglii udowodnił, że skład chemiczny zawierał wodór i chlor .
Synteza bezpośrednia
Chlorowodór powstaje w wyniku połączenia chloru i wodoru :
- Cl 2 + H 2 → 2 HCl
Ponieważ reakcja jest egzotermiczna , instalacja nazywana jest piecem HCl lub palnikiem HCl. Powstały gazowy chlorowodór jest absorbowany w wodzie dejonizowanej , w wyniku czego powstaje chemicznie czysty kwas chlorowodorowy. Ta reakcja może dać bardzo czysty produkt, np. do zastosowania w przemyśle spożywczym.
Synteza organiczna
Przemysłowa produkcja chlorowodoru jest często zintegrowana z powstawaniem chlorowanych i fluorowanych związków organicznych , np. teflonu , freonu i innych CFC , a także kwasu chlorooctowego i PCW . Często ta produkcja kwasu solnego jest zintegrowana z jego własnym wykorzystaniem na miejscu. W reakcjach chemicznych atomy wodoru na węglowodorze są zastępowane atomami chloru, po czym uwolniony atom wodoru łączy się z atomem zapasowym cząsteczki chloru, tworząc chlorowodór. Fluorowanie to kolejna reakcja wymiany chloru, w której ponownie powstaje chlorowodór:
- R-H + CI 2 → R-Cl + HCl
- R−Cl + HF → R−F + HCl
Powstały chlorowodór jest albo bezpośrednio ponownie wykorzystywany, albo absorbowany w wodzie, w wyniku czego powstaje kwas solny o jakości technicznej lub przemysłowej.
Metody laboratoryjne
Małe ilości chlorowodoru do użytku laboratoryjnego można wytworzyć w generatorze HCl przez odwodnienie kwasu solnego kwasem siarkowym lub bezwodnym chlorkiem wapnia . Alternatywnie, HCl można wytworzyć w reakcji kwasu siarkowego z chlorkiem sodu:
- NaCl + H 2 SO 4 → NaHSO 4 + HCl
Ta reakcja zachodzi w temperaturze pokojowej. Pod warunkiem, że w generatorze pozostanie NaCl i zostanie on podgrzany powyżej 200 °C, reakcja przebiega dalej:
- NaCl + NaHSO 4 → HCI + Na 2 SO 4
Aby takie generatory działały, odczynniki powinny być suche.
Chlorowodór można również wytwarzać przez hydrolizę niektórych reaktywnych chlorków, takich jak chlorki fosforu , chlorkiem tionylu (SOCh 2 ) oraz chlorkami acylowymi . Na przykład zimna woda może być stopniowo nakrapla się pentachlorek fosforu (PCL 5 ) uzyskując HCl:
- PCl 5 + H 2 O → POCl 3 + 2 HCl
Aplikacje
Większość chlorowodoru jest wykorzystywana do produkcji kwasu solnego. Wykorzystywany jest również do produkcji chlorku winylu i wielu chlorków alkilu . Trichlorosilan jest produkowany przy użyciu HCl:
- Si + 3 HCl → HSiCl 3 + H 2
Historia
Około roku 900 autorzy arabskich pism przypisywanych Jabirowi ibn Hayyanowi (łac. Geber) oraz perskiemu lekarzowi i alchemikowi Abu Bakr al-Razi (ok. 865–925, łac. Rhazes) eksperymentowali z salmonem ( chlorkiem amonu ). , który po destylacji wraz z witriolem (uwodnionymi siarczanami różnych metali) wytworzył chlorowodór. Wydaje się jednak, że w tych wczesnych eksperymentach z solami chlorkowymi produkty gazowe zostały odrzucone, a chlorowodór mógł być wytwarzany wiele razy, zanim odkryto, że można go zastosować w chemii. Jednym z pierwszych takich zastosowań była synteza chlorku rtęci(II) (sublimacja korozyjna), której wytwarzanie przez ogrzewanie rtęci z ałunem i chlorkiem amonu lub z witriolem i chlorkiem sodu zostało po raz pierwszy opisane w De aluminibus et salibus (" O ałunach i solach”, tekst arabski z XI lub XII wieku fałszywie przypisywany Abu Bakr al-Razi i przetłumaczony na łacinę w drugiej połowie XII wieku przez Gerarda z Cremony , 1144-1187). Innym ważnym osiągnięciem było odkrycie pseudo-Geber (w veritatis O inwencji „na odkryciu Prawda”, po ok. 1300), że przez dodanie chlorku amonu do kwasu azotowego , silny rozpuszczalnik zdolny do rozpuszczania złota (np wodny regia ). Po odkryciu pod koniec XVI wieku procesu, za pomocą którego można wytwarzać niezmieszany kwas solny , uznano, że ten nowy kwas (wtedy znany jako spirytus z soli lub acidum salis ) uwalniał chlorowodór w postaci pary, który nazwano kwasem morskim powietrzem . W XVII wieku Johann Rudolf Glauber używał soli ( chlorku sodu ) i kwasu siarkowego do wytwarzania siarczanu sodu , uwalniając gazowy chlorowodór (patrz produkcja powyżej). W 1772 r. Carl Wilhelm Scheele również zgłosił tę reakcję i czasami przypisuje mu się jej odkrycie. Joseph Priestley przygotował chlorowodór w 1772 roku, aw 1810 Humphry Davy ustalił, że składa się on z wodoru i chloru .
Podczas rewolucji przemysłowej wzrosło zapotrzebowanie na substancje alkaliczne , takie jak soda kalcynowana , a Nicolas Leblanc opracował nowy proces produkcji sody kalcynowanej na skalę przemysłową. W procesie Leblanc sól została przekształcona w sodę kalcynowaną przy użyciu kwasu siarkowego, wapienia i węgla, otrzymując chlorowodór jako produkt uboczny. Początkowo gaz ten był odprowadzany do powietrza, ale ustawa o alkaliach z 1863 r. zabroniła takiego uwalniania, więc producenci sody kalcynowanej zaabsorbowali gaz odlotowy HCl w wodzie, wytwarzając kwas solny na skalę przemysłową. Później opracowano proces Hargreavesa , który jest podobny do procesu Leblanc, z wyjątkiem tego, że w reakcji, która jest ogólnie egzotermiczna, zamiast kwasu siarkowego stosuje się dwutlenek siarki , wodę i powietrze. Na początku XX wieku proces Leblanc został skutecznie zastąpiony przez proces Solvaya , który nie wytwarzał HCl. Produkcja chlorowodoru była jednak kontynuowana jako etap w produkcji kwasu solnego.
Historyczne zastosowania chlorowodoru w XX wieku obejmują chlorowodorowanie alkinów w produkcji chlorowanych monomerów chloroprenu i chlorku winylu , które są następnie polimeryzowane w celu wytworzenia odpowiednio polichloroprenu ( neopren ) i polichlorku winylu (PVC). W produkcji chlorku winylu, acetylen (C 2 H 2 ) jest chlorowodorowany przez dodanie HCl w poprzek potrójnego wiązania cząsteczki C 2 H 2 , zamieniając potrójne wiązanie w podwójne wiązanie , w wyniku czego otrzymuje się chlorek winylu.
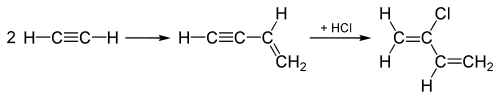
„Proces acetylenowy”, stosowany do lat 60. XX wieku do wytwarzania chloroprenu , rozpoczyna się od połączenia dwóch cząsteczek acetylenu , a następnie dodaje HCl do połączonego związku pośredniego przez wiązanie potrójne, aby przekształcić go w chloropren, jak pokazano tutaj:
Ten „proces acetylen” zostało zastąpione przez proces, który dodaje Cl 2 do podwójnego wiązania zamiast etylenu, a następnie eliminacja wytwarza HCI zamiast, jak chloropren.
Bezpieczeństwo
Chlorowodór tworzy żrący kwas solny w kontakcie z wodą znajdującą się w tkankach ciała. Wdychanie oparów może powodować kaszel , zadławienia , stany zapalne nosa, gardła i górne drogi oddechowe , aw ciężkich przypadkach obrzęku płuc , układu krążenia niewydolności i śmierci. Kontakt ze skórą może powodować zaczerwienienie, ból i poważne oparzenia chemiczne . Chlorowodór może powodować poważne oparzenia oka i trwałe uszkodzenie oczu.
Amerykańska Administracja Bezpieczeństwa i Zdrowia w Pracy oraz Narodowy Instytut Bezpieczeństwa i Zdrowia w Pracy ustaliły limity narażenia zawodowego na chlorowodór na poziomie 5 ppm (7 mg/m 3 ) i zebrały obszerne informacje dotyczące kwestii bezpieczeństwa w miejscu pracy chlorowodoru.
Zobacz też
- Kwas żołądkowy , kwas solny wydzielany w żołądku do pomocy trawienia z białek
- Chlorki , sole chlorowodorowe
- Chlorowodorek , organiczne sole kwasu solnego
- Chlorowanie , reakcja addycji z alkenami
Bibliografia
Zewnętrzne linki
- Międzynarodowa Karta Bezpieczeństwa Chemicznego 0163
- Podręcznik eksperymentów Thames & Kosmos Chem C2000