Kwas podfluorowy - Hypofluorous acid
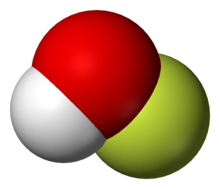
 Struktura fazy gazowej
|
|
|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Kwas podfluorowy
|
|
| Inne nazwy
Wodór hypofluorite
wodoru fluorate (-I) fluorowego (-I) Kwas wodoru monofluoroxygenate (0), grupę hydroksylową fluorek |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| HOF | |
| Masa cząsteczkowa | 36,0057 g mol -1 |
| Wygląd | bladożółta ciecz powyżej -117 ° C białe ciało stałe poniżej -117 ° C |
| Temperatura topnienia | -117 ° C (-179 ° F; 156 K) |
| Temperatura wrzenia |
rozkłada się w temperaturze 0 ° C |
| Struktura | |
| C s | |
| Zagrożenia | |
| Główne zagrożenia | silny utleniacz, żrący |
| NFPA 704 (ognisty diament) | |
| Związki pokrewne | |
|
Inne kationy
|
podfluoryt litu |
|
Związki pokrewne
|
kwas podchlorawy nitroksylo- cyjanowodór formaldehyd |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Kwas Hypofluorous , wzór chemiczny H O F , jest jedynym tlenowym fluoru, a jedyne znane kwasy tlenowe, w których głównymi zyskuje elektrony z atomów tlenu , aby utworzyć stopień utlenienia ujemny. Stopień utlenienia tlenu w podfluorynach wynosi 0. Jest to również jedyny kwas podfluorowaty, który można wyodrębnić jako ciało stałe . Hof jest pośredni w utlenianiu w wodzie przez fluor , który wytwarza się fluorowodór , difluorek tlen , nadtlenek wodoru , ozon i tlen . HOF jest wybuchowy w temperaturze pokojowej, tworząc HF i O 2 :
- 2 HOF → 2 HF + O 2
Został wyizolowany w czystej postaci przepuszczając gaz F 2 nad lodem w temperaturze -40 ° C, zbierając gaz HOF i kondensując go:
- F 2 + H 2 O → HOF + HF
Związek został scharakteryzowany w fazie stałej metodą krystalografii rentgenowskiej jako cząsteczka wygięta pod kątem 101 °. Długości wiązań O – F i O – H wynoszą odpowiednio 144,2 i 96,4 pikometrów . Solidna struktura składa się z łańcuchów z połączeniami O – H ··· O. Strukturę analizowano również w fazie gazowej, czyli w stanie, w którym kąt wiązania H – O – F jest nieco węższy (97,2 °).
Kwas podfluorowaty w acetonitrylu (wytwarzany in situ przez przepuszczanie gazowego fluoru przez „mokry” acetonitryl ) jest powszechnie znany jako odczynnik Rozena .
Podfluoryty
Podfluoryty są formalnie pochodnymi OF - , który jest sprzężoną zasadą kwasu podfluorawego. Jednym z przykładów jest podfluoryn trifluorometylu (CF 3 OF).
Zobacz też
- Kwas podchlorawy , pokrewny związek, który ma większe znaczenie technologiczne, ale nie został uzyskany w czystej postaci.

