Wodorek litowo-glinowy - Lithium aluminium hydride
|
|
|||

|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Tetrahydrydoglinian litu (III) |
|||
|
Systematyczna nazwa IUPAC
Alumanuek litu |
|||
| Inne nazwy
Wodorek litowo-glinowy
Lithal |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| Skróty | LAH | ||
| ChEBI | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.037.146 |
||
| Numer WE | |||
| 13167 | |||
|
PubChem CID
|
|||
| Numer RTECS | |||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| LiAlH 4 | |||
| Masa cząsteczkowa | 37,95 g / mol | ||
| Wygląd | białe kryształy (czyste próbki) szary proszek (materiał handlowy) higroskopijny |
||
| Zapach | bezwonny | ||
| Gęstość | 0,917 g / cm 3 , stałe | ||
| Temperatura topnienia | 150 ° C (302 ° F; 423 K) (rozkłada się) | ||
| Reaguje | |||
| Rozpuszczalność w tetrahydrofuranie | 112,332 g / l | ||
| Rozpuszczalność w eterze dietylowym | 39,5 g / 100 ml | ||
| Struktura | |||
| Jednoskośny | |||
| P 2 1 / c | |||
| Termochemia | |||
|
Pojemność cieplna ( C )
|
86,4 J / mol K | ||
|
Entropia trzonowa standardowa ( S |
87,9 J / mol K | ||
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-117 kJ / mol | ||
|
Energia swobodna Gibbsa (Δ f G ˚)
|
-48,4 kJ / mol | ||
| Zagrożenia | |||
| Arkusz danych dotyczących bezpieczeństwa | Wodorek litowo-glinowy | ||
| Piktogramy GHS |
 
|
||
| Hasło ostrzegawcze GHS | Niebezpieczeństwo | ||
| H260 , H314 | |||
| P223 , P231 + 232 , P280 , P305 + 351 + 338 , P370 + 378 , P422 | |||
| NFPA 704 (ognisty diament) | |||
| Temperatura zapłonu | 125 ° C (257 ° F, 398 K) | ||
| Związki pokrewne | |||
|
Powiązany wodorek
|
wodorek glinu borowodorek sodu wodorek sodu wodorek glinowo-sodowy |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencje Infobox | |||
Wodorek litowo-glinowy , powszechnie w skrócie LAH , jest związkiem nieorganicznym o wzorze chemicznym Li Al H 4 . Jest to szare ciało stałe. Został odkryty przez Finholta, Bonda i Schlesingera w 1947 roku. Związek ten jest stosowany jako środek redukujący w syntezie organicznej , zwłaszcza do redukcji estrów , kwasów karboksylowych i amidów . Ciało stałe jest niebezpiecznie reaktywne w stosunku do wody, uwalniając gazowy wodór (H 2 ). Omówiono niektóre pokrewne pochodne do przechowywania wodoru .
Właściwości, struktura, przygotowanie
LAH jest bezbarwną substancją stałą, ale próbki handlowe są zwykle szare z powodu zanieczyszczenia. Ten materiał można oczyścić przez rekrystalizację z eteru dietylowego . Oczyszczanie na dużą skalę wykorzystuje ekstraktor Soxhleta . Zwykle w syntezie stosuje się zanieczyszczony szary materiał, ponieważ zanieczyszczenia są nieszkodliwe i można je łatwo oddzielić od produktów organicznych. Czysty sproszkowany materiał jest piroforyczny , ale nie zawiera dużych kryształów. Niektóre materiały handlowe zawierają olej mineralny, który hamuje reakcje z wilgocią atmosferyczną, ale częściej jest on pakowany w odporne na wilgoć plastikowe worki.
LAH gwałtownie reaguje z wodą, w tym wilgocią atmosferyczną, uwalniając gaz diwodorowy. Reakcja przebiega według następującego wyidealizowanego równania:
- LiAlH 4 + 4 H 2 O → LiOH + Al (OH) 3 + 4 H 2
Ta reakcja jest użyteczną metodą wytwarzania wodoru w laboratorium. Stare, wystawione na działanie powietrza próbki często wyglądają na białe, ponieważ wchłonęły dostateczną ilość wilgoci, aby wytworzyć mieszaninę białych związków wodorotlenku litu i wodorotlenku glinu .
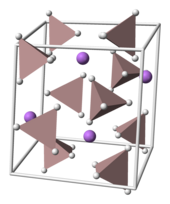
Struktura
LAH krystalizuje w jednoskośnej grupie przestrzennej P 2 1 / c . Komórki jednostkowej o wymiarach: a = 4,82, b = 7.81 i c = 7,92 A, α = γ = 90 °, β = 112 ° C. W strukturze centra Li + są otoczone przez pięć AlH -
4 czworościany . Centra Li + są związane z jednym atomem wodoru z każdego z otaczających czworościanów, tworząc układ dwipiramidowy . Przy wysokich ciśnieniach (> 2,2 GPa) może wystąpić przemiana fazowa, w wyniku której powstaje β-LAH.
Przygotowanie
LiAlH 4 został po raz pierwszy przygotowany z reakcji między wodorkiem litu (LiH) a chlorkiem glinu :
- 4 LiH + AlCl 3 → LiAlH 4 + 3 LiCl
Oprócz tej metody synteza przemysłowa polega na wstępnym przygotowaniu wodorku sodowo-glinowego z pierwiastków pod wysokim ciśnieniem i temperaturą:
- Na + Al + 2 H 2 → NaAlH 4
LiAlH 4 jest następnie przygotowywany w reakcji metatezy soli zgodnie z:
- NaAlH 4 + LiCl → LiAlH 4 + NaCl
który przebiega z dużą wydajnością. LiCl usunięto przez odsączenie z eterowego roztworu LAH z dalszego wytrącania LiAlH 4 , z wytworzeniem produktu zawierającego około 1% wagowo / wagowo LiCl.
Alternatywne przygotowanie zaczyna się od LiH i metalicznego Al zamiast AlCl 3 . Katalizowana przez małą ilością TiCl 3 (0,2%), przy czym reakcja przebiega również przy użyciu dimetylowy jako rozpuszczalnik. Ta metoda pozwala uniknąć kogeneracji soli.
Dane dotyczące rozpuszczalności
| Rozpuszczalnik | Temperatura (° C) | ||||
|---|---|---|---|---|---|
| 0 | 25 | 50 | 75 | 100 | |
| Eter dietylowy | - | 5.92 | - | - | - |
| THF | - | 2,96 | - | - | - |
| Monoglyme | 1.29 | 1.80 | 2.57 | 3.09 | 3.34 |
| Diglyme | 0,26 | 1.29 | 1.54 | 2.06 | 2.06 |
| Triglyme | 0.56 | 0,77 | 1.29 | 1.80 | 2.06 |
| Tetraglyme | 0,77 | 1.54 | 2.06 | 2.06 | 1.54 |
| Dioksan | - | 0,03 | - | - | - |
| Eter dibutylowy | - | 0.56 | - | - | - |
LAH jest rozpuszczalny w wielu eterycznych roztworach. Jednak może się samorzutnie rozkładać z powodu obecności zanieczyszczeń katalitycznych, chociaż wydaje się, że jest bardziej stabilny w tetrahydrofuranie (THF). Zatem THF jest korzystniejszy niż np. Eter dietylowy , pomimo mniejszej rozpuszczalności.
Dane termodynamiczne
Tabela podsumowuje dane termodynamiczne dla LAH i reakcji z udziałem LAH, odpowiednio w postaci standardowej entalpii , entropii i zmiany energii swobodnej Gibbsa .
| Reakcja | ΔH ° (kJ / mol) |
ΔS ° (J / (mol · K)) |
ΔG ° (kJ / mol) |
Komentarz |
|---|---|---|---|---|
| Li (s) + Al (s) + 2 H 2 (g) → LiAlH 4 (s) | −116,3 | −240,1 | −44,7 | Standardowa formacja z żywiołów. |
| LiH (s) + Al (s) + 3 / 2 H 2 (G) → LiAlH 4 (a) | −95,6 | −180,2 | 237,6 | Przy użyciu ΔH ° f (LiH) = -90,579865, ΔS ° f (LiH) = -679,9 i ΔG ° f (LiH) = -67,31235744. |
| LiAlH 4 (s) → LiAlH 4 (l) | 22 | - | - | Ciepło topnienia. Wartość może być niewiarygodna. |
| LiAlH 4 (L) → 1 / 3 Li 3 AlH 6 (a) + 2 / 3 Al (s) + H 2 (g) | 3.46 | 104,5 | −27,68 | ΔS ° obliczone na podstawie podanych wartości ΔH ° i ΔG °. |
Rozkład termiczny
LAH jest metastabilny w temperaturze pokojowej. Podczas długotrwałego przechowywania powoli rozkłada się do Li 3 AlH 6 i LiH. Proces ten można przyspieszyć dzięki obecności pierwiastków katalitycznych , takich jak tytan , żelazo czy wanad .

Po podgrzaniu LAH rozkłada się w trzystopniowym mechanizmie reakcji :
-
3 LiAlH 4 → Li 3 AlH 6 + 2 Al + 3 H 2
( R1 )
-
2 Li 3 AlH 6 → 6 LiH + 2 Al + 3 H 2
( R2 )
-
2 LiH + 2 Al → 2 LiAl + H 2
( R3 )
R1 jest zwykle inicjowane przez stopienie LAH w zakresie temperatur 150–170 ° C, po którym bezpośrednio następuje rozkład do stałego Li 3 AlH 6 , chociaż wiadomo , że R1 również przebiega poniżej temperatury topnienia LiAlH 4 . Przy około 200 ° C Li 3 AlH 6 rozkłada się na LiH ( R2 ) i Al, które następnie przekształcają się w LiAl powyżej 400 ° C ( R3 ). Reakcja R1 jest faktycznie nieodwracalna. R3 jest odwracalny przy ciśnieniu równowagowym około 0,25 bara w 500 ° C. R1 i R2 mogą występować w temperaturze pokojowej z odpowiednimi katalizatorami.
Aplikacje
Zastosowanie w chemii organicznej
Wodorek litowo-glinowy (LiAlH4) jest szeroko stosowany w chemii organicznej jako środek redukujący . Jest silniejszy niż powiązany odczynnik borowodorek sodu ze względu na słabsze wiązanie Al-H w porównaniu z wiązaniem BH. Często jako roztwór w eterze dietylowym, a następnie poddawany obróbce kwasem, przekształca estry , kwasy karboksylowe , chlorki acylowe , aldehydy i ketony w odpowiednie alkohole (patrz: redukcja karbonylowa ). Podobnie przekształca związki amidowe , nitro , nitrylowe , iminowe , oksymowe i azydkowe w aminy (patrz: redukcja amidów ). Redukuje czwartorzędowe kationy amoniowe do odpowiednich trzeciorzędowych amin. Reaktywność można regulować zastępując grupy wodorkowe grupami alkoksylowymi . Ze względu na jego piroforyczny charakter, niestabilność, toksyczność, krótki okres przydatności do spożycia i problemy z obsługą związane z jego reaktywnością, został on zastąpiony w ostatniej dekadzie, zarówno na małą skalę przemysłową, jak i na dużą skalę, przez wygodniejszy, pokrewny odczynnik sodu. Wodorek bis (2-metoksyetoksy) glinu , który wykazuje podobną reaktywność, ale z większym bezpieczeństwem, łatwiejszą obsługą i lepszą ekonomią.
LAH jest najczęściej stosowany do redukcji estrów i kwasów karboksylowych do alkoholi pierwszorzędowych; przed pojawieniem się LiAlH 4 była to trudna konwersja z udziałem metalicznego sodu we wrzącym etanolu ( redukcja Bouveault-Blanca ). Aldehydy i ketony mogą być również zredukowane do alkoholi przez LAH, ale zazwyczaj odbywa się za pomocą łagodniejsze reagentów, takich jak NaBH 4 ; α, β-nienasycone ketony są redukowane do alkoholi allilowych. Kiedy epoksydy są redukowane przy użyciu LAH, odczynnik atakuje mniej utrudniony koniec epoksydu, zwykle wytwarzając drugorzędny lub trzeciorzędowy alkohol. Epoksycykloheksany redukuje się, dając preferencyjnie alkohole osiowe.
Częściowa redukcja chlorków kwasowych do odpowiedniego produktu aldehydowego nie może przebiegać przez LAH, ponieważ ten ostatni redukuje się aż do alkoholu pierwszorzędowego. Zamiast tego należy zastosować łagodniejszy trój (t-butoksy) wodorek litowo-glinowy , który reaguje znacznie szybciej z chlorkiem kwasowym niż z aldehydem. Na przykład, gdy kwas izowalerianowy traktuje się chlorkiem tionylu z wytworzeniem chlorku izowaleroilu, można go następnie redukować tri (t-butoksy) wodorek litowo-glinowy z wytworzeniem aldehydu izowalerianowego z 65% wydajnością.

Wodorek litowo-glinowy redukuje również halogenki alkilowe do alkanów . Najszybciej reagują jodki alkilu, następnie bromki alkilu, a następnie chlorki alkilu. Halogenki pierwotne są najbardziej reaktywne, a zaraz po nich następują halogenki wtórne. Trzeciorzędowe halogenki reagują tylko w określonych przypadkach.
Wodorek litowo-glinowy nie redukuje prostych alkenów ani arenów . Alkiny są redukowane tylko wtedy, gdy w pobliżu znajduje się grupa alkoholowa. Zaobserwowano, że LiAlH4 zmniejsza wiązanie podwójne w N-alliloamidach.
Chemia nieorganiczna
LAH jest szeroko stosowany do wytwarzania wodorków grup głównych i metali przejściowych z odpowiednich halogenków metali . Na przykład wodorek sodu (NaH) można otrzymać z chlorku sodu (NaCl) w następującej reakcji:
- LiAlH 4 + 4 NaCl → 4 NaH + LiCl + AlCl 3
LAH reaguje również z wieloma nieorganicznymi ligandami, tworząc skoordynowane kompleksy tlenku glinu związane z jonami litu.
- LiAlH 4 + 4NH 3 → Li [Al (NH 2 ) 4 ] + 4H 2
Magazyn wodoru

LiAlH 4 zawiera 10,6% wagowych wodoru, a tym samym LAH potencjalne magazynowania wodoru medium dla przyszłych ogniwa parowe pojazdów . Wysoka zawartość wodoru, a także odkrycie odwracalnego magazynowania wodoru w NaAlH 4 domieszkowanym Ti zainicjowały ponowne badania nad LiAlH 4 w ciągu ostatniej dekady. Wiele prac badawczych poświęcono przyspieszeniu kinetyki rozkładu przez domieszkowanie katalityczne i mielenie kulowe . Aby wykorzystać całkowitą pojemność wodoru, związek pośredni LiH również musi zostać odwodorniony. Ze względu na wysoką stabilność termodynamiczną wymaga to temperatur przekraczających 400 ° C, co nie jest uważane za wykonalne do celów transportowych. Przyjmując LiH + Al jako produkt końcowy, zdolność magazynowania wodoru zmniejsza się do 7,96% wag. Innym problemem związanym z magazynowaniem wodoru jest zawracanie do LiAlH 4, który ze względu na swoją stosunkowo niską stabilność wymaga wyjątkowo wysokiego ciśnienia wodoru, przekraczającego 10000 barów. Rowerze jedyną reakcją R2 - to jest, przy użyciu Li 3 ALH 6 jako materiał wyjściowy - będzie przechowywał 5,6% wagowych wodoru w jednym etapie, w dwóch etapach (w porównaniu do NaAlH 4, która przechowuje w tej samej ilości wodoru). Jednak próby tego procesu do tej pory nie kończyły się sukcesem.
Inne tetrahydrydogliniany
Znanych jest wiele soli analogicznych do LAH. NaH, mogą być stosowane do wydajnego wytwarzania aluminium wodorek sodu (NaAlH 4 ) przez metatezę w THF:
- LiAlH 4 + NaH → NaAlH 4 + LiH
Wodorek potasowo-glinowy (KAlH 4 ) można wytwarzać podobnie w diglimie jako rozpuszczalniku:
- LiAlH 4 + KH → KAlH 4 + LiH
Odwrotność, tj. Wytwarzanie LAH z wodorku glinowo-sodowego lub wodorku glinowo-potasowego można osiągnąć poprzez reakcję z LiCl lub wodorkiem litu w eterze dietylowym lub THF :
- NaAlH 4 + LiCl → LiAlH 4 + NaCl
- KAlH 4 + LiCl → LiAlH 4 + KCl
„Alanian magnezu” (Mg (AlH 4 ) 2 ) powstaje podobnie przy użyciu MgBr 2 :
- 2 LiAlH 4 + MgBr 2 → Mg (AlH 4 ) 2 + 2 LiBr
Red-Al (lub SMEAH, NaAlH 2 (OC 2 H 4 OCH 3 ) 2 ) jest syntetyzowany w reakcji tetrawodnika glinowo-sodowego (NaAlH 4 ) i 2-metoksyetanolu :
Zobacz też
Bibliografia
Dalsza lektura
- Wiberg, E .; Amberger, E. (1971). Wodorki pierwiastków z grup głównych I-IV . Elsevier. ISBN 0-444-40807-X .
- Hajos, A. (1979). Złożone wodorki i powiązane czynniki redukujące w syntezie organicznej . Elsevier. ISBN 0-444-99791-1 .
- Lide, DR, wyd. (1997). Podręcznik chemii i fizyki . CRC Press. ISBN 0-8493-0478-4 .
- Carey, FA (2002). Chemia organiczna z centrum edukacyjnym online i CD-ROM z uczeniem się przez model . McGraw-Hill. ISBN 0-07-252170-8 .
- Andreasen, A. (2005). „Rozdział 5: Złożone Wodorki” (PDF) . Materiały do magazynowania wodoru ze szczególnym uwzględnieniem pierwiastków z grupy I-II . Krajowe Laboratorium Risø. ISBN 87-550-3498-5 . Zarchiwizowane od oryginalnego (PDF) w dniu 2012-08-19.
Zewnętrzne linki
- „Użycie LiAlH 4 ” . Synteza organiczna.
- „Tetrahydrydoglinian litu - Podsumowanie związku (CID 28112)” . PubChem.
- „Tetrahydrydoglinian litu” . WebBook . NIST.
- „Karta charakterystyki materiałów” . Uniwersytet Cornella. Zarchiwizowane od oryginału w dniu 8 marca 2006 r.
- „Centrum informacji o wodorkach” . Sandia National Laboratory. Zarchiwizowane od oryginału w dniu 7 maja 2005 r.
- „Reakcje na redukcję” (PDF) . Materiały dydaktyczne - 4 rok . Uniwersytet w Birmingham. Zarchiwizowane od oryginalnego (PDF) w dniu 23 maja 2016 r.