Acetylid - Acetylide
Acetylenku odnosi się do związków chemicznych o to wzorach chemicznych MC≡CH i MC≡CM, przy czym M jest metalem. Termin jest używany luźno i może odnosić się do podstawionych acetylenków o ogólnej strukturze RC≡CM (gdzie R oznacza organiczny łańcuch boczny ). Acetylidy są odczynnikami w syntezie organicznej . Acetyloid wapnia powszechnie nazywany węglikiem wapnia jest głównym związkiem handlowym.
Struktura i klejenie
Metali alkalicznych i metali ziem alkalicznych, acetylenki o wzorze ogólnym MC≡CM są podobne do soli fazy Zintl związki zawierające C,2−
2jony. Dowód na ten charakter jonowy można zobaczyć w szybkiej hydrolizie tych związków z wytworzeniem acetylenu i tlenków metali, istnieją również pewne dowody na rozpuszczalność C2−
2jony w ciekłym amoniaku. C2−
2jonowego zamkniętej powłoki stanu podstawowego z 1 Ď+
g, czyniąc ją izoelektroniczną z obojętną cząsteczką N 2 , co może zapewnić jej pewną stabilność.
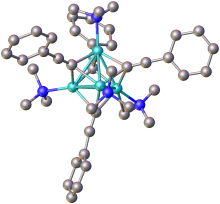
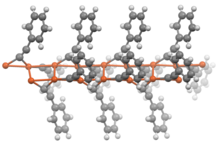
Analogiczne acetylenki wytworzone z innych metali, zwłaszcza metali przejściowych , wykazują charakter kowalencyjny i są niezmiennie związane z ich centrami metalowymi. Można to zaobserwować na ich ogólną odporność na wodę (takie jak acetylenek srebra , miedzi acetylenku ) i skrajnie różnych procesach chemicznych.
Acetylidy o wzorze ogólnym RC≡CM (gdzie R = H lub alkil) ogólnie wykazują podobne właściwości do ich podwójnie podstawionych analogów. W przypadku braku dodatkowych ligandów, acetylidki metali przyjmują struktury polimerowe, w których grupy acetylidkowe są ligandami mostkowymi .
Przygotowanie
Końcowe grupy alkinowe są słabe kwasy :
- RC≡CH + R″M ⇌ R″H + RC≡CM
W celu wytworzenia acetylenki z acetylenu i alkinów polega na zastosowaniu metaloorganicznych i nieorganicznych superbases w rozpuszczalnikach, które są mniej kwaśna niż złącze alkinu. We wczesnych badaniach stosowano ciekły amoniak , ale rozpuszczalniki eterowe są bardziej powszechne.
Amidek litu , LiHMDS lub odczynniki litoorganiczne , takie jak butylolit , są często używane do tworzenia acetylenków litu:
Acetyleny sodu lub potasu można wytwarzać z różnych odczynników nieorganicznych (takich jak amidek sodu ) lub z ich pierwiastków, często w temperaturze pokojowej i pod ciśnieniem atmosferycznym.
Acetylodek miedzi(I) można wytworzyć przepuszczając acetylen przez wodny roztwór chlorku miedzi(I) ze względu na niską równowagę rozpuszczalności . Podobnie, acetylenki srebra można otrzymać z azotanu srebra .
Węglik wapnia jest wytwarzany przez ogrzewanie węgla z wapnem ( tlenkiem wapnia ) w temperaturze około 2000 °C. Podobny proces stosuje się do produkcji węglika litu .
Reakcje
Acetylidy typu RC 2 M są szeroko stosowane w alkinylowaniu w chemii organicznej . Są to nukleofile, które dodają się do różnych elektrofilowych i nienasyconych substratów. Klasycznym zastosowaniem jest reakcja Favorskiego .
Przykładem jest sekwencja pokazana poniżej, propiolan etylu jest deprotonowany przez n- butylolit z wytworzeniem odpowiedniego acetylidku. Ten acetylen dodaje się do centrum karbonylowego cyklopentanonu . Obróbka hydrolityczna uwalnia alkohol alkinylowy.
Reakcje sprzęgające
Acetylidy są czasami produktami pośrednimi w reakcjach sprzęgania . Przykłady obejmują sprzęganie Sonogashira , sprzęgło Cadiot-Chodkiewicz , sprzęgło Glaser i sprzęgło Eglinton .
Zagrożenia
Niektóre acetylenki są notorycznie wybuchowe. Powstawanie acetylenków stwarza ryzyko przy operowaniu gazowym acetylenem w obecności metali takich jak rtęć , srebro czy miedź lub stopów o dużej zawartości ( mosiądz , brąz , lut srebrny ).
Zobacz też
- Etynylo
- Rodnik etynylowy
- Węgiel dwuatomowy (neutralny C 2 )
- Acetylenodiol

![{\ Displaystyle {\ ce {{HC\! {\ równoważny} \! CH} + {\ overset {butylolit} {BuLi}} -> [{\ ce {THF}}][-78 ^ {\ circ} \ce {C}}]{Li-\!{\equiv }\!-H}+BuH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ae261811e4519409e7516a7a6c4576ec44871845)
