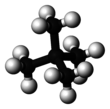
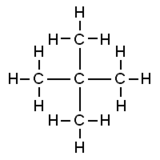
Neopentan - Neopentane

|
|||
|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
2,2-dimetylopropan |
|||
| Inne nazwy
Neopentan
Tetrametylometan |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| 1730722 | |||
| CZEBI | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.006.677 |
||
| Numer WE | |||
| 1850 | |||
| Siatka | neopentan | ||
|
Identyfikator klienta PubChem
|
|||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 5 H 12 | |||
| Masa cząsteczkowa | 72,151 g·mol -1 | ||
| Wygląd zewnętrzny | Bezbarwny gaz | ||
| Zapach | Bezwonny | ||
| Gęstość | 3,255 kg/m 3 (gaz, 9,5°C) 601,172 kg/m 3 (ciecz, 9,5°C) |
||
| Temperatura topnienia | -16,5 ° C (2,3 ° F; 256,6 K) | ||
| Temperatura wrzenia | 9,5 ° C (49,1 ° F; 282,6 K) | ||
| Ciśnienie pary | 146 kPa (przy 20 °C) | ||
|
Stała prawa Henry'ego ( k H ) |
4,7 nmol Pa -1 kg -1 | ||
| Termochemia | |||
|
Pojemność cieplna ( C )
|
121,07–120,57 JK -1 mol -1 | ||
|
Standardowa
entropia molowa ( S |
217 JK -1 mol -1 | ||
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-168,5–167,3 kJ mol -1 | ||
|
Standardowa entalpia
spalania (Δ c H ⦵ 298 ) |
−3,51506–−3,51314 MJ mol −1 | ||
| Zagrożenia | |||
|
Klasyfikacja UE (DSD) (nieaktualna)
|
|
||
| Zwroty R (nieaktualne) | R12 , R51/53 | ||
| Zwroty S (nieaktualne) | (S2) , S16 , S33 | ||
| NFPA 704 (ognisty diament) | |||
| Związki pokrewne | |||
|
Powiązane alkany
|
|||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
Neopentan , zwany także 2,2-dimetylopropanem , to alkan o podwójnym łańcuchu z pięcioma atomami węgla. Neopentan jest gazem palnym w temperaturze pokojowej i pod ciśnieniem, który może skraplać się w bardzo lotną ciecz w zimny dzień, w łaźni lodowej lub po sprężeniu do wyższego ciśnienia.
Neopentan jest najprostszym alkanem z czwartorzędowym węglem i ma achiralną symetrię tetraedryczną . Jest to jeden z trzech izomerów strukturalnych z o wzorze cząsteczkowym C 5 H 12 ( pentanów ), a dwa pozostałe istoty n -pentano i izopentan . Z tych trzech jako jedyny jest gazem w standardowych warunkach; pozostałe to płyny.
Nomenklatura
Tradycyjna nazwa neopentan była nadal zachowana w zaleceniach IUPAC z 1993 r. , ale nie jest już zalecana zgodnie z zaleceniami z 2013 r. Korzystne nazwa według IUPAC to nazwa systematyczna 2,2-dimetylopropan, a liczba podstawników są zbędne, ponieważ jest to tylko możliwe „dimetylopropan”.
Podstawnik neopentylowy , często symbolizowany przez „Np”, ma budowę Me 3 C–CH 2 – np. alkohol neopentylowy (Me 3 CCH 2 OH lub NpOH). Ponieważ Np symbolizuje również pierwiastek neptun (liczba atomowa 93), skrót ten należy stosować ostrożnie.
Używana jest również przestarzała nazwa tetrametylometan, zwłaszcza w starszych źródłach.
Właściwości fizyczne
Temperatura wrzenia i topnienia
Temperatura wrzenia neopentanu wynosi tylko 9,5 °C, znacznie mniej niż izopentanu (27,7 °C) i normalnego pentanu (36,0 °C). Dlatego neopentan jest gazem w temperaturze pokojowej i ciśnieniu atmosferycznym, podczas gdy pozostałe dwa izomery są (ledwo) cieczami.
Z drugiej strony temperatura topnienia neopentanu (-16,6 ° C) jest o 140 stopni wyższa niż izopentanu (-159,9 ° C) i 110 stopni wyższa niż n- pentanu (-129,8 ° C). Ta anomalia została przypisana lepszemu upakowaniu ciała stałego, co do którego zakłada się, że jest możliwe w przypadku tetraedrycznej cząsteczki neopentanu; ale to wyjaśnienie zostało zakwestionowane, ponieważ ma mniejszą gęstość niż pozostałe dwa izomery. Co więcej, jego entalpia topnienia jest niższa niż entalpie topnienia zarówno n- pentanu, jak i izopentanu, co wskazuje, że jego wysoka temperatura topnienia wynika z efektu entropii wynikającego z wyższej symetrii cząsteczkowej. Rzeczywiście, entropia fuzji neopentanu jest około czterokrotnie niższa niż n- pentanu i izopentanu.
1 H NMR
Ze względu na pełną tetraedryczną symetrię neopentanu wszystkie protony są chemicznie równoważne, co prowadzi do pojedynczego przesunięcia chemicznego NMR δ = 0,902 po rozpuszczeniu w tetrachlorku węgla . Pod tym względem neopentan jest podobny do swojego analogu silanowego , tetrametylosilanu , którego pojedyncze przesunięcie chemiczne zgodnie z konwencją wynosi zero.
Symetria cząsteczki neopentanu może zostać złamana, jeśli niektóre atomy wodoru zostaną zastąpione atomami deuteru . W szczególności, jeśli każda grupa metylowa ma inną liczbę podstawionych atomów (0, 1, 2 i 3), otrzymuje się cząsteczkę chiralną . Chiralność w tym przypadku wynika wyłącznie z rozkładu masy jego jąder, podczas gdy rozkład elektronów jest nadal zasadniczo achiralny.
Bibliografia
Zewnętrzne linki
- Linstrom, Peter J.; Mallard, William G. (red.); NIST Chemistry WebBook, NIST Standard Reference Database Number 69 , Narodowy Instytut Standardów i Technologii, Gaithersburg (MD), http://webbook.nist.gov
- Nomenklatura IUPAC Chemii Organicznej (wersja internetowa „ Niebieskiej Księgi ”)