Oxohalogenek - Oxohalide
Oksohalogenki cząsteczkowe ( oksyhalogenki ) to grupa związków chemicznych, w których zarówno atomy tlenu, jak i halogenu są połączone z innym pierwiastkiem chemicznym A w jednej cząsteczce . Mają one wzór ogólny AO m X, n , X = F , Cl , Br , I . Pierwiastek A może być głównym pierwiastkiem grupy, pierwiastkiem przejściowym lub aktynowcem . Termin oksohalogenek lub oksyhalogenek może również odnosić się do minerałów i innych substancji krystalicznych o tym samym ogólnym wzorze chemicznym, ale o strukturze jonowej .
Synteza
Oksohalogenki można postrzegać jako związki pośrednie między tlenkami i halogenkami . Istnieją trzy ogólne metody syntezy:
- Częściowe utlenianie halogenku: 2 PCl 3 + O 2 → 2 POCl 3 . W tym przykładzie stopień utlenienia wzrasta o dwa, a ładunek elektryczny pozostaje niezmieniony.
- Częściowe halogenowanie tlenku: 2 V 2 O 5 + 6 Cl 2 + 3 C → 4 VOCl 3 + 3 CO 2
- Zastępowanie tlenków: [CrO 4 ] 2− + 2 Cl - + 4 H + → CrO 2 Cl 2 + 4 H 2 O
Ponadto, różne oxohalides mogą być uzyskiwane w reakcji wymiany chlorowca, reakcja ta może prowadzić do powstawania mieszanych oxohalides jak POFCl 2 i CrC 2 fcl.
Nieruchomości
W odniesieniu do tlenku lub halogenku, dla danego stopnia utlenienia pierwiastka A, jeśli dwa atomy halogenu zastąpią jeden atom tlenu lub odwrotnie , całkowity ładunek na cząsteczce pozostaje niezmieniony, a liczba koordynacyjna atomu centralnego zmniejsza się o jeden . Na przykład, jak tlenochlorek fosforu , tlenochlorku fosforu 3 i pięciochlorek fosforu , PCL 5 są obojętne kowalencyjne związki fosforu w + 5 stopniu utlenienia . Jeśli atom tlenu jest po prostu zastąpiony atomem halogenu, ładunek wzrasta o +1, ale liczba koordynacyjna pozostaje niezmieniona. Ilustruje to reakcja mieszaniny soli chromianowej lub dwuchromianowej i chlorku potasu ze stężonym kwasem siarkowym .
- [Cr 2 O 7 ] 2− + 4 Cl - + 6 H + → 2 CrO 2 Cl 2 + 3 H 2 O
Chlorek chromylu wytwarza ma ładunek elektryczny i lotny kowalencyjnym cząsteczki, która może być oddestylowany z mieszaniny reakcyjnej.
Oksohalogenki pierwiastków o wysokich stopniach utlenienia są silnymi utleniaczami o sile utleniającej podobnej do odpowiedniego tlenku lub halogenku. Większość oksohalogenków łatwo ulega hydrolizie . Na przykład chlorek chromilu jest hydrolizowany do chromianu w odwrotnej kolejności reakcji syntezy, opisanej powyżej. Siłą napędową tej reakcji jest tworzenie wiązań AO, które są silniejsze niż wiązania A-Cl. Daje to korzystny wkład entalpii do zmiany energii swobodnej Gibbsa dla reakcji
Wiele oksohalogenków może działać jako kwasy Lewisa . Dzieje się tak zwłaszcza w przypadku oksohalogenków o numerze koordynacyjnym 3 lub 4, które przyjmując jedną lub więcej par elektronów z zasady Lewisa , stają się współrzędną 5 lub 6. Aniony oksohalogenkowe, takie jak [VOCl 4 ] 2−, można postrzegać jako kompleksy kwasowo-zasadowe oksohalogenku (VOCl 2 ) z większą liczbą jonów halogenkowych działających jako zasady Lewisa. Innym przykładem jest VOCl 2, który tworzy trygonalny kompleks bipiramidalny VOCl 2 (N (CH 3 ) 3 ) 2 z zasadą trimetyloaminy .
Szczegółowo przypisano widma wibracyjne wielu oksohalogenków. Dostarczają użytecznych informacji na temat względnej siły wiązania. Na przykład w CrO 2 F 2 drgania rozciągające Cr – O wynoszą przy 1006 cm –1 i 1016 cm –1, a drgania rozciągające Cr – F przy 727 cm – 1 i 789 cm –1 . Różnica jest zbyt duża, aby wynikać z różnych mas atomów O i F. Pokazuje raczej, że wiązanie Cr – O jest znacznie silniejsze niż wiązanie Cr – F. Wiązania M – O są ogólnie uważane za wiązania podwójne, co jest poparte pomiarami długości wiązań M – O. Oznacza to, że elementy A i O są ze sobą chemicznie związane wiązaniem σ i wiązaniem π.
Oksohalogenki pierwiastków na wysokich stopniach utlenienia są intensywnie zabarwione dzięki przejściom przenoszenia ładunku z liganda na metal (LMCT).
Główne elementy grupy
-
Grupa węglowa : węgiel tworzy oksohalogenki COX 2 , X = F , Br i bardzo toksyczny fosgen (X = Cl), który jest wytwarzany przemysłowo w katalizowanej węglem reakcji tlenku węgla z chlorem . Jest użytecznym odczynnikiem w chemii organicznej do tworzenia związków karbonylowych . Na przykład,
- COCl 2 + 2 ROH → CO (OR) 2 + 2 HCl
- Pnictogeny : Azot tworzy z azotem dwie serie oksohalogenków na stopniach utlenienia 3, NOX, X = F , Cl , Br i 5, NO 2 X, X = F , Cl. Powstają przez halogenowanie tlenków azotu. Należy zauważyć, że NO 2 F jest izoelektroniczny z jonem azotanowym , NO 3 - . Znane są tylko oksohalogenki fosforu (V).
-
Chalkogeny : Siarka tworzy oksohalogenki na stopniu utlenienia +4, takie jak chlorek tionylu , SOCl 2 i stopień utlenienia +6, takie jak fluorek sulfurylu , SO 2 F 2 , chlorek sulfurylu , SO 2 Cl 2 i tetrafluorek tionylu , SOF 4 . Wszystkie są łatwo hydrolizowane. Rzeczywiście, chlorek tionylu może być stosowany jako środek odwadniający, ponieważ cząsteczki wody są przekształcane w produkty gazowe, pozostawiając bezwodny stały chlorek.
- MgCl 2 · 6H 2 O + 6 SOCl 2 → MgCl 2 + 6 SO 2 + 12 HCl
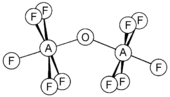
Selen i tellur tworzą podobne związki, a także gatunki z mostkami okso F 5 AOAF 5 (A = S, Se, Te). Są nieliniowe z kątem AOA 142,5, 142,4 i 145,5 ° odpowiednio dla S, Se i Te. Anion telluru [TeOF 5 ] - , znany jako teflat , jest dużym i raczej stabilnym anionem, przydatnym do tworzenia stabilnych soli z dużymi kationami.
- Halogeny : Halogeny tworzą różne oksofluorki o wzorach XO 2 F , XO 3 F i XOF 3 z X = Cl, Br i I. Znane są również IO 2 F 3 i IOF 5 .
- Gazy szlachetne : XeOF 4
Metale przejściowe i aktynowce
Wybór znanych oksohalogenków metali przejściowych przedstawiono poniżej, a bardziej szczegółowe listy są dostępne w literaturze. X oznacza różne halogenki, najczęściej F i Cl.
| Stan utlenienia | oksohalogenki |
|---|---|
| 3 | VOCl, VOBr, FeOCl |
| 4 | [TiOCl 4 ] 2− , Cl 3 TiOTiCl 3 , VOCl 2 , [VOCl 4 ] 2− |
| 5 | VOX 3 , VO 2 X, [CrOF 4 ] - , [CrOF 5 ] 2− , MnOCl 3 , TcOCl 3 , VOF 3 , VOCl 3 , NbOCl 3 |
| 6 | CrO 2 Cl 2 [CrO 3 Cl] - , Reox 4 REO 2 F 2 , OSOF 4 , CrO 2 F 2 , MoOCl 4 MoO 2 Cl 2 , WO 2 Cl 2 , WOCL 4 |
| 7 | MnO 3 Cl, ReOF 5 , ReO 2 F 3 , ReO 3 Cl, OsOF 5 |
| 8 | OsO 2 F 4 , OsO 3 F 2 |
Wysokie stopnie utlenienia metalu są podyktowane tym, że tlen jest silnym utleniaczem , podobnie jak fluor . Brom i jod są stosunkowo słabymi utleniaczami, dlatego znanych jest mniej oksobromków i oksojodków. Struktury związków o konfiguracji d 0 są przewidywane przez teorię VSEPR . Tak więc, CrO 2 Cl 2 jest czworościenne , OsO 3 F 2 jest trójkątny bipiramidalną , XeOF 4 ma ostrosłup o podstawie kwadratu i OSOF 5 jest ośmiościenny . Kompleks d 1 ReOCl 4 jest piramidą kwadratową.
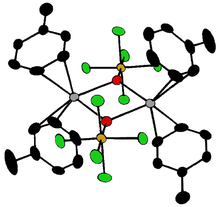
Związki [Ta 2 OX 10 ] 2− i [M 2 OCl 10 ] 4− (M = W, Ru, Os) mają dwie grupy MX 5 połączone mostkującym atomem tlenu. Każdy metal ma środowisko ośmiościenne. Niezwykłą liniową strukturę M-O-M można zracjonalizować pod względem teorii orbitali molekularnych , wskazując na obecność wiązania d π - p π między atomami metalu i tlenu. Mostki tlenowe występują w bardziej złożonych konfiguracjach, takich jak M (cp) 2 (OTeF 5 ) 2 (M = Ti, Zr, Hf, Mo lub W; cp = η 5 −C 5 H 5 ) lub [AgOTeF 5 - (C 6 H 5 CH 3 ) 2 ] 2 .
W szeregu aktynowców , związki uranylowe , takie jak UO 2 Cl 2 i [UO 2 Cl 4 ] 2−, są dobrze znane i zawierają liniowe ugrupowanie UO 2 . Podobne gatunki występują w przypadku neptunu i plutonu .
Minerały i związki jonowe
Oksochlorek bizmutu (BiOCl, bismoclite ) jest rzadkim przykładem mineralnego oksohalogenku. Struktura kryształu ma symetrię tetragonalną i można ją traktować jako składającą się z warstw jonów Cl - , Bi 3+ i O 2− , w kolejności Cl-Bi-O-Bi-Cl-Cl-Bi-O-Bi- Cl. Ta warstwowa struktura podobna do grafitu skutkuje stosunkowo niską twardością bismoklitu (w skali Mohsa 2–2,5) i większości innych minerałów oksohalogenkowych. Te inne minerały obejmują terlinguaite Hg 2 OCl, powstały w wyniku wietrzenia minerałów zawierających rtęć. Mendipit , Pb 3 O 2 Cl 2 , utworzony z pierwotnego złoża siarczku ołowiu w kilku etapach jest kolejnym przykładem wtórnego minerału oksohalogenkowego.
Pierwiastki żelazo , antymon , bizmut i lantan tworzą tlenochloryny o ogólnym wzorze MOCl. MOBr i MOI są również znane z Sb i Bi. Wiele ich struktur krystalicznych zostało określonych.
Zobacz też
Bibliografia
Bibliografia
- Greenwood, Norman N .; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8 .
- Housecroft, CE and Sharpe, AG Inorganic Chemistry , wyd. 2, Pearson Prentice-Hall 2005. ISBN 0-582-31080-6
- Shrivr, DF and Atkins, PW Inorganic Chemistry , 3rd edn. Oxford University Press, 1999. ISBN 0-19-850330-X
- Wells, AF (1962). Structural Inorganic Chemistry (3rd ed.). Oxford: Clarendon Press. pp. 384–392. ISBN 0-19-855125-8 . .