Porfiryna - Porphyrin
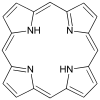
Porfiryny ( / p ɔːr F ər ɪ n / POR -fər w ), to grupa heterocykliczna makrocyklu związków organicznych , składa się z czterech zmodyfikowanych pirolo podjednostek połączonych na alfa atomów węgla poprzez metinowych mostków (= CH-). Macierzystą porfiryny jest porfina , rzadki związek chemiczny o znaczeniu wyłącznie teoretycznym. Podstawione porfiny nazywane są porfirynami. Mając łącznie 26 π-elektronów, z których 18 π-elektronów tworzy płaski, ciągły cykl, struktura pierścienia porfirynowego jest często określana jako aromatyczna . Jednym z rezultatów dużego sprzężonego układu jest to, że porfiryny zazwyczaj silnie absorbują w widzialnym obszarze widma elektromagnetycznego, tj. są głęboko zabarwione. Nazwa „porfiryna” wywodzi się od greckiego słowa πορφύρα ( porphyra ), oznaczającego purpurę .
Kompleksy metali pochodzące z porfiryn występują naturalnie. Jedną z najbardziej znanych rodzin kompleksów porfiryn jest hem , barwnik krwinek czerwonych , kofaktor białka hemoglobiny .
Kompleksy porfiryn
- Reprezentatywne porfiryny i pochodne
Porfina jest najprostszą porfiryną, rzadkim związkiem o znaczeniu teoretycznym.
Pochodne protoporfiryny IX są w przyrodzie powszechne, prekursora hemów .
Oktaetyloporfiryna (H 2 OEP) jest syntetycznym analogiem protoporfiryny IX. W przeciwieństwie do naturalnych ligandów porfirynowych, OEP 2− jest wysoce symetryczny.
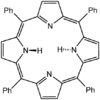
Tetrafenyloporfiryna (H 2 TPP) to kolejny syntetyczny analog protoporfiryny IX. W przeciwieństwie do naturalnych ligandów porfirynowych, TPP 2- jest wysoce symetryczny. Inną różnicą jest to, że jego centra metynowe są zajęte przez grupy fenylowe.
Uproszczony widok hemu , kompleksu protoporfiryny IX.
Porfiryny są sprzężonymi kwasami ligandów, które wiążą metale tworząc kompleksy . Jon metalu ma zwykle ładunek 2+ lub 3+. Schematyczne równanie dla tych syntez jest pokazane:
- H 2 porfiryna + [ML n ] 2+ → M(porfirynian)L n−4 + 4 L + 2 H + , gdzie M = jon metalu a L = ligand
Porfiryna bez jonu metalu w swojej wnęce jest wolną zasadą . Niektóre porfiryny zawierające żelazo nazywane są hemami. Białka zawierające hem lub hemoproteiny występują powszechnie w przyrodzie. Hemoglobina i mioglobina to dwa białka wiążące O 2 zawierające porfiryny żelaza. Hemoproteinami są również różne cytochromy .
Gatunki pokrewne
Benzoporfiryny jest porfiryna pierścień benzenowy skondensowany z jednym z zespołów pirolowymi. np. werteporfina jest pochodną benzoporfiryny.
Kilka innych heterocykli jest spokrewnionych z porfirynami. Należą corrins , chloryn , bakteriochlorofili i corphins . Chlory (2,3-dihydroporfiryny) są bardziej zredukowane, zawierają więcej wodoru niż porfiryny, tzn. jeden pirol został przekształcony w pirolinę . Ta struktura występuje w chlorofilach . Zastąpienie dwóch z czterech podjednostek pirolowych podjednostkami pirolinowymi powoduje powstanie bakteriochloryny (występującej w niektórych bakteriach fotosyntetycznych ) lub izobakteriochloryny, w zależności od względnych pozycji zredukowanych pierścieni. Niektóre pochodne porfiryny są zgodne z regułą Hückla , ale większość nie.
Naturalna formacja
Geoporfiryna, znana również jako petroporfiryna, jest porfiryną pochodzenia geologicznego. Mogą występować w ropie naftowej , łupkach bitumicznych , węglu lub skałach osadowych. Abelsonit jest prawdopodobnie jedynym minerałem geoporfirynowym, ponieważ porfiryny rzadko występują w izolacji i tworzą kryształy.
Synteza
Biosynteza
U niefotosyntetycznych eukariontów, takich jak zwierzęta, owady, grzyby i pierwotniaki , a także z grupy bakterii α-proteobakterii, etapem biosyntezy porfiryn jest tworzenie kwasu δ-aminolewulinowego (δ-ALA, 5-ALA lub dALA) w reakcji aminokwasu glicyny z sukcynylo-CoA z cyklu kwasu cytrynowego . W roślinach , algach , bakteriach (z wyjątkiem grupy α-proteobakterii) i archeonach wytwarzany jest z kwasu glutaminowego za pośrednictwem glutamylo-tRNA i glutaminian-1-semialdehydu . Enzymy uczestniczące w tym szlaku są glutamylo-tRNA , glutamylo-tRNA reduktazy i glutaminianu 1-semialdehyd 2,1 aminomutase . Ta ścieżka jest znana jako ścieżka C5 lub Beale.
Dwie cząsteczki dALA są następnie łączone przez syntazę porfobilinogenu w celu uzyskania porfobilinogenu (PBG), który zawiera pierścień pirolu. Cztery PBG są następnie łączone poprzez deaminację w hydroksymetylobilan (HMB), który jest hydrolizowany z wytworzeniem kolistego tetrapirolu uroporfirynogenu III . Ta cząsteczka przechodzi szereg dalszych modyfikacji. Półprodukty są używane u różnych gatunków do tworzenia określonych substancji, ale u ludzi główny produkt końcowy protoporfiryny IX łączy się z żelazem, tworząc hem. Pigmenty żółci są produktami rozpadu hemu.
Poniższy schemat podsumowuje biosyntezę porfiryn, z odniesieniami według numeru EC i bazy danych OMIM . Porfirię związane z niedoborem każdego enzymu jest również sposób:
Synteza laboratoryjna

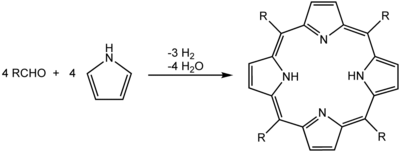
Jedną z najczęstszych syntez porfiryn jest reakcja Rothemunda , po raz pierwszy opisana w 1936 r., która jest również podstawą nowszych metod opisanych przez Adlera i Longo. Ogólny schemat to proces kondensacji i utleniania rozpoczynający się od pirolu i aldehydu .
Porfiryny izomeryczne
Pierwszy porfiryny syntetyczny izomer odnotował Emanuela Vogel i wsp w 1986. izomer [18] porphyrin- (2.0.2.0) została jako porficyny i centralny N 4 wgłębienie tworzy prostokątny kształt, jak pokazano na rysunku. Porficeny wykazały interesujące zachowanie fotofizyczne i znalazły wszechstronny związek w terapii fotodynamicznej . To zainspirowało Vogela i Sesslera do podjęcia wyzwania przygotowania [18]porfiryny-(2.1.0.1) i nazwania go Corrphycene lub Porphycerin . Trzecią porfirynę, czyli [18]porfirynę-(2.1.1.0), opisali Callot i Vogel-Sessler. Vogel i współpracownicy donieśli o udanej izolacji [18]porfiryny-(3.0.1.0) lub izoporficenu . Japoński uczony Furuta i polski uczony Latos-Grażyński niemal równocześnie zgłosili porfiryny N-Confused . Inwersja jednej z podjednostek pirolowych w pierścieniu makrocyklicznym spowodowała zwrócenie się do jednego z atomów azotu na zewnątrz rdzenia makrocyklu.
Aplikacje
Terapia fotodynamiczna
Porfiryny zostały ocenione w kontekście terapii fotodynamicznej (PDT), ponieważ silnie pochłaniają światło, które jest następnie przekształcane w energię i ciepło w oświetlonych obszarach. Technika ta została zastosowana w zwyrodnieniu plamki żółtej przy użyciu werteporfiny .
PDT jest uważane za nieinwazyjne leczenie raka, polegające na interakcji światła o określonej częstotliwości, fotouczulacza i tlenu. Ta interakcja powoduje powstanie wysoce reaktywnych form tlenu (ROS), zwykle tlenu singletowego, a także anionu ponadtlenkowego, wolnego rodnika hydroksylowego lub nadtlenku wodoru. Te wysoko reaktywne formy tlenu reagują z podatnymi komórkowymi biocząsteczkami organicznymi, takimi jak; lipidy, aminokwasy aromatyczne i zasady heterocykliczne kwasów nukleinowych, w celu wytworzenia rodników oksydacyjnych, które uszkadzają komórkę, prawdopodobnie wywołując apoptozę lub nawet martwicę.
Geochemia organiczna
Dziedzina geochemii organicznej wywodzi się z izolacji porfiryn z ropy naftowej. To odkrycie pomogło ustalić biologiczne pochodzenie ropy naftowej. Ropa naftowa jest czasami "odciskana palcami" poprzez analizę śladowych ilości porfiryn niklu i wanadylu .
Toksykologia
Biosynteza hemu jest wykorzystywana jako biomarker w badaniach toksykologii środowiskowej. Podczas gdy nadmierna produkcja porfiryn wskazuje na ekspozycję na chloroorganiczne związki , ołów hamuje enzym dehydratazę ALA .
Potencjalne aplikacje
Kataliza biomimetyczna
Chociaż nie są one skomercjalizowane, kompleksy metaloporfiryn są szeroko badane jako katalizatory utleniania związków organicznych. Szczególnie popularne w takich badaniach laboratoryjnych są kompleksy mezo - tetrafenyloporfiryny i oktaetyloporfiryny . Kompleksy z Mn, Fe i Co katalizują różne reakcje potencjalnie interesujące w syntezie organicznej . Niektóre kompleksy naśladują działanie różnych enzymów hemu , takich jak cytochrom P450 , peroksydaza ligninowa . Metaloporfiryny są również badane jako katalizatory rozszczepiania wody w celu wytwarzania wodoru cząsteczkowego i tlenu do ogniw paliwowych.
Elektronika molekularna i czujniki
Związki na bazie porfiryny są przedmiotem zainteresowania jako możliwe komponenty elektroniki molekularnej i fotoniki. Syntetyczne barwniki porfirynowe zostały włączone do prototypowych ogniw słonecznych uczulanych barwnikiem .
Metaloporfiryny badano jako czujniki.
Ftalocyjaniny , które są strukturalnie spokrewnione z porfirynami, są stosowane w handlu jako barwniki i katalizatory, ale porfiryny nie.
Chemia supramolekularna


Porfiryny są często wykorzystywane do budowy struktur w chemii supramolekularnej . Systemy te wykorzystują kwasowość Lewisa metalu, zwykle cynku. Przykład kompleksu gość-gospodarz, który został zbudowany z makrocyklu składającego się z czterech porfiryn. Porfiryna zasadowa bez gościa jest związana z centrum przez koordynację z jej czteropirydynowymi podstawnikami.
Teoretyczne zainteresowanie aromatycznością
Makrocykle porfirynoidowe mogą wykazywać zmienną aromatyczność. Porfiryną aromatyczną Hückla jest porficen. Znane są makrocykle antyaromatyczne , aromatyczne Mobiusa i niearomatyczne porfirynoidowe.
Zobacz też
- Choroba związana z porfiryną : porfiria
- Porfiryna skoordynowana z żelazem: hem
- Grupa enzymów zawierająca hem: cytochrom P450
- Porfiryna skoordynowana z magnezem: chlorofil
- Krótsze o jeden węgiel analogi: korole , w tym witamina B 12 , która jest skoordynowana z kobaltem
- Corphins, wysoce zredukowana porfiryna skoordynowana z niklem, która wiąże miejsce aktywne kofaktora F430 w reduktazie metylokoenzymu M (MCR)
- Porfiryny podstawione azotem: ftalocyjanina
Galeria
Odczyt UV-vis dla mezo- tetrafenyloporfiryny