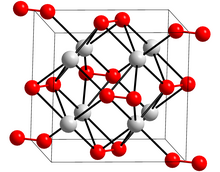
Nadtlenek potasu - Potassium peroxide

|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Nadtlenek potasu
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.037.339 |
| Numer WE | |
|
PubChem CID
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| K 2 O 2 | |
| Masa cząsteczkowa | 110,196 g / mol |
| Wygląd | żółte bezpostaciowe ciało stałe |
| Temperatura topnienia | 490 ° C (914 ° F, 763 K) |
| reaguje z wodą | |
| Struktura | |
| Orthorombic | |
| Cmca, OS16 | |
| Termochemia | |
|
Entropia trzonowa standardowa ( S |
113 J · mol −1 · K −1 |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
−496 kJ · mol −1 |
| Zagrożenia | |
| NFPA 704 (ognisty diament) | |
| Związki pokrewne | |
|
Inne aniony
|
Tlenek potasu Ponadtlenek potasu Chlorek potasu |
|
Inne kationy
|
Nadtlenek litu Nadtlenek sodu |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Nadtlenek potasu jest związkiem nieorganicznym o wzorze cząsteczkowym K 2 O 2 . Powstaje w wyniku reakcji potasu z tlenem zawartym w powietrzu wraz z tlenkiem potasu (K 2 O) i ponadtlenkiem potasu (KO 2 ).
Nadtlenek potasu reaguje z wodą, tworząc wodorotlenek potasu i tlen :
Bibliografia
| Ten artykuł związany ze związkami nieorganicznymi jest niedopałkiem . Możesz pomóc Wikipedii, rozbudowując ją . |