Nadtlenek potasu - Potassium superoxide
|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Dwutlenek potasu
|
|
| Inne nazwy
Nadtlenek potasu
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100,031,574 |
| Numer WE | |
|
Identyfikator klienta PubChem
|
|
| Numer RTECS | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| K O 2 | |
| Masa cząsteczkowa | 71,096 g·mol -1 |
| Wygląd zewnętrzny | żółte ciało stałe |
| Gęstość | 2,14 g / cm 3 , stałe |
| Temperatura topnienia | 560 ° C (1040 ° F; 833 K) (rozkłada się) |
| Hydroliza | |
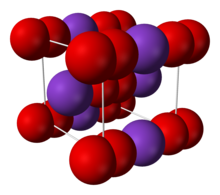
| Struktura | |
| sześcienny skoncentrowany na ciele ( O− 2) |
|
| Termochemia | |
|
Standardowa
entropia molowa ( S |
117 J·mol -1 ·K -1 |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-283 kJ·mol -1 |
| Zagrożenia | |
| Główne zagrożenia | żrące, utleniające |
| Zwroty R (nieaktualne) | 8-14-34 |
| Zwroty S (nieaktualne) | 17-27-36/37/39 |
| NFPA 704 (ognisty diament) | |
| Związki pokrewne | |
|
Inne aniony
|
Tlenek potasu Nadtlenek potasu |
|
Inne kationy
|
Nadtlenek litu Nadtlenek sodu Nadtlenek rubidu |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Nadtlenek potasu jest związkiem nieorganicznym o wzorze KO 2 . Jest to żółte, paramagnetyczne ciało stałe, które rozkłada się w wilgotnym powietrzu. Jest to rzadki przykład stabilnej soli anionu ponadtlenkowego . Nadtlenek potasu jest używany jako CO
2płuczka, H
2O osuszacz i O
2generator w rebreatherach , statkach kosmicznych , łodziach podwodnych i systemach podtrzymywania życia skafandrów kosmicznych .
Produkcja i reakcje
Nadtlenek potasu jest wytwarzany przez spalanie stopionego potasu w atmosferze tlenu .
- K + O
2 → KO
2
Sól składa się z K+
i O−
2jony połączone wiązaniem jonowym. Odległość O-O wynosi 1,28 Å.
Reaktywność
Nadtlenek potasu jest silnym utleniaczem , zdolnym do przekształcania tlenków w nadtlenki lub tlen cząsteczkowy . Hydroliza daje gazowy tlen, nadtlenek wodoru i wodorotlenek potasu :
- 2 KO
2 + 2 godz
2O → 2 KOH + H
2O
2+ O
2
Pochłaniający dwutlenek węgla wodorotlenek potasu (KOH) wytwarza węglany:
- 2 KOH + CO
2 → K 2 CO 3 + H 2 O - KOH + CO
2 → KHCO 3
Połączenie tych dwóch reakcji daje:
- 4 KO
2 + 2 CO
2 → 2 K 2 CO 3 + 3 O
2 - 4 KO
2 + 4 CO
2 + 2 H 2 O → 4 KHCO 3 + 3 O
2
Nadtlenek potasu znajduje jedynie niszowe zastosowania jako odczynnik laboratoryjny. Ponieważ reaguje z wodą, KO
2jest często badany w rozpuszczalnikach organicznych. Ponieważ sól jest słabo rozpuszczalna w rozpuszczalnikach niepolarnych, zazwyczaj stosuje się etery koronowe . Tetraetyloamoniowy sól jest również znane. Reprezentatywne reakcje tych soli obejmują stosowanie ponadtlenku jako nukleofila , np. w przekształcaniu bromków alkilu w alkohole i chlorków acylu w nadtlenki diacylu .
Aplikacje
Rosyjska Agencja Kosmiczna miał powodzenia przy użyciu nadtlenku potasu w chemicznych generatorach tlenu dla swoich skafandrach i Sojuz statku kosmicznego . KO
2została również zastosowana w kanistrach o rebreatherów do gaszenia pożarów i ratownictwa górniczego pracy, ale nie ograniczone zastosowanie w butlą rebreatherów niebezpiecznie ze względu na jej wybuchową reakcję z wodą.
KO
2reaguje z CO
2 w następującej reakcji:
- 4 KO 2 (s) + 2 CO 2 (g) → 2K 2 CO 3 (s) + 3O 2 (g)
Teoretycznie 1 kg KO
2pochłania 0,310 kg CO
2uwalniając 0,338 kg O
2. Jeden mol KO
2pochłania 0,5 mola CO
2ale uwalnia tylko 0,75 mola cząsteczek gazowego tlenu ( O 2 ).
Zagrożenia
Nadtlenek potasu jest silnym utleniaczem i może powodować wybuchowe reakcje w połączeniu z różnymi substancjami i związkami, w tym wodą, kwasami, substancjami organicznymi lub sproszkowanym grafitem. Nawet suchy ponadtlenek może wytworzyć wrażliwy na uderzenia związek wybuchowy w połączeniu z olejami organicznymi, takimi jak nafta. W 1999 roku w Oak Ridge National Laboratory oczyszczanie tlenków potasu z wycieku metalu NaK spowodowało eksplozję wrażliwą na uderzenia po nasyceniu olejem mineralnym.
Bibliografia
- ^ B Zumdahl Steven S. (2009). Zasady chemiczne (6 wyd.). Houghtona Mifflina. P. A22. Numer ISBN 978-0-618-94690-7.
- ^ Hayyan M.; mgr Haszim; AlNashef IM (2016). „Jon ponadtlenkowy: wytwarzanie i implikacje chemiczne” . Chem. ks . 116 (5): 3029–3085. doi : 10.1021/acs.chemrev.5b00407 . PMID 26875845 .CS1 maint: używa parametru autorów ( link )
- ^ Jakob, Harald; Leininger, Stefan; Lehmanna, Thomasa; Jacobi, Sylwia; Gutewort, Sven (2007). „Związki Peroxo, nieorganiczne”. Encyklopedia Chemii Przemysłowej Ullmanna . Wiley-VCH. doi : 10.1002/14356007.a19_177.pub2 . Numer ISBN 978-3527306732.
- ^ Abrahams, SC; Kalnajs, J. (1955). „Struktura krystaliczna nadtlenku α-potasu” . Acta Crystallographica . 8 (8): 503–6. doi : 10.1107/S0365110X55001540 .
- ^ Kumar De Anil (2007). Księga Tekstowa Chemii Nieorganicznej . New Age International. P. 247. Numer ISBN 978-8122413847.
- ^ Johnson, Roy A.; Adrio, Javier; Ribagorda, Maria (2001). „Nadtlenek potasu”. Encyklopedia odczynników do syntezy organicznej e-EROS . Wileya. doi : 10.1002/047084289X.rp250.pub2 . Numer ISBN 0471936235.
-
^ Aerojet Nuclear Company (1975). „Analiza zagrożeń wybuchowych w roztworze eutektycznym NaK i KO
2Narodowe Laboratorium Inżynieryjne Idaho. - ^ „Dochodzenie w sprawie wypadku Y-12 NaK” . Departament Energii Stanów Zjednoczonych. Luty 2000. Zarchiwizowane z oryginału w dniu 28.05.2010.

