1-Propanol - 1-Propanol

|
|

|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
Propan-1-ol |
|
| Inne nazwy | |
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| 3DMet | |
| 1098242 | |
| CZEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| Karta informacyjna ECHA |
100.000.679 |
| Numer WE | |
| 25616 | |
| KEGG | |
| Siatka | 1-Propanol |
|
Identyfikator klienta PubChem
|
|
| Numer RTECS | |
| UNII | |
| Numer ONZ | 1274 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 3 H 8 O | |
| Masa cząsteczkowa | 60,096 g·mol -1 |
| Wygląd zewnętrzny | Bezbarwna ciecz |
| Zapach | łagodny, przypominający alkohol |
| Gęstość | 0,803 g/ml |
| Temperatura topnienia | -126°C; -195°F; 147 tys |
| Temperatura wrzenia | 97 do 98 °C; 206 do 208 ° F; 370 do 371 tys |
| mieszalny | |
| log P | 0,329 |
| Ciśnienie pary | 1,99 kPa (przy 20 °C) |
| Kwasowość (p K a ) | 16 |
| Zasadowość (p K b ) | -2 |
| -45,176 x 10 -6 cm 3 / mol | |
|
Współczynnik załamania ( n D )
|
1,387 |
| Lepkość | 1,959 mPa·s (przy 25 °C) |
| 1,68 D | |
| Termochemia | |
|
Pojemność cieplna ( C )
|
143,96 J/(K·mol) |
|
Standardowa
entropia molowa ( S |
192,8 J/(K·mol) |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-302,79…-302,29 kJ/mol |
|
Standardowa entalpia
spalania (Δ c H ⦵ 298 ) |
-2,02156…-2,02106 MJ/mol |
| Farmakologia | |
| D08AX03 ( KTO ) | |
| Zagrożenia | |
| Piktogramy GHS |
  
|
| Hasło ostrzegawcze GHS | Zagrożenie |
| H225 , H318 , H336 | |
| P210 , P261 , P280 , P305+351+338 | |
| NFPA 704 (ognisty diament) | |
| Temperatura zapłonu | 22 ° C (72 ° F; 295 K) |
| 371 ° C (700 ° F; 644 K) | |
| Granice wybuchowości | 2,2–13,7% |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
2800 mg/kg (królik, doustnie) 6800 mg/kg (mysz, doustnie) 1870 mg/kg (szczur, doustnie) |
| NIOSH (limity ekspozycji dla zdrowia w USA): | |
|
PEL (dopuszczalne)
|
TWA 200 ppm (500 mg/m 3 ) |
|
REL (zalecane)
|
TWA 200 ppm (500 mg/m 3 ) ST 250 ppm (625 mg/m 3 ) [skóra] |
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
800 ppm |
| Związki pokrewne | |
|
Związki pokrewne
|
Propan Alkohol izopropylowy Propanamina Etanol Butanol |
| Strona z danymi uzupełniającymi | |
|
Współczynnik załamania ( n ), stała dielektryczna (ε r ) itp. |
|
|
Dane termodynamiczne |
Zachowanie fazowe ciało stałe-ciecz-gaz |
| UV , IR , NMR , MS | |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
1-Propanol jest pierwszorzędowym alkoholem o wzorze CH
3CH
2CH
2OH i czasami przedstawiane jako PrOH lub n- PrOH . Jest to ciecz bezbarwna i izomer z 2-propanolu . Powstaje naturalnie w niewielkich ilościach podczas wielu procesów fermentacyjnych i jest stosowany jako rozpuszczalnik w przemyśle farmaceutycznym, głównie do żywic i estrów celulozy, a czasami jako środek dezynfekujący .
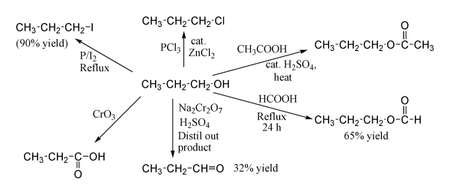
Właściwości chemiczne
1-Propanol wykazuje normalne reakcje alkoholu pierwszorzędowego . W ten sposób można go przekształcić w halogenki alkilowe ; np. czerwony fosfor i jod dają jodek n-propylu z wydajnością 80%, natomiast PCl
3z katalitycznym ZnCl
2daje chlorek n-propylu . Reakcja z kwasem octowym w obecności H
2WIĘC
4katalizator w warunkach estryfikacji Fischera daje octan propylu , podczas gdy ogrzewanie pod chłodnicą zwrotną propanolu przez noc z samym kwasem mrówkowym może wytworzyć mrówczan propylu z wydajnością 65%. Utlenianie 1-propanolu Na
2Cr
2O
7i H
2WIĘC
4daje tylko 36% wydajność aldehydu propionowego , dlatego dla tego typu reakcji zalecane są metody o wyższej wydajności z zastosowaniem PCC lub utleniania Swerna . Utlenianie kwasem chromowym daje kwas propionowy .
Przygotowanie
1-propanol jest wytwarzany przez katalityczne uwodornienie z aldehydu propionowego . Propionowy jest wytwarzany poprzez proces okso, przez hydroformylowanie z etylenu przy użyciu tlenku węgla i wodoru w obecności katalizatora, takiego jak octacarbonyl kobaltowego lub rodowego kompleksu.
- h
2C=CH
2 + CO + H
2 → CH
3CH
2CH=O
- CH
3CH
2CH=O + H
2 → CH
3CH
2CH
2OH
Tradycyjny laboratoryjny preparat 1-propanolu polega na poddaniu jodku n- propylu wilgotnego Ag
2O .
Bezpieczeństwo
Uważa się, że 1-Propanol jest podobny do etanolu pod względem wpływu na organizm ludzki, ale jest 2–4 razy silniejszy. Doustna LD 50 u szczurów wynosi 1870 mg / kg (w porównaniu do 7060 mg / kg etanolu). Jest metabolizowany do kwasu propionowego . Efekty obejmują zatrucie alkoholowe i kwasicę metaboliczną z dużą luką anionową . Do 2011 r. zgłoszono tylko jeden przypadek śmiertelnego zatrucia 1-propanolem.
Propanol jako paliwo
1-propanol ma wysoką liczbę oktanową i nadaje się do stosowania jako paliwo silnikowe . Jednak propanol jest zbyt drogi, aby można go było stosować jako paliwo silnikowe. Liczby oktanowej (RON) propanol 118 oraz wskaźnik przeciwstukowy (AKI) wynosi 108.
Bibliografia
Dalsza lektura
- Furniss, BS; Hannaford, AJ; Smith, PWG; Tatchell, AR (1989), Podręcznik Vogla Praktycznej Chemii Organicznej (5th ed.), Harlow: Longman, ISBN 0-582-46236-3
- Lide DR, wyd. (2006). CRC Handbook of Chemistry and Physics (wyd. 87.). TF-CRC. Numer ISBN 0849304873.
- O'Neil MJ, wyd. (2006). Indeks Merck: Encyklopedia chemikaliów, leków i biologii (wyd. 14). Merck. Numer ISBN 091191000X.
- Perkin WH, Kipping FS (1922). Chemia organiczna . Londyn: W. & R. Chambers. Numer ISBN 0080223540.