Tlenek srebra - Silver oxide
|
|

|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Tlenek srebra(I)
|
|
| Inne nazwy
Srebrna rdza, tlenek srebrzysty, tlenek srebra
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.039.946 |
| Numer WE | |
| Siatka | srebro + tlenek |
|
Identyfikator klienta PubChem
|
|
| Numer RTECS | |
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| Ag 2 O | |
| Masa cząsteczkowa | 231.735 g·mol -1 |
| Wygląd zewnętrzny | Czarne/brązowe kryształy sześcienne |
| Zapach | Bezwonny |
| Gęstość | 7,14 g / cm 3 |
| Temperatura topnienia | 300 °C (572 °F; 573 K) rozkłada się od ≥200 °C |
| 0,013 g/L (20°C) 0,025 g/L (25°C) 0,053 g/L (80°C) |
|
|
Iloczyn rozpuszczalności ( K sp ) AgOH
|
1,52·10 -8 (20 °C) |
| Rozpuszczalność | Rozpuszczalny w kwasie , zasada Nierozpuszczalny w etanolu |
| -134,0 x 10 -6 cm 3 / mol | |
| Struktura | |
| Sześcienny | |
| Pn 3 m, 224 | |
| Termochemia | |
|
Pojemność cieplna ( C )
|
65,9 J/mol·K |
|
Standardowa
entropia molowa ( S |
122 J/mol·K |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
−31 kJ/mol |
|
Energia swobodna Gibbsa (Δ f G ˚)
|
-11,3 kJ/mol |
| Zagrożenia | |
| Piktogramy GHS |
 
|
| Hasło ostrzegawcze GHS | Zagrożenie |
| H272 , H315 , H319 , H335 | |
| P220 , P261 , P305+351+338 | |
| NFPA 704 (ognisty diament) | |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
2,82 g/kg (szczury, doustnie) |
| Związki pokrewne | |
|
Związki pokrewne
|
Tlenek srebra(I,III) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Tlenek srebra(I) to związek chemiczny o wzorze Ag 2 O. Jest to drobny czarny lub ciemnobrązowy proszek, który jest używany do wytwarzania innych związków srebra .
Przygotowanie

Tlenek srebra można otrzymać przez połączenie wodnych roztworów azotanu srebra i wodorotlenku alkalicznego . Ta reakcja nie daje znacznych ilości wodorotlenku srebra ze względu na korzystną energetykę dla następującej reakcji:
- 2 AgOH → Ag 2 O + H 2 O ( p K = 2,875)
Z odpowiednio kontrolowanych warunkach, reakcja ta może być wykorzystana do przygotowania Ag 2 O w proszku o właściwościach odpowiednich dla różnych zastosowań, w tym jako drobnoziarnisty wypełniacz pasty przewodzącej.
Struktura i właściwości
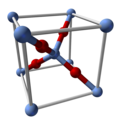
Ag 2 O charakteryzuje się liniowymi, dwukoordynacyjnymi centrami Ag połączonymi tetraedrycznymi tlenkami. Jest izostrukturalna z Cu 2 O . „Rozpuszcza się” w rozpuszczalnikach, które go degradują. Jest słabo rozpuszczalny w wodzie dzięki powstawaniu jonu Ag(OH)−
2i ewentualnie pokrewne produkty hydrolizy. Jest rozpuszczalny w roztworze amoniaku , tworząc aktywny związek odczynnika Tollensa . Zawiesinę Ag 2 O łatwo atakowane przez kwasy :
- Ag 2 O + 2 HX → 2 AgX + H 2 O
w którym HX = HF , HCI , HBr , HI lub CF 3 COOH . Będzie również reagował z roztworami chlorków alkalicznych, aby wytrącić chlorek srebra , pozostawiając roztwór odpowiedniego wodorotlenku alkalicznego.
Podobnie jak wiele związków srebra, tlenek srebra jest światłoczuły. Rozkłada się również w temperaturach powyżej 280 °C.
Aplikacje
Ten tlenek jest używany w akumulatorach ze tlenku srebra . W chemii organicznej tlenek srebra jest używany jako łagodny środek utleniający . Na przykład utlenia aldehydy do kwasów karboksylowych . Takie reakcje często działają najlepiej, gdy tlenek srebra jest wytwarzany in situ z azotanu srebra i wodorotlenku alkalicznego .
Bibliografia
Zewnętrzne linki
- Wyżarzanie tlenku srebra – Eksperyment demonstracyjny: Instrukcja i wideo

