Naftalenek sodu - Sodium naphthalenide
|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
Naftalenek sodu |
|
|
Systematyczna nazwa IUPAC
Naftalen-1-jaz sodowy |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.020.420 |
| Numer WE | |
|
PubChem CID
|
|
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 10 H 8 Na | |
| Masa cząsteczkowa | 151,164 g · mol −1 |
| Związki pokrewne | |
|
Inne aniony
|
Cyklopentadienidek sodu |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
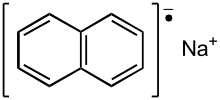
Naftalenek sodu , znany również jako naftalorek sodu , jest solą organiczną o wzorze chemicznym Na + C 10 H 8 - . W laboratorium badawczym jest stosowany jako reduktor w syntezie chemii organicznej, metaloorganicznej i nieorganicznej. Zwykle nie jest izolowany jako ciało stałe, ale przygotowywany na świeżo przed użyciem.
Przygotowanie i właściwości
Naftalenidy metali alkalicznych wytwarza się przez mieszanie metalu z naftalenem w rozpuszczalniku eterowym , zwykle w postaci tetrahydrofuranu lub dimetoksyetanu . Powstała sól jest ciemnozielona. Anion jest rodnikiem, dającym silny sygnał EPR w pobliżu g = 2,0, z potencjałem redukcji bliskim -2,5 V względem NHE . Jego ciemnozielony kolor wynika z absorpcji przy 463,735 nm.
Kilka solwatów naftalenku sodu scharakteryzowano za pomocą krystalografii rentgenowskiej .
Anion jest silnie zasadowy, a typowa ścieżka degradacji obejmuje reakcję z wodą i pokrewnymi źródłami protonowymi, takimi jak alkohole. Te reakcje dają dihydronaftalen :
- 2 NaC 10 H 8 + 2 H 2 O → C 10 H 10 + C 10 H 8 + 2 NaOH
Powiązane odczynniki
W przypadku niektórych operacji syntetycznych naftalenek sodu jest nadmiernie redukowany (zbyt ujemny) lub zbyt nierozpuszczalny. W takich przypadkach wybiera się alternatywne reduktory.
- Acenaftalenek sodu jest łagodniejszy o około 0,75 V, co odzwierciedla łagodniejszy potencjał redukcyjny wielopierścieniowych związków aromatycznych.
- Litowo bifenyl jest THF rozpuszczalnych gatunków związanych naphthalenide litu wyjątkiem tego, że jest słabszym ligandem.
- 1-metylonaftalenek sodu jest bardziej rozpuszczalny niż naftalenek sodu, co jest przydatne do redukcji w niskich temperaturach.
- Piren sodowy.

