Standardowa entalpia tworzenia - Standard enthalpy of formation
Średnia entalpia tworzenia lub standardową ciepło tworzenia związku jest zmiana entalpii podczas formowania 1 mol substancji z jego składowych elementów , wszystkich substancji w ich standardowych stanów . Średnia wartość ciśnienia p ⦵ = 10 5 Pa (= 100 kPa = 1 bar ) jest zalecane przez IUPAC , ale przed 1.982 wartości 1,00 atm (101,325 kPa) była używana. Nie ma standardowej temperatury. Jego symbolem jest Δ f H ⦵ . Indeks górny Plimsoll na tym symbolu wskazuje, że proces zaszedł w standardowych warunkach w określonej temperaturze (zwykle 25 °C lub 298,15 K). Standardowe stany są następujące:
- Dla gazu: stan hipotetyczny, który miałby przy założeniu, że jest zgodny z równaniem gazu doskonałego przy ciśnieniu 1 bara
- Dla gazowej lub stałej substancji rozpuszczonej obecnej w rozcieńczonym idealnym roztworze : hipotetyczny stan stężenia substancji rozpuszczonej dokładnie jednego mola na litr (1 M ) pod ciśnieniem 1 bara ekstrapolowany z nieskończonego rozcieńczenia
- Dla czystej substancji lub rozpuszczalnika w stanie skondensowanym (ciecz lub ciało stałe): stanem standardowym jest czysta ciecz lub ciało stałe pod ciśnieniem 1 bara
- Dla elementu: forma, w której element jest najbardziej stabilny pod ciśnieniem 1 bara. Jedynym wyjątkiem jest fosfor , dla którego najbardziej stabilną formą przy 1 bar jest fosfor czarny , ale fosfor biały jest wybrany jako standardowy stan odniesienia dla zerowej entalpii tworzenia.
Na przykład standardowa entalpia tworzenia dwutlenku węgla byłaby entalpią następującej reakcji w powyższych warunkach:
- C(s, grafit ) + O 2 (g) → CO 2 (g)
Wszystkie elementy są zapisane w stanach standardowych i powstaje jeden mol produktu. Dotyczy to wszystkich entalpii formacji.
Standardowa entalpia tworzenia jest mierzona w jednostkach energii na ilość substancji, zwykle wyrażoną w kilodżulach na mol (kJ mol- 1 ), ale także w kilokaloriach na mol , dżulach na mol lub kilokaloriach na gram (dowolna kombinacja tych jednostek zgodna zgodnie z wytycznymi dotyczącymi energii na masę lub ilości).
Wszystkie pierwiastki w ich stanach standardowych ( gaz tlen , węgiel stały w postaci grafitu , itp.) mają standardową entalpię tworzenia zerową, ponieważ w ich powstawaniu nie zachodzi żadna zmiana.
Reakcja tworzenia jest procesem o stałym ciśnieniu i stałej temperaturze. Ponieważ ciśnienie standardowej reakcji tworzenia jest ustalone na 1 bar, standardowa entalpia tworzenia lub ciepło reakcji jest funkcją temperatury. Dla celów tabelarycznych wszystkie standardowe entalpie tworzenia są podane w jednej temperaturze: 298 K, reprezentowane przez symbol Δ f H⦵
298 tys.
Prawo Hessa
W przypadku wielu substancji reakcję tworzenia można traktować jako sumę szeregu prostszych reakcji, rzeczywistych lub fikcyjnych. Entalpia reakcji może być następnie analizowane przez zastosowanie Prawo Hessa , który stanowi, że suma zmian entalpii dla szeregu poszczególnych etapów reakcji jest równa zmianie entalpii ogólnej reakcji. Jest to prawdą, ponieważ entalpia jest funkcją stanu , której wartość dla całego procesu zależy tylko od stanów początkowych i końcowych, a nie od stanów pośrednich. Przykłady podano w poniższych sekcjach.
Związki jonowe: cykl Borna-Habera
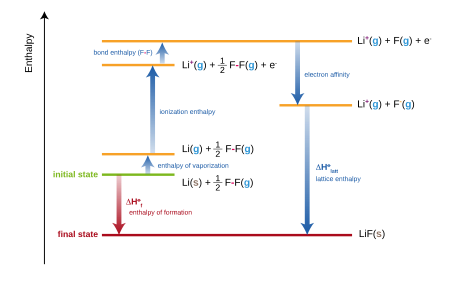
W przypadku związków jonowych standardowa entalpia tworzenia jest równoważna sumie kilku terminów zawartych w cyklu Borna-Habera . Na przykład tworzenie fluorku litu ,
- Li(s) + 1 ⁄ 2 F 2 (g) → LiF(s)
można traktować jako sumę kilku kroków, każdy z własną entalpią (lub energią, w przybliżeniu):
- Średnia entalpia rozpylanie (lub sublimację ) stałego litu.
- Pierwszy energia jonizacji gazowego litu.
- Standardowa entalpia atomizacji (lub energia wiązania) gazowego fluoru.
- Powinowactwo elektronów atomu fluoru.
- Energia sieci fluorku litu.
Suma wszystkich tych entalpii da standardową entalpię tworzenia fluorku litu.
W praktyce entalpię tworzenia fluorku litu można określić doświadczalnie, ale energii sieci nie da się zmierzyć bezpośrednio. W związku z tym równanie jest uporządkowane w celu oceny energii sieci.
Związki organiczne
Reakcje tworzenia większości związków organicznych są hipotetyczne. Na przykład węgiel i wodór nie będą bezpośrednio reagować z wytworzeniem metanu (CH 4 ), tak że standardowej entalpii tworzenia nie można bezpośrednio zmierzyć. Jednak standardową entalpię spalania można łatwo zmierzyć za pomocą kalorymetrii bombowej . Standardowa entalpia tworzenia jest następnie określana za pomocą prawa Hessa . Spalanie metanu (CH 4 + 2 O 2 → CO 2 + 2 H 2 O) jest równoważne sumie hipotetycznego rozkładu na pierwiastki, po którym następuje spalanie pierwiastków z wytworzeniem dwutlenku węgla i wody:
- CH 4 → C + 2 H 2
- C + O 2 → CO 2
- 2 H 2 + O 2 → 2 H 2 O
Stosowanie prawa Hessa,
- Δ grzebień H ⦵ (CH 4 ) = [Δ f H ⦵ (CO 2 ) + 2 Δ f H ⦵ (H 2 O)] − Δ f H ⦵ (CH 4 ).
Ustalenie standardu entalpii formacji,
- Δ f H ⦵ (CH 4 ) = [Δ f H ⦵ (CO 2 ) + 2 Δ f H ⦵ (H 2 O)] − Δ grzebień H ⦵ (CH 4 ).
Wartość hemibursztynianu f H ⦵ (CH 4 ) jest ustalona na -74,8 kJ / mol. Znak ujemny wskazuje, że reakcja, gdyby miała postępować, byłaby egzotermiczna ; oznacza to, że metan jest entalpicznie bardziej stabilny niż gazowy wodór i węgiel.
Możliwe jest przewidzenie ciepła tworzenia prostych nieodkształconych związków organicznych metodą addytywności grup ciepła tworzenia .
Użyj w obliczeniach dla innych reakcji
Średnia entalpia każdej reakcji może być obliczona na podstawie standardowych entalpii tworzenia reagentów i produktów przy użyciu prawa Hessa. Dana reakcja jest uważana za rozkład wszystkich reagentów na pierwiastki w ich stanach standardowych, po którym następuje powstanie wszystkich produktów. Ciepło reakcji jest wówczas pomniejszone o sumę standardowych entalpii tworzenia reagentów (każda pomnożona przez odpowiedni współczynnik stechiometryczny, ν ) plus suma standardowych entalpii tworzenia produktów (każda również pomnożona przez odpowiedni współczynnik stechiometryczny współczynnik), jak pokazano w poniższym równaniu:
- Δ r H ⦵ = Σ ν Δ f H ⦵ (produkty) − Σ ν Δ f H ⦵ (reagenty).
Jeśli standardowa entalpia produktów jest mniejsza niż standardowa entalpia reagentów, standardowa entalpia reakcji jest ujemna. Oznacza to, że reakcja jest egzotermiczna. Odwrotność też jest prawdziwa; standardowa entalpia reakcji jest dodatnia dla reakcji endotermicznej. Ta kalkulacja ma milczące założenie idealnego rozwiązania pomiędzy reagentami i produktami, gdzie entalpia mieszania wynosi zero.
Na przykład do spalania metanu CH 4 + 2 O 2 → CO 2 + 2 H 2 O:
- Δ r H ⦵ = [Δ f H ⦵ (CO 2 ) + 2 Δ f H ⦵ (H 2 O)] - [Δ f H ⦵ (CH 4 ) + 2 Δ f H ⦵ (O 2 )].
Jednak O 2 jest pierwiastkiem w swoim stanie standardowym, więc Δ f H ⦵ (O 2 ) = 0, a ciepło reakcji jest uproszczone do
- Δ r H ⦵ = [Δ f H ⦵ (CO 2 ) + 2 Δ f H ⦵ (H 2 O)] − Δ f H ⦵ (CH 4 ),
co jest równaniem w poprzednim rozdziale na entalpię spalania Δ grzebień H ⦵ .
Kluczowe pojęcia dotyczące wykonywania obliczeń entalpii
- Kiedy reakcja jest odwrócona, wielkość Δ H pozostaje taka sama, ale znak się zmienia.
- Gdy zrównoważone równanie reakcji jest pomnożone przez liczbę całkowitą, odpowiednia wartość Δ H musi również zostać pomnożona przez tę liczbę całkowitą.
- Zmianę entalpii dla reakcji można obliczyć z entalpii tworzenia reagentów i produktów
- Elementy w swoich stanach standardowych nie mają wpływu na obliczenia entalpii reakcji, ponieważ entalpia elementu w stanie standardowym wynosi zero. Alotropy pierwiastka innego niż stan standardowy na ogół mają niezerowe standardowe entalpie tworzenia.
Przykłady: standardowe entalpie tworzenia w 25 °C
Właściwości termochemiczne wybranych substancji w 298,15 K i 1 atm
Substancje nieorganiczne
| Gatunek | Faza | Wzór chemiczny | Δ f H ⦵ /(kJ/mol) |
|---|---|---|---|
| Aluminium | |||
| Aluminium | Solidny | Glin | 0 |
| Chlorek glinu | Solidny | AlCl 3 | -705.63 |
| Tlenek glinu | Solidny | Al 2 O 3 | −1675,5 |
| Wodorotlenek glinu | Solidny | Al(OH) 3 | -1277 |
| Siarczan glinu | Solidny | Al 2 (SO 4 ) 3 | -3440 |
| Bar | |||
| Chlorek baru | Solidny | BaCl 2 | -858,6 |
| Węglan baru | Solidny | BaCO 3 | -1216 |
| Wodorotlenek baru | Solidny | Ba(OH) 2 | -944,7 |
| Tlenek baru | Solidny | BaO | -548.1 |
| Siarczan baru | Solidny | BaSO 4 | -1473,2 |
| Beryl | |||
| Beryl | Solidny | Być | 0 |
| Wodorotlenek berylu | Solidny | Be(OH) 2 | −903 |
| Tlenek berylu | Solidny | BeO | -609.4 |
| Bor | |||
| trichlorek boru | Solidny | bcl 3 | -402,96 |
| Brom | |||
| Brom | Płyn | Br 2 | 0 |
| Jon bromkowy | Wodny | Br − | -121 |
| Brom | Gaz | Br | 111,884 |
| Brom | Gaz | Br 2 | 30,91 |
| Trifluorek bromu | Gaz | BrF 3 | −255,60 |
| bromowodór | Gaz | HBr | −36,29 |
| Kadm | |||
| Kadm | Solidny | Płyta CD | 0 |
| Tlenek kadmu | Solidny | CdO | -258 |
| Wodorotlenek kadmu | Solidny | Cd(OH) 2 | -561 |
| Siarczek kadmu | Solidny | CdS | -162 |
| Siarczan kadmu | Solidny | CDSO 4 | -935 |
| Cez | |||
| Cez | Solidny | Cs | 0 |
| Cez | Gaz | Cs | 76,50 |
| Cez | Płyn | Cs | 2,09 |
| Jon cezu(I) | Gaz | CS + | 457.964 |
| Chlorek cezu | Solidny | CsCl | -443,04 |
| Wapń | |||
| Wapń | Solidny | Ca | 0 |
| Wapń | Gaz | Ca | 178,2 |
| Jon wapnia(II) | Gaz | Ca 2+ | 1925.90 |
| Jon wapnia(II) | Wodny | Ca 2+ | -542,7 |
| Węglik wapnia | Solidny | CaC 2 | -59.8 |
| Węglan wapnia ( Kalcyt ) | Solidny | CaCO 3 | -1206,9 |
| Chlorek wapnia | Solidny | CaCl 2 | -795,8 |
| Chlorek wapnia | Wodny | CaCl 2 | -877,3 |
| Fosforan wapniowy | Solidny | Ca 3 (PO 4 ) 2 | −4132 |
| Fluorek wapnia | Solidny | CaF 2 | -1219,6 |
| Wodorek wapnia | Solidny | CaH 2 | −186,2 |
| Wodorotlenek wapnia | Solidny | Ca(OH) 2 | -986,09 |
| Wodorotlenek wapnia | Wodny | Ca(OH) 2 | -1002,82 |
| Tlenek wapnia | Solidny | CaO | -635.09 |
| Siarczan wapnia | Solidny | CaSO 4 | -1434,52 |
| Siarczek wapnia | Solidny | CaS | −482,4 |
| Wollastonit | Solidny | CaSiO 3 | -1630 |
| Węgiel | |||
| Węgiel ( Grafit ) | Solidny | C | 0 |
| Węgiel ( Diament ) | Solidny | C | 1,9 |
| Węgiel | Gaz | C | 716,67 |
| Dwutlenek węgla | Gaz | CO 2 | -393,509 |
| Dwusiarczek węgla | Płyn | CS 2 | 89,41 |
| Dwusiarczek węgla | Gaz | CS 2 | 116,7 |
| Tlenek węgla | Gaz | WSPÓŁ | -110,525 |
| Karbonylu ( fosgen ) | Gaz | COCl 2 | -218,8 |
| Dwutlenek węgla (niezjonizowany) | Wodny | CO 2 (aq) | -419,26 |
| Jon wodorowęglanowy | Wodny | HCO 3 – | -689,93 |
| Jon węglanowy | Wodny | CO 3 2– | -675,23 |
| Chlor | |||
| Chlor jednoatomowy | Gaz | Cl | 121,7 |
| Jon chlorkowy | Wodny | Cl − | -167.2 |
| Chlor | Gaz | Ćw 2 | 0 |
| Chrom | |||
| Chrom | Solidny | Cr | 0 |
| Miedź | |||
| Miedź | Solidny | Cu | 0 |
| Tlenek miedzi(II) | Solidny | CuO | -155.2 |
| Siarczan miedzi(II) | Wodny | CuSO 4 | -769,98 |
| Fluor | |||
| Fluor | Gaz | F 2 | 0 |
| Wodór | |||
| Wodór jednoatomowy | Gaz | h | 218 |
| Wodór | Gaz | H 2 | 0 |
| Woda | Gaz | H 2 O | -241.818 |
| Woda | Płyn | H 2 O | -285,8 |
| Jon wodorowy | Wodny | H + | 0 |
| Jon wodorotlenkowy | Wodny | OH - | −230 |
| Nadtlenek wodoru | Płyn | H 2 O 2 | −187,8 |
| Kwas fosforowy | Płyn | H 3 PO 4 | -1288 |
| Cyjanowodór | Gaz | HCN | 130,5 |
| bromowodór | Płyn | HBr | -36.3 |
| Chlorek wodoru | Gaz | HCl | −92,30 |
| Chlorek wodoru | Wodny | HCl | -167.2 |
| Fluorowodór | Gaz | HF | −273,3 |
| Jodek wodorowy | Gaz | CZEŚĆ | 26,5 |
| Jod | |||
| Jod | Solidny | ja 2 | 0 |
| Jod | Gaz | ja 2 | 62,438 |
| Jod | Wodny | ja 2 | 23 |
| jodek ion | Wodny | ja − | -55 |
| Żelazo | |||
| Żelazo | Solidny | Fe | 0 |
| Węglik żelaza ( cementyt ) | Solidny | Fe 3 C | 5.4 |
| Węglan żelaza(II) ( syderyt ) | Solidny | FeCO 3 | -750,6 |
| Chlorek żelaza(III) | Solidny | FeCl 3 | -399,4 |
| Tlenek żelaza(II) ( Wüstite ) | Solidny | FeO | -272 |
| Tlenek żelaza(II,III) ( Magnetyt ) | Solidny | Fe 3 O 4 | -1118,4 |
| Tlenek żelaza(III) ( hematyt ) | Solidny | Fe 2 O 3 | -824,2 |
| Siarczan żelaza(II) | Solidny | FeSO 4 | -929 |
| Siarczan żelaza(III) | Solidny | Fe 2 (SO 4 ) 3 | -2583 |
| Siarczek żelaza(II) | Solidny | FeS | −102 |
| Piryt | Solidny | FeS 2 | −178 |
| Ołów | |||
| Ołów | Solidny | Pb | 0 |
| Dwutlenek ołowiu | Solidny | PbO 2 | -277 |
| Siarczek ołowiu | Solidny | PbS | −100 |
| Siarczan ołowiu | Solidny | PbSO 4 | -920 |
| Azotan ołowiu(II) | Solidny | Pb(NO 3 ) 2 | -452 |
| Siarczan ołowiu(II) | Solidny | PbSO 4 | -920 |
| Lit | |||
| Fluorek litu | Solidny | LiF | -616,93 |
| Magnez | |||
| Magnez | Solidny | Mg | 0 |
| Jon magnezu | Wodny | Mg 2+ | -466,85 |
| Węglan magnezu | Solidny | MgCO 3 | −1095.797 |
| Chlorek magnezu | Solidny | MgCl 2 | -641,8 |
| Wodorotlenek magnezu | Solidny | Mg(OH) 2 | -924,54 |
| Wodorotlenek magnezu | Wodny | Mg(OH) 2 | -926,8 |
| Tlenek magnezu | Solidny | MgO | -601,6 |
| Siarczan magnezu | Solidny | MgSO 4 | -1278.2 |
| Mangan | |||
| Mangan | Solidny | Mn | 0 |
| Tlenek manganu(II) | Solidny | MnO | -384,9 |
| Tlenek manganu(IV) | Solidny | MnO 2 | -519,7 |
| Tlenek manganu(III) | Solidny | Mn 2 O 3 | -971 |
| Tlenek manganu(II,III) | Solidny | Mn 3 O 4 | −1387 |
| Nadmanganian | Wodny |
MnO− 4 |
-543 |
| Rtęć | |||
| Tlenek rtęci(II) (czerwony) | Solidny | HgO | −90,83 |
| Siarczek rtęci (czerwony, cynober ) | Solidny | HgS | -58.2 |
| Azot | |||
| Azot | Gaz | N 2 | 0 |
| Amoniak (wodorotlenek amonu) | Wodny | NH 3 (NH 4 OH) | -80.8 |
| Amoniak | Gaz | NH 3 | -46.1 |
| Azotan amonowy | Solidny | NH 4 NO 3 | -365,6 |
| Chlorek amonu | Solidny | NH 4 Cl | -314,55 |
| Dwutlenek azotu | Gaz | NIE 2 | 33,2 |
| Hydrazyna | Gaz | N 2 H 4 | 95,4 |
| Hydrazyna | Płyn | N 2 H 4 | 50,6 |
| Podtlenek azotu | Gaz | N 2 O | 82,05 |
| Tlenek azotu | Gaz | NIE | 90,29 |
| Czterotlenek diazotu | Gaz | N 2 O 4 | 9.16 |
| pięciotlenek diazotu | Solidny | N 2 O 5 | -43.1 |
| pięciotlenek diazotu | Gaz | N 2 O 5 | 11,3 |
| Kwas azotowy | Wodny | HNO 3 | −207 |
| Tlen | |||
| Tlen jednoatomowy | Gaz | O | 249 |
| Tlen | Gaz | O 2 | 0 |
| Ozon | Gaz | O 3 | 143 |
| Fosfor | |||
| Fosfor biały | Solidny | P 4 | 0 |
| Czerwony fosfor | Solidny | P | -17,4 |
| Czarny fosfor | Solidny | P | -39.3 |
| Trójchlorek fosforu | Płyn | PCl 3 | -319,7 |
| Trójchlorek fosforu | Gaz | PCl 3 | -278 |
| pięciochlorek fosforu | Solidny | PCl 5 | −440 |
| pięciochlorek fosforu | Gaz | PCl 5 | -321 |
| pięciotlenek fosforu | Solidny | P 2 O 5 | -1505,5 |
| Potas | |||
| Bromek potasu | Solidny | KBr | -392,2 |
| Weglan potasu | Solidny | K 2 CO 3 | -1150 |
| Chloran potasu | Solidny | KClO 3 | -391,4 |
| Chlorek potasu | Solidny | KCl .Name | -436,68 |
| Fluorek potasu | Solidny | KF | −562,6 |
| Tlenek potasu | Solidny | K 2 O | -363 |
| Azotan potasu | Solidny | KNO 3 | −494,5 |
| Nadchloran potasu | Solidny | KClO 4 | -430,12 |
| Krzem | |||
| Krzem | Gaz | Si | 368.2 |
| Węglik krzemu | Solidny | SiC | -74.4, -71.5 |
| Tetrachlorek krzemu | Płyn | SiCU 4 | -640,1 |
| Krzemionka ( Kwarc ) | Solidny | SiO 2 | -910,86 |
| Srebro | |||
| Bromek srebra | Solidny | AgBr | -99,5 |
| chlorek srebra | Solidny | AgCl | -127.01 |
| Jodek srebra | Solidny | AgI | -62.4 |
| Tlenek srebra | Solidny | Ag 2 O | -31.1 |
| Siarczek srebra | Solidny | Ag 2 S | -31.8 |
| Sód | |||
| Sód | Solidny | Na | 0 |
| Sód | Gaz | Na | 107,5 |
| Wodorowęglan sodu | Solidny | NaHCO 3 | -950,8 |
| Węglan sodu | Solidny | Na 2 CO 3 | -1130,77 |
| Chlorek sodu | Wodny | NaCl | -407.27 |
| Chlorek sodu | Solidny | NaCl | -411,12 |
| Chlorek sodu | Płyn | NaCl | -385,92 |
| Chlorek sodu | Gaz | NaCl | −181,42 |
| chloran sodu | Solidny | NaClO 3 | -365,4 |
| Fluorek sodu | Solidny | NaF | -569,0 |
| Wodorotlenek sodu | Wodny | NaOH | -469,15 |
| Wodorotlenek sodu | Solidny | NaOH | -425,93 |
| Podchloryn sodu | Solidny | NaOCl | -347,1 |
| Azotan sodu | Wodny | NaNO 3 | -446,2 |
| Azotan sodu | Solidny | NaNO 3 | -424,8 |
| Tlenek sodu | Solidny | Na 2 O | -414,2 |
| Siarka | |||
| Siarka (jednoskośna) | Solidny | S 8 | 0,3 |
| Siarka (rombowa) | Solidny | S 8 | 0 |
| Siarkowodór | Gaz | H 2 S | -20,63 |
| Dwutlenek siarki | Gaz | SO 2 | -296,84 |
| Trójtlenek siarki | Gaz | SO 3 | -395,7 |
| Kwas Siarkowy | Płyn | H 2 SO 4 | -814 |
| Cyna | |||
| Tytan | |||
| Tytan | Gaz | Ti | 468 |
| Tetrachlorek tytanu | Gaz | TiCl 4 | -763,2 |
| Tetrachlorek tytanu | Płyn | TiCl 4 | -804,2 |
| Dwutlenek tytanu | Solidny | TiO 2 | -944,7 |
| Cynk | |||
| Cynk | Gaz | Zn | 130,7 |
| Chlorek cynku | Solidny | ZnCl 2 | -415,1 |
| Tlenek cynku | Solidny | ZnO | -348,0 |
| Siarczan cynku | Solidny | ZnSO 4 | -980,14 |
Węglowodory alifatyczne
| Formuła | Nazwa | Δ f H ⦵ /(kcal/mol) | Δ f H ⦵ /(kJ/mol) |
|---|---|---|---|
| Prosty łańcuch | |||
| CH 4 | Metan | -17,9 | -74.9 |
| C, 2 H 6 | Etan | -20,0 | -83,7 |
| C 2 H 4 | Etylen | 12,5 | 52,5 |
| C, 2 H 2 | Acetylen | 54,2 | 226,8 |
| C 3 H 8 | Propan | -25,0 | -104.6 |
| C 4 H 10 | n - butan | -30,0 | -125,5 |
| C 5 H 12 | n - Pentan | -35.1 | -146,9 |
| C 6 H 14 | n - Heksan | -40,0 | -167.4 |
| C 7 H 16 | n - heptan | -44.9 | −187,9 |
| C 8 H 18 | n - oktan | −49,8 | -208.4 |
| C 9 H 20 | n - nonan | -54.8 | -229,3 |
| C 10 H 22 | n - Dekan | -59,6 | -249,4 |
| Rozgałęzione izomery C 4 Alkan | |||
| C 4 H 10 | Izobutan (metylopropan) | -32.1 | -134,3 |
| Rozgałęzione izomery C 5 Alkan | |||
| C 5 H 12 | Neopentan (dimetylopropan) | -40,1 | −167,8 |
| C 5 H 12 | Izopentan (metylobutan) | -36,9 | −154,4 |
| Rozgałęzione izomery C 6 Alkan | |||
| C 6 H 14 | 2,2-dimetylobutan | -44,5 | −186,2 |
| C 6 H 14 | 2,3-dimetylobutan | -42,5 | -177.8 |
| C 6 H 14 | 2-Metylopentan (izoheksan) | -41.8 | −174,9 |
| C 6 H 14 | 3-Metylopentan | -41.1 | -172.0 |
| Rozgałęzione izomery C 7 Alkan | |||
| C 7 H 16 | 2,2-dimetylopentan | -49.2 | −205,9 |
| C 7 H 16 | 2,2,3-trimetylobutan | -49.0 | -205,0 |
| C 7 H 16 | 3,3-dimetylopentan | -48.1 | −201,3 |
| C 7 H 16 | 2,3-dimetylopentan | −47,3 | −197,9 |
| C 7 H 16 | 2,4-dimetylopentan | -48.2 | −201,7 |
| C 7 H 16 | 2-Metyloheksan | -46,5 | -194.6 |
| C 7 H 16 | 3-Metyloheksan | -45.7 | -191,2 |
| C 7 H 16 | 3-etylopentan | -45.3 | -189,5 |
| Rozgałęzione izomery C 8 Alkan | |||
| C 8 H 18 | 2,3-dimetyloheksan | -55.1 | −230,5 |
| C 8 H 18 | 2,2,3,3-Tetrametylobutan | -53,9 | −225,5 |
| C 8 H 18 | 2,2-dimetyloheksan | -53,7 | -224,7 |
| C 8 H 18 | 2,2,4-trimetylopentan (izooktan) | -53,5 | −223,8 |
| C 8 H 18 | 2,5-dimetyloheksan | −53,2 | −222,6 |
| C 8 H 18 | 2,2,3-trimetylopentan | -52,6 | −220,1 |
| C 8 H 18 | 3,3-dimetyloheksan | -52,6 | −220,1 |
| C 8 H 18 | 2,4-dimetyloheksan | -52.4 | -219,2 |
| C 8 H 18 | 2,3,4-trimetylopentan | -51.9 | -217,1 |
| C 8 H 18 | 2,3,3-trimetylopentan | -51.7 | -216,3 |
| C 8 H 18 | 2-Metyloheptan | -51,5 | -215,5 |
| C 8 H 18 | 3-etylo-3-metylopentan | -51.4 | -215.1 |
| C 8 H 18 | 3,4-dimetyloheksan | -50,9 | -213,0 |
| C 8 H 18 | 3-etylo-2-metylopentan | -50,4 | -210.9 |
| C 8 H 18 | 3-Metyloheptan | -60,3 | -252,5 |
| C 8 H 18 | 4-Metyloheptan | ? | ? |
| C 8 H 18 | 3-etyloheksan | ? | ? |
| C 9 Rozgałęzione izomery alkanu (wybrane) | |||
| C 9 H 20 | 2,2,4,4-tetrametylopentan | -57.8 | -241,8 |
| C 9 H 20 | 2,2,3,3-Tetrametylopentan | -56,7 | -237,2 |
| C 9 H 20 | 2,2,3,4-tetrametylopentan | -56,6 | -236,8 |
| C 9 H 20 | 2,3,3,4-tetrametylopentan | -56.4 | -236,0 |
| C 9 H 20 | 3,3-Dietylopentan | -55.7 | −233,0 |
Inne związki organiczne
| Gatunek | Faza | Wzór chemiczny | Δ f H ⦵ /(kJ/mol) |
|---|---|---|---|
| Aceton | Płyn | C 3 H 6 O | -248,4 |
| Benzen | Płyn | C 6 H 6 | 48,95 |
| Kwas benzoesowy | Solidny | C 7 H 6 O 2 | -385,2 |
| Tetrachlorek węgla | Płyn | CCI 4 | -135,4 |
| Tetrachlorek węgla | Gaz | CCI 4 | -95,98 |
| Etanol | Płyn | C 2 H 5 OH | -277,0 |
| Etanol | Gaz | C 2 H 5 OH | −235,3 |
| Glukoza | Solidny | C 6 H 12 O 6 | -1271 |
| Izopropanol | Gaz | C 3 H 7 OH | -318,1 |
| Metanol (alkohol metylowy) | Płyn | CH 3 OH | -238,4 |
| Metanol (alkohol metylowy) | Gaz | CH 3 OH | −201,0 |
| Linoleinian metylu ( Biodiesel ) | Gaz | C 19 H 34 O 2 | -356,3 |
| Sacharoza | Solidny | C 12 H 22 O 11 | −2226.1 |
| Trichlorometan ( chloroform ) | Płyn | CHCI 3 | −134,47 |
| Trichlorometan ( chloroform ) | Gaz | CHCI 3 | -103,18 |
| Chlorek winylu | Solidny | C 2 H 3 Cl | −94,12 |
Zobacz też
Bibliografia
- Zumdahl, Steven (2009). Zasady chemiczne (6 wyd.). Boston. Nowy Jork: Houghton Mifflin. s. 384-387. Numer ISBN 978-0-547-19626-8.


