Syndekan - Syndecan
| Syndecan | |||||||||
|---|---|---|---|---|---|---|---|---|---|
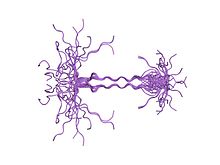 Struktura roztworu całej domeny cytoplazmatycznej Syndecan-4 w obecności 4,5-bisfosforanu fosfatydyloinozytolu.
| |||||||||
| Identyfikatory | |||||||||
| Symbol | Syndecan | ||||||||
| Pfam | PF01034 | ||||||||
| InterPro | IPR001050 | ||||||||
| PROSITE | PDOC00745 | ||||||||
| SCOP2 | 1ejp / zakres / SUPFAM | ||||||||
| Nadrodzina OPM | 535 | ||||||||
| Białko OPM | 6th | ||||||||
| Membrana | 18 | ||||||||
| |||||||||
Syndecans są pojedyncze transbłonowe domeny białka , które jak się uważa, działają jako koreceptorów, zwłaszcza dla receptorów sprzężonych z białkiem G . Dokładniej, takie białko rdzeniowe przeprowadzić trzy do pięciu siarczan heparanu i siarczan chondroityny łańcuchów, czyli są one proteoglikanów , które pozwalają na wzajemne oddziaływanie z wielu różnych ligandów, w tym fibroblastów czynniki wzrostu , czynnik wzrostu śródbłonka naczyniowego , transformujący czynnik wzrostu beta, fibronektyny i antytrombina -1. Interakcje między fibronektyną a niektórymi syndekanami mogą być modulowane przez białko macierzy zewnątrzkomórkowej - tenascynę C .
Członkowie rodziny i struktura
Rodzina białek syndekanu ma czterech członków. Syndekany 1 i 3 oraz syndekany 2 i 4 , tworzące oddzielne podrodziny, powstały w wyniku duplikacji genów i rozbieżnej ewolucji z jednego genu przodków. Liczby syndekanów odzwierciedlają kolejność sklonowania cDNA każdego członka rodziny . Wszystkie syndekany mają N-końcowy peptyd sygnałowy , ektodomenę , pojedynczą hydrofobową domenę transbłonową i krótką C-końcową domenę cytoplazmatyczną . Wszystkie syndekany są zakotwiczone do błony komórkowej przez hydrofobową domenę transbłonową o długości 24-25 aminokwasów, w przeciwieństwie do innego typu proteoglikanów powierzchni komórek, które przyłączają się do błony komórkowej za pomocą wiązania glikozylo-fosfatydylo-inozytol. Najbardziej oczywiste różnice między syndekanami obejmują (wraz z różnicami w rozmieszczeniu) podklasyfikacje rodziny w zależności od istnienia miejsc wiążących GAG na obu końcach ektodomeny ( syndekan-1 i -3 ) lub tylko w części dystalnej ( syndekan -2 i -4 ) oraz stosunkowo długi obszar bogaty w Thr-Ser-Pro w środku ektodomeny syndekanu-3. Ektodomeny wykazują najmniejszą konserwację sekwencji aminokwasów , nie większą niż 10–20%; w przeciwieństwie do tego domeny transbłonowe i cytoplazmatyczne mają około 60–70% identyczności sekwencji aminokwasów. Domeny transbłonowe zawierają nietypowy motyw sekwencji alaniny/glicyny , podczas gdy domena cytoplazmatyczna składa się zasadniczo z dwóch regionów konserwowanej sekwencji aminokwasowej (C1 i C2), oddzielonych centralną zmienną sekwencją aminokwasów, która jest odrębna dla każdego członka rodziny ( V).
W komórkach ssaków syndekany są wyrażane przez unikalne geny zlokalizowane na różnych chromosomach. Jest to ogólny brak dowodów na alternatywny splicing w genach syndekanu. Wszyscy członkowie rodziny syndecan mają 5 egzonów. Różnicę w wielkości syndekanów przypisuje się zmiennej długości eksonu 3, który koduje domenę odstępnika [1, 14]. U ludzi długość aminokwasów syndekanu 1, 2, 3 i 4 wynosi odpowiednio 310, 201, 346 i 198. Łańcuchy glikozaminoglikanów, należące do grupy siarczanów heparanu, są ważnym składnikiem syndekanu i odpowiadają za różnorodny zestaw funkcji syndekanu. Dodanie glikozaminoglikanów do syndekanu jest kontrolowane przez szereg zdarzeń potranslacyjnych. Preferencyjne miejsce addycji glikozaminoglikanów znajduje się na reszcie seryny, a następnie na reszcie glicyny, gdzie łącznik jest przyłączony do wydłużania glikozaminoglikanów przez α-N-acetyloglukozaminylotransferazę I [1]. Łącznik składa się z czterech sacharydów, z których pierwszy to ksyloza, która jest niezwykłym cukrem w unikalnym miejscu, przyłączona do seryny rdzenia białkowego, a po niej kolejno dwie galaktozy i kwas β-D-glukuronowy [1, 12].
Wyrażenie
Syndekany ulegają ekspresji na powierzchni komórki w sposób specyficzny dla komórki. Na przykład, w komórkach i tkankach myszy, syndekan 1 jest silnie eksprymowany w komórkach fibroblastycznych i nabłonkowych. Jest szczególnie wysoki w keratynocytach, a niski w komórkach śródbłonka i nerwowych. Tkanki te obejmują skórę, wątrobę, nerki i płuca. Syndekan 2 jest silnie eksprymowany w komórkach śródbłonka, nerwowych i fibroblastycznych, podczas gdy ma niski poziom ekspresji w komórkach nabłonkowych. Jest specyficzny dla tkanek, takich jak wątroba, śródbłonek i fibroblasty. Syndekan 3 jest silnie eksprymowany w komórkach nerwowych, ale ma niską lub niewykrywalną ilość w komórkach nabłonka. W tkankach jest specyficzny dla mózgu i wyrażany na niskim poziomie w wątrobie, nerkach, płucach i jelicie cienkim. Syndekan 4 jest silnie wyrażany przez komórki nabłonkowe i fibroblastyczne, ale ma niski poziom ekspresji w komórkach nerwowych i śródbłonkowych. W tkankach preferencyjnie ulega ekspresji w wątrobie i płucach [11].
Funkcje
Funkcjonalność syndekanu jest wspierana przez glikozaminoglikany, które pomagają w interakcji z różnymi ligandami zewnątrzkomórkowymi. W zależności od lokalizacji syndekanu w komórce, glikozaminoglikany mają różne struktury, aby sprostać funkcjonalnym potrzebom regionu. Wiadomo, że syndekany tworzą homologiczne oligomery, które mogą być ważne dla ich funkcji.
Funkcje syndekanu można podzielić na cztery sposoby. Pierwszym z nich jest aktywacja receptora czynnika wzrostu. Glikozaminoglikany przyłączone do syndekanu pomagają wiązać różne czynniki wzrostu w celu aktywacji ważnych mechanizmów sygnalizacji komórkowej. Czynniki wzrostu, takie jak FGF2 , HGF , EGF, VEGF, neureguliny i inne oddziałują z syndekanami [1, 2, 8]. Na przykład, w miejscu uszkodzenia tkanki, rozpuszczalne ektodomeny syndekanu-1 są rozszczepiane przez heparanazy, tworząc fragmenty podobne do heparyny, które aktywują bFGF [13]. Podczas gdy większość czynników wzrostu oddziałuje z syndekanami poprzez łańcuchy siarczanu heparanu, prosekrecyjna mitogen lakrytyna wymaga heparanazy zarówno do odsłonięcia, jak i utworzenia miejsca wiązania na N-końcu syndekanu 1.
Drugi to adhezja matrycy. Syndekany wiążą się ze strukturalnymi cząsteczkami macierzy zewnątrzkomórkowej, takimi jak kolageny I, III, V, fibronektyna, trombospondyna i tenascyna, zapewniając strukturalne wsparcie dla adhezji [1, 2].
Trzecią funkcją jest adhezja komórka-komórka. Dowody na rolę syndekanu w adhezji komórka-komórka pochodzą z linii komórek ludzkiego szpiczaka. Te komórki szpiczaka wykazywały niedobór zdolności przylegania do siebie w macierzy agregacji za pośrednictwem rotacji. Ten niedobór przypisuje się brakowi ekspresji syndekanu 1. Syndekan 4 oddziałuje również z białkami integryn w celu adhezji komórka–komórka [1, 2, 12].
Ostatnia rola polega na supresji i progresji guza. Syndekany działają jako inhibitory nowotworów, zapobiegając proliferacji komórek nowotworowych linii komórkowych. Na przykład w linii komórek nowotworowych pochodzenia nabłonkowego S115 ektodomena syndekanu 1 hamuje wzrost komórek S115 bez wpływu na wzrost prawidłowych komórek nabłonka [7]. Jednak ekspresja syndekanu 1 odgrywa również rolę w progresji guza w szpiczaku i innych nowotworach [5, 6, 9, 15]. Łączy się z wewnątrzkomórkowym cytoszkieletem aktynowym i pomaga w utrzymaniu prawidłowej morfologii arkusza nabłonka
Domeny białkowe
Białka syndekanu mogą zawierać następujące domeny białkowe,
- Sekwencja sygnałowa;
- Domena zewnątrzkomórkowa (ektodomena) o zmiennej długości, której sekwencja nie jest zachowana ewolucyjnie w różnych formach syndekanów. Domena ektodomena zawiera miejsca przyłączenia łańcuchów bocznych glikozaminoglikanów siarczanu heparanu;
- Region transbłonowy;
- Wysoce konserwatywna domena cytoplazmatyczna składająca się z około 30 do 35 reszt, która może oddziaływać z białkami cytoszkieletu.
Znaczenie kliniczne
Endometrioza
Syndekan-4 jest podwyższony w endometriozie, a hamowanie syndekanu-4 w ludzkich komórkach endometriotycznych powoduje zmniejszenie inwazyjnego wzrostu in vitro i zmiany w ekspresji metaloproteinazy macierzy .
Zapalenie kości i stawów
Syndekan-4 jest podwyższony w chorobie zwyrodnieniowej stawów, a hamowanie syndekanu-4 zmniejsza zniszczenie chrząstki w mysich modelach OA.
Regulacja metaboliczna i skład ciała
Homolog dSdc z Drosophila i ludzki SDC4 są zaangażowane w homeostazę energetyczną.
Szpiczak mnogi
Syndecan1 jest podwyższony w szpiczaku mnogim . Wysokie poziomy zrzuconego syndekanu1 w surowicy pacjenta zazwyczaj są skorelowane ze złym rokowaniem.
Syndecan 1 jest najlepiej zbadanym ze wszystkich syndekanów w badaniach nad rakiem. Wiele badań wykazało, że syndekan 1 odgrywa ważną rolę w progresji raka, a także może być stosowany jako biomarker raka. Na przykład ekspresja syndekanu 1 jest wyższa w szpiku kostnym pacjentów cierpiących na szpiczaka mnogiego [9]. W jednym z opublikowanych badań komórki eksprymujące rozpuszczalną ektodomenę syndekanu 1 promowały wzrost i przerzuty guzów B-limfoidalnych w większym stopniu niż komórki z powierzchniowym syndekanem 1 lub pozbawione ekspresji syndekanu 1 [16]. Podobnie ekspresja syndekanu 1 została powiązana z niskim zróżnicowaniem w raku płaskonabłonkowym głowy i szyi [15].
Syndekan 1 został również powiązany z progresją raka poprzez pośredniczenie w działaniu czynników wzrostu w komórkach. Na przykład ekspresja syndekanu 1 jest zwiększona w przewodowych rakach piersi i jest związana z czynnikami angiogenezy i limfangiogenezy [5]. Badania pacjentów cierpiących na raka endometrium wykazały, że te pacjentki mają zwiększoną ekspresję syndekanu 1, a także, że ekspresja tego białka pozytywnie reguluje rozrost endometrium, który może prowadzić do raka endometrium [6].
Bibliografia
- Gotte, Martin; Kersting, Chrześcijanin; Radke, Izabela; Kiesel, Ludwig; Wülfing, Pia (2007). „Podpis ekspresji syndekanu-1 (CD138), E-kadheryny i c-met jest związany z czynnikami angiogenezy i limfangiogenezy w przewodowym raku piersi in situ” . Badania nad rakiem piersi . 9 (1): R8. doi : 10.1186/bcr1641 . PMC 1851383 . PMID 17244359 .
- Kim, H; Choi, DS; Chang, SJ; Han, JH; Min, CK; Chang, KH; Ryu, HS (2010). „Ekspresja syndekanu-1 jest związana z ryzykiem progresji przerostu endometrium do raka endometrium” . Czasopismo Ginekologii Onkologicznej . 21 (1): 50–55. doi : 10.3802/jgo.2010.21.1.50 . PMC 2849949 . PMID 20379448 .
- Mali, M; Andtfolk, H; Miettinen, HM; Jalkanena, M (1994). „Tłumienie wzrostu komórek nowotworowych przez syndekan-1 ektodomenę” . Czasopismo Chemii Biologicznej . 269 (45): 27795-27798. doi : 10.1016/S0021-9258(18)46853-6 . PMID 7961703 .
- Rapraeger AC (2000). „Sygnalizacja receptora regulowana przez Syndecan” . Czasopismo Biologii Komórki . 149 (5): 995-998. doi : 10.1083/jcb.149.5.995 . PMC 2174822 . PMID 10831602 .
- Seidela, C; Borset, M; Hjertner, O; Cao, D; Abildgaard, N; Hjorth-Hansen, H; Sandersona, RD; Wynagrodzenie, A; Sundan, A (2000). „Wysokie poziomy rozpuszczalnego syndekanu-1 w szpiku kostnym pochodzącym ze szpiczaka: modulacja aktywności czynnika wzrostu hepatocytów”. Krew . 96 (9): 3139–3146. doi : 10.1182/krew.V96.9.3139 . PMID 11049995 .
- Stanford, Kalifornia; biskup JR; Foley, EM; Gonzales, JC; Niesman, IR; Witztum, JL; Esko, JD (2009). „Syndekan-1 jest głównym proteoglikanem siarczanu heparanu pośredniczącym w klirensie wątrobowym lipoprotein bogatych w triglicerydy u myszy” . Journal of Clinical Investigation . 119 (11): 3236–3245. doi : 10.1172/JCI38251 . PMC 2769193 . PMID 19805913 .
- Kim, CW; Goldberger, OA; Gallo, RL; Bernfield, M (1994). „Członkowie rodziny syndekanów proteoglikanów siarczanu heparanu ulegają ekspresji w odrębnych wzorcach komórkowych, tkankowych i rozwojowych” . Biologia molekularna komórki . 5 (7): 797-805. doi : 10.1091/mbc.5.7.9797 . PMC 301097 . PMID 7812048 .
- Shin, J; Lee, W; Lee, D; Koo, BK; Han, ja; Lim, Y; Lasy, A; Couchman, JR; Och, ES (2001). „Struktura roztworu dimerycznej domeny cytoplazmatycznej syndekanu-4”. Biochemia . 40 (29): 8471–8478. doi : 10.1021/bi002750r . PMID 11456484 .
- Kato, M; Wang, H; Kainulainen, V; Fitzgeralda, ML; Ledbetter, S; Ornitz, DM; Bernfield, M (1998). „Degradacja fizjologiczna przekształca rozpuszczalną ektodomenę syndekanu-1 z inhibitora w silny aktywator FGF-2”. Medycyna przyrodnicza . 4 (6): 691–697. doi : 10.1038/nm0698-691 . PMID 9623978 . S2CID 10148022 .
- Saunders, S; Jalkanena, M; O'Farrell, S; Bernfield, M (1989). „Klonowanie molekularne syndekanu, integralnego proteoglikanu błony” . Czasopismo Biologii Komórki . 108 (4): 1547-1556. doi : 10.1083/jcb.108.4.1547 . PMC 2115498 . PMID 2494194 .
- Anttonen, A; Kajanti, M; Heikkila, P; Jalkanena, M; Joensuu, H (1999). „Ekspresja Syndekanu-1 ma znaczenie prognostyczne w raku głowy i szyi” . Brytyjski Dziennik Raka . 79 (3–4): 558–564. doi : 10.1038/sj.bjc.6690088 . PMC 2362450 . PMID 10027330 .
- Yang, Y; Yaccoby, S; Liu, W; Langford, JK; Pumphrey, CY; Teus, A; Epstein, J; Sanderson, RD (2002). „Rozpuszczalny syndekan-1 promuje wzrost guzów szpiczaka in vivo” . Krew . 100 (2): 610–617. doi : 10.1182/krew.V100.2.610 . PMID 12091355 .
