Benzydamina - Benzydamine
 | |
| Dane kliniczne | |
|---|---|
| AHFS / Drugs.com | Międzynarodowe nazwy leków |
Kategoria ciąży |
|
| Drogi administracji |
Doustnie, miejscowo |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Dane farmakokinetyczne | |
| Wiązanie białek | <20% |
| Okres półtrwania eliminacji | 13 godzin |
| Wydalanie | Nerkowy |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CZEBI | |
| CHEMBL | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA |
100.010.354 |
| Dane chemiczne i fizyczne | |
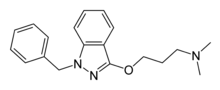
| Formuła | C 19 H 23 N 3 O |
| Masa cząsteczkowa | 309.413 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
| (zweryfikować) | |
Benzydamina (znana również jako Tantum Verde, a w niektórych krajach znana pod nazwą Difflam i Septabene), dostępna jako sól chlorowodorkowa, jest niesteroidowym lekiem przeciwzapalnym (NLPZ) o miejscowym działaniu o właściwościach miejscowo znieczulających i przeciwbólowych , łagodzącym ból i przeciwzapalnych stanów zapalnych jamy ustnej i gardła . Należy do klasy chemikaliów znanych jako indazol .
Historia
Został zsyntetyzowany we Włoszech w 1964 roku i wprowadzony na rynek w 1966 roku.
Zastosowania
Medyczny
- Odonto stomatologii : zapalenie dziąseł , zapalenie jamy ustnej , zapalenie języka , owrzodzenia aftowego , stomatologii i doustne owrzodzeniu na skutek napromieniania .
- Otorynolaryngologia: gorączka gruczołowa , zapalenie gardła , zapalenie migdałków , po wycięciu migdałków , zapalenie błony śluzowej po napromienianiu lub intubacji .
Może być stosowany samodzielnie lub jako uzupełnienie innej terapii dając możliwość zwiększenia efektu terapeutycznego przy niewielkim ryzyku interakcji.
Na niektórych rynkach lek dostarczany jest w postaci kremu dostępnego bez recepty (Lonol w Meksyku firmy Boehringer Ingelheim ) stosowany do miejscowego leczenia schorzeń układu mięśniowo-szkieletowego: skręceń, nadwyrężeń, zapalenia kaletki, zapalenia ścięgien, zapalenia błony maziowej, bólu mięśni, zapalenia okołostawowego.
Rekreacyjny
Benzydamina była używana rekreacyjnie. W przedawkowaniu działa deliriantycznie i pobudzająco na ośrodkowy układ nerwowy . Takie zażywanie, zwłaszcza wśród nastolatków, odnotowano w Polsce, Brazylii i Rumunii.
Przeciwwskazania
Nie ma przeciwwskazań do stosowania benzydaminy poza stwierdzoną nadwrażliwością .
Skutki uboczne
Benzydamina jest dobrze tolerowana. Czasami może wystąpić drętwienie lub kłucie tkanki jamy ustnej, a także swędzenie, wysypka skórna, obrzęk lub zaczerwienienie skóry, trudności w oddychaniu i świszczący oddech.
Farmakologia
Wiąże się wybiórczo z tkankami objętymi stanem zapalnym ( inhibitor syntetazy prostaglandyn ) i zwykle nie wywołuje niepożądanych efektów ogólnoustrojowych. W przeciwieństwie do innych NLPZ nie hamuje cyklooksygenazy ani lipooksygenazy i nie jest wrzodziejący. Ma silne działanie wzmacniające i uczula krzyżowo na nadużywane narkotyki, takie jak heroina i kokaina u zwierząt. Przypuszcza się, że ma działanie agonistyczne wobec kannabinoidów .
Farmakokinetyka
Benzydamina jest słabo wchłaniana przez skórę i pochwę.
Synteza
Synteza rozpoczyna się od reakcji pochodnej N- benzylowej z antranilanu metylu z kwasem azotawym, w wyniku której otrzymuje się pochodną N- nitrozową . Redukcja za pomocą tiosiarczanu sodu prowadzi do przejściowej hydrazyny ( 3 ), która ulega spontanicznemu wewnętrznemu tworzeniu hydrazydu. Traktowanie enolanu tego amidu 3-chloro-1-dimetyloamkinopropanem daje benzydaminę ( 5 ). Należy zauważyć, że w tej sekcji występuje błąd: US3318905 stwierdza, że pochodna nitrozowa jest redukowana podsiarczynem sodu (ditioninem sodu), a nie podsiarczynem sodu (tiosiarczan sodu), jak pokazano na powyższym schemacie i podano w tekście.
Ciekawą alternatywną syntezą tej substancji jest sekwencyjna reakcja N- benzyloaniliny z fosgenem , a następnie z azydkiem sodu, w wyniku której powstaje odpowiedni azydek karbonylu. Podczas ogrzewania wydziela się azot i powstaje dająca się oddzielić mieszanina produktu wstawiania nitrenu i pożądanego ketoindazolu #. Ta ostatnia reakcja wydaje się być produktem typu przegrupowania Curtiusa z wytworzeniem N-izocyjanianu #, który następnie ulega cyklizacji. Alkilowanie enolu metanolanem sodu i chlorkiem 3-dimetyloaminopropylu daje benzydaminę.
Alternatywnie, zastosowanie chloroacetamidu w etapie alkilowania, po którym następuje hydroliza kwasowa, daje zamiast tego bendazac .
Badania
Badania wskazują, że benzydamina wykazuje znaczną aktywność przeciwbakteryjną in vitro , a także wykazuje synergizm w połączeniu z innymi antybiotykami, zwłaszcza tetracyklinami, przeciwko opornym na antybiotyki szczepom Staphylococcus aureus i Pseudomonas aeruginosa .
Wykazuje również pewną aktywność kannabinoidową u szczurów, ale nie był testowany na ludziach. Przypuszcza się również, że działa na receptory 5-HT2A ze względu na podobieństwo strukturalne do serotoniny.
Zobacz też
Bibliografia
Zewnętrzne linki
- „Płukanie jamy ustnej Benzydamina” . Medycyna.
- „Spray Difflam (benzydamina)” . Lekarz sieci, Wielka Brytania.
- „Tantum Verde (benzydamina)” . Carysfort Healthcare Limited, Irlandia. Zarchiwizowane od oryginału w dniu 2015-11-25.


