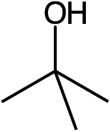
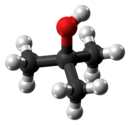
tert -Alkohol butylowy - tert-Butyl alcohol
|
|
|||

|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
2-Metylopropan-2-ol |
|||
Inne nazwy
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| 906698 | |||
| CZEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Karta informacyjna ECHA |
100.000.809 |
||
| Numer WE | |||
| 1833 | |||
| Siatka | tert-Butyl+Alkohol | ||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS | |||
| UNII | |||
| Numer ONZ | 1120 | ||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 4 H 10 O | |||
| Masa cząsteczkowa | 74,123 g·mol -1 | ||
| Wygląd zewnętrzny | Bezbarwne ciało stałe | ||
| Zapach | Kamforowy | ||
| Gęstość | 0,775 g/ml | ||
| Temperatura topnienia | 25 do 26°C; 77 do 79 ° F; 298 do 299 tys | ||
| Temperatura wrzenia | 82 do 83 °C; 179 do 181 ° F; 355 do 356 tys | ||
| mieszalny | |||
| log P | 0,584 | ||
| Ciśnienie pary | 4,1 kPa (przy 20 °C) | ||
| Kwasowość (p K a ) | 16.54 | ||
| 5,742 x 10 -5 cm 3 / mol | |||
|
Współczynnik załamania ( n D )
|
1,387 | ||
| 1.31 D | |||
| Termochemia | |||
|
Pojemność cieplna ( C )
|
215,37 J K -1 mol -1 | ||
|
Standardowa
entropia molowa ( S |
189,5 J K -1 mol -1 | ||
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-360,04 do -358,36 kJ mol -1 | ||
|
Standardowa entalpia
spalania (Δ c H ⦵ 298 ) |
−2,64479 do −2,64321 MJ mol −1 | ||
| Zagrożenia | |||
| Arkusz danych dotyczących bezpieczeństwa | inchem.org | ||
| Piktogramy GHS |
 
|
||
| Hasło ostrzegawcze GHS | Zagrożenie | ||
| H225 , H319 , H332 , H335 | |||
| P210 , P261 , P305 + 351 + 338 | |||
| NFPA 704 (ognisty diament) | |||
| Temperatura zapłonu | 11 ° C (52 ° F; 284 K) | ||
| 480 ° C (896 ° F; 753 K) | |||
| Granice wybuchowości | 2,4-8,0% | ||
| Dawka lub stężenie śmiertelne (LD, LC): | |||
|
LD 50 ( mediana dawki )
|
3559 mg/kg (królik, doustnie) 3500 mg/kg (szczur, doustnie) |
||
| NIOSH (limity ekspozycji dla zdrowia w USA): | |||
|
PEL (dopuszczalne)
|
TWA 100 ppm (300 mg/m 3 ) | ||
|
REL (zalecane)
|
TWA 100 ppm (300 mg/m 3 ) ST 150 ppm (450 mg/m 3 ) | ||
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
1600 ppm | ||
| Związki pokrewne | |||
|
Powiązane butanole
|
2-butanol |
||
|
Związki pokrewne
|
2-Metylo-2-butanol Trimetylosilanol |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
tert alkohol butylo jest najprostszym trzeciorzędowy alkohol , o wzorze o (CH 3 ) 3 COH (czasami przedstawiony w t -BuOH). Jest to jeden z czterech izomerów w butanolu . Alkohol tert-butylowy to bezbarwne ciało stałe, które topi się w pobliżu temperatury pokojowej i mazapach podobny do kamfory . Jest mieszalny z wodą , etanolem i eterem dietylowym .
Naturalne występowanie
Alkohol tert-butylowy został zidentyfikowany w piwie i ciecierzycy . Występuje również w manioku , który jest używany jako składnik fermentacji w niektórych napojach alkoholowych .
Przygotowanie
Alkohol tert-butylowy jest komercyjnie otrzymywany z izobutanu jako współproduktu produkcji tlenku propylenu . Może być również wytwarzany przez katalityczną hydratacji z izobutenu , lub przez reakcję Grignarda pomiędzy acetonu i chlorku metylomagnezowego .
Oczyszczania nie można przeprowadzić przez prostą destylację ze względu na tworzenie azeotropu z wodą, chociaż wstępne suszenie rozpuszczalnika zawierającego duże ilości wody przeprowadza się przez dodanie benzenu z wytworzeniem trzeciorzędowego azeotropu i oddestylowanie wody. Mniejsza ilość wody usuwa się poprzez suszenie z tlenku wapnia (CaO), węglanu potasu (K 2 CO 3 ), siarczan wapnia (CaSO 4 ), i siarczan magnezu (MgSO 4 ), a następnie destylacji frakcjonowanej. Bezwodny alkohol tert - butylowy otrzymuje się przez dalsze ogrzewanie w temperaturze wrzenia i destylację z magnezu aktywowanego jodem lub metali alkalicznych, takich jak sód lub potas. Inne sposoby obejmują zastosowanie 4 nm sitach molekularnych , aluminium tert -butylate , wodorek wapnia (CaH 2 ) lub krystalizacji frakcyjnej, w obojętnej atmosferze.
Aplikacje
tert- alkohol-butylu stosuje się jako rozpuszczalnik, etanol denaturującego , zmywających składnika i benzyna oktan zasilającą i związków tlenowych . Jest to związek chemiczny, produkt pośredni stosowany do wytwarzania metylo -tert -butylowego (MTBE) i octan tert -butylowym (ETBE) przez reakcję z metanolem i etanolem , odpowiednio, i tert -butylu (TBHP) na drodze reakcji z nadtlenkiem wodoru .
Reakcje
Jako alkohol trzeciorzędowy, alkohol tert - butylowy jest bardziej odporny na utlenianie niż inne izomery butanolu.
Alkohol tert-butylowy deprotonuje się silną zasadą, otrzymując alkoholan . Szczególnie często występuje potasowy t -butoksylan , który wytwarza się przez traktowanie tert -butanolu z potasu metalu.
- K + t -BuOH → t -BuO − K + + 1/2 H 2
Tert -butanolanu jest silny, nie- nukleofilowej zasady w chemii organicznej. Łatwo abstracts kwasowe protony z podłoża, lecz jego stearynowy luzem hamuje grupę udziału w reakcji podstawienia nukleofilowego , taką jak w Williamson eter syntezy lub S N 2 reakcji.
tert -Butylo alkohol reaguje z roztworem chlorowodoru , z wytworzeniem tert -butyl chlorek .
O-chlorowanie alkoholu tert-butylowego kwasem podchlorawym w celu otrzymania podchlorynu tert-butylu :
- (CH 3 ) 3 COH + HOCl → (CH 3 ) 3 COCl + H 2 O
Farmakologia i toksykologia
Istnieją ograniczone dane dotyczące farmakologii i toksykologii tert-butanolu u ludzi i innych zwierząt. Narażenie ludzi może wystąpić z powodu metabolizmu tlenu w paliwie. Tert-butanol słabo wchłania się przez skórę, ale szybko wchłania się w przypadku wdychania lub połknięcia. Tert-butanol działa drażniąco na skórę lub oczy. Toksyczność pojedynczych dawek jest zwykle niska, ale duże dawki mogą powodować działanie uspokajające lub znieczulające.
Uwagi
Bibliografia
Zewnętrzne linki
- Międzynarodowa Karta Bezpieczeństwa Chemicznego 0114
- Kieszonkowy przewodnik NIOSH dotyczący zagrożeń chemicznych. „#0078” . Narodowy Instytut Bezpieczeństwa i Higieny Pracy (NIOSH).
- Kryteria zdrowia środowiskowego IPCS 65: Butanole: cztery izomery
- Poradnik BHP 7 IPCS : tert- butanol