Jodek talu (I) - Thallium(I) iodide
|
|
| Nazwy | |
|---|---|
| Inne nazwy
Jodek talu Jodek
thallousa |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.029.272 |
|
PubChem CID
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| TlI | |
| Masa cząsteczkowa | 331,287 g / mol |
| Wygląd | żółte kryształy |
| Gęstość | 7,1 g / cm 3 |
| Temperatura topnienia | 441,7 ° C (827,1 ° F; 714,8 K) |
| Temperatura wrzenia | 824 ° C (1515 ° F; 1097 K) |
| 0,085 g / l (25 ° C) | |
| Rozpuszczalność | nierozpuszczalny w alkoholu |
| -82,2 · 10-6 cm 3 / mol | |
| Zagrożenia | |
|
Klasyfikacja UE (DSD) (nieaktualne)
|
Bardzo toksyczny ( T + ) Niebezpieczny dla środowiska ( N ) |
| Zwroty R (nieaktualne) | R26 / 28 , R33 , R51 / 53 |
| Zwroty S (nieaktualne) | (S1 / 2) , S13 , S28 , S45 , S61 |
| Temperatura zapłonu | Nie palne |
| Związki pokrewne | |
|
Inne aniony
|
Fluorek talu (I) Chlorek talu (I) Bromek talu (I) |
|
Inne kationy
|
Jodek galu (I) Jodek indu (I) |
|
Związki pokrewne
|
Jodek rtęci (II) Jodek ołowiu (II) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Jodek talu (I) jest związkiem chemicznym o wzorze TlI . Jest to niezwykłe jest jednym z kilku metali nierozpuszczalnych w wodzie jodek , wraz z Agi , Cul , Sni 2 , Sni 4 , pBI 2 i HGI 2 .
Chemia
Tli może być utworzony w roztworze wodnym przez metatezę z każdej rozpuszczalnej soli talu z jonu jodkowego. Tworzy się również jako produkt uboczny w jodowaniu fenoli za pomocą octanu talu (I) za pomocą promowanego talem.
Próby utlenienia tli się talu (III), jodek niepowodzeniem, ponieważ utlenianie produkuje talu (I), trijodek , Tl + I 3 - .
Właściwości fizyczne
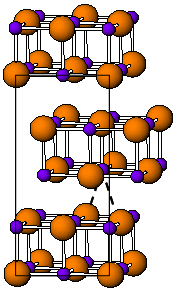
Postać TlI w temperaturze pokojowej jest żółta i ma strukturę rombową , którą można uznać za zniekształconą strukturę NaCl. Uważa się, że zniekształcona struktura jest spowodowana korzystnymi interakcjami tal-tal, najbliższa odległość Tl-Tl wynosi 383 µm. W 175 ° C żółta postać przechodzi w czerwoną postać CsCl . Temu przejściu fazowemu towarzyszy skok przewodnictwa elektrycznego o około dwa rzędy wielkości. Strukturę CsI można ustabilizować do temperatury pokojowej poprzez domieszkowanie TlI innymi halogenkami, takimi jak RbI, CsI, KI, AgI, TlBr i TlCl. Zatem obecność zanieczyszczeń może być odpowiedzialna za współistnienie sześciennej i ortorombowej fazy TlI w warunkach otoczenia. Pod wysokim ciśnieniem, 160 kbar, TlI staje się przewodnikiem metalicznym. Nanometrów cienkie tli folie hodowane w LiF, NaCl lub podłoży KBr wykazuje sześcienne RockSalt strukturę.
Aplikacje
Jodek talu (I) jest dodawany do lamp rtęciowych w celu poprawy ich wydajności. Wytwarzane światło znajduje się głównie w niebiesko-zielonej części widma światła widzialnego, najmniej pochłanianego przez wodę, dlatego te lampy były używane do oświetlenia podwodnego. Jodek talu (I) jest również stosowany w śladowych ilościach z NaI lub CsI do produkcji scyntylatorów stosowanych w detektorach promieniowania.
Występowanie naturalne
Naturalny jodek talu (I) został odkryty dopiero niedawno, jako rombowy polimorf zwany nataliyamalikite. Jest pochodzenia fumarolowego.
Bezpieczeństwo
Jak wszystkie związki talu, jodek talu (I) jest silnie toksyczny.
Bibliografia
Cytowane źródła
- Haynes, William M., wyd. (2011). Podręcznik chemii i fizyki CRC (wyd. 92). Boca Raton, FL: CRC Press . ISBN 1439855110 .
