Cyna - Tin
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cyna | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Alotropy | alfa, α (szary) ; beta, β (biały) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd zewnętrzny | srebrzystobiały (beta, β) lub szary (alfa, α) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Średnia masa atomowa R STD (Sn) | 118.710(7) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cyna w układzie okresowym | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liczba atomowa ( Z ) | 50 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupa | grupa 14 (grupa węglowa) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Okres | okres 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | p-blok | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konfiguracja elektronów | [ Kr ] 4d 10 5s 2 5p 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrony na powłokę | 2, 8, 18, 18, 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości fizyczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Faza w STP | solidny | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura topnienia | 505,08 K (231,93 °C, 449,47 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura wrzenia | 2875 K (2602 ° C, 4716 ° F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gęstość (w pobliżu rt ) | biały, β: 7,265 g/cm 3 szary, α: 5,769 g/cm 3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| w stanie ciekłym (przy mp ) | 6,99 g / cm 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ciepło stapiania | biały, β: 7,03 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ciepło parowania | biały, β: 296,1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molowa pojemność cieplna | biały, β: 27,112 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ciśnienie pary
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości atomowe | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stany utleniania | -4 , -3, -2, -1, 0, +1, +2 , +3, +4 ( tlenek amfoteryczny ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroujemność | Skala Paulinga: 1,96 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energie jonizacji | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Promień atomowy | empiryczny: 140 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Promień kowalencyjny | 139±4 po południu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Promień Van der Waalsa | 217 po południu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Linie widmowe cyny | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inne właściwości | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Naturalne występowanie | pierwotny | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struktura krystaliczna | Ciało skoncentrowane czworokątny
biały (β) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struktura krystaliczna | face-centered cubic diamentu
szary (α) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prędkość dźwięku cienki pręt | 2730 m/s (w temperaturze pokojowej ) (walcowane) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozszerzalność termiczna | 22,0 µm/(m⋅K) (przy 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Przewodność cieplna | 66,8 W/(m⋅K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rezystancja | 115 nΩ⋅m (przy 0°C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Zamawianie magnetyczne | szary: diamagnetyczny biały (β): paramagnetyczny |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molowa podatność magnetyczna | (biały) +3,1 × 10 -6 cm 3 /mol (298 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moduł Younga | 50 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moduł ścinania | 18 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moduł objętościowy | 58 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Współczynnik Poissona | 0,36 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Twardość Brinella | 50–440 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | 7440-31-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Historia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Odkrycie | około 35 wieku p.n.e. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Symbol | „Sn”: od łacińskiego stannum | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Główne izotopy cyny | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Cyna to pierwiastek chemiczny o symbolu Sn (z łac . stannum ) i liczbie atomowej 50. Cyna to srebrzysty metal, który ma charakterystyczny bladożółty odcień.
Cyna jest na tyle miękka, że można ją ciąć przy użyciu niewielkiej siły. Kiedy sztabka cyny jest wyginana, w wyniku bliźniaczych kryształów cyny słychać tak zwany „ krzyk cyny ” ; cecha ta jest wspólna dla indu , kadmu , cynku i mrożonej rtęci .
Czysta cyna po zestaleniu ma lustrzany wygląd podobny do większości metali. W większości stopów cyny (takich jak cyna ) metal zestala się na matowoszary kolor.
Cyna jest metalem po transformacji w grupy 14 do okresowego pierwiastków . Otrzymuje się go głównie z mineralnych kasyteryt , który zawiera tlenek cynowy , SnO
2. Cyna wykazuje podobieństwo chemiczne do obu swoich sąsiadów z grupy 14, germanu i ołowiu , i ma dwa główne stopnie utlenienia , +2 i nieco stabilniejszy +4. Cyna jest 49. najobficiej występującym pierwiastkiem na Ziemi i ma, z 10 stabilnymi izotopami, największą liczbę stabilnych izotopów w układzie okresowym, dzięki swojej magicznej liczbie protonów.
Ma dwa główne alotropy : w temperaturze pokojowej stabilny alotrop to β-cyna, srebrzystobiały, plastyczny metal; w niskich temperaturach jest mniej gęstą szarą cyną α, która ma strukturę sześcienną diamentu . Cyna metaliczna nie utlenia się łatwo w powietrzu.
Pierwszy stop cyny wykorzystywane na dużą skalę z brązu , z 1 / 8 cyny i 7 / 8 miedzi , od roku 3000 przed naszą erą. Po 600 rpne wyprodukowano czystą metaliczną cynę. Cyna , która jest stopem 85-90% cyny z pozostałością zwykle składającą się z miedzi , antymonu i ołowiu , była używana do produkcji sztućców od epoki brązu do XX wieku. W dzisiejszych czasach cynę stosuje się w wielu stopach, w szczególności w miękkich lutach cynowo-ołowiowych , które zazwyczaj zawierają 60% lub więcej cyny, oraz w produkcji przezroczystych, przewodzących elektrycznie warstw tlenku indu i cyny w zastosowaniach optoelektronicznych . Kolejna duża aplikacja jest korozja oporny cynowanie od stali . Ze względu na niską toksyczność cyny nieorganicznej, stal cynowana jest szeroko stosowana do pakowania żywności jako puszki cynowe . Niektóre związki cynoorganiczne mogą być bardzo toksyczne.
Charakterystyka
Fizyczny

Cyna jest miękkim, plastycznym , ciągliwym i wysoce krystalicznym srebrzystobiałym metalem . Kiedy bar cyny jest wygięta trzaski dźwięku znany jako „ cyny okrzykiem ” można usłyszeć od bliźniaczych kryształów. Cyna topi się w około 232°C (450°F), najniżej w grupie 14. Temperatura topnienia jest dalej obniżana do 177,3°C (351,1°F) dla cząstek 11 nm.
| Wideo zewnętrzne | |
|---|---|
|
|
β-cyna, forma metaliczna lub biała cyna, ma strukturę BCT i jest stabilna w temperaturze pokojowej i wyższej oraz jest ciągliwa. α-cyna, postać niemetaliczna lub szara cyna, jest stabilna poniżej 13,2 ° C (55,8 ° F) i jest krucha . α-cyna ma strukturę sześciennego kryształu diamentu , zbliżoną do diamentu , krzemu czy germanu . α-cyna nie ma właściwości metalicznych, ponieważ jej atomy tworzą strukturę kowalencyjną , w której elektrony nie mogą się swobodnie poruszać. α-cyna to matowoszary sproszkowany materiał, który nie ma typowych zastosowań poza specjalistycznymi zastosowaniami półprzewodnikowymi . γ-cyna i σ-cyna występują w temperaturach powyżej 161 °C (322 °F) i ciśnieniach powyżej kilku GPa .
W zimnych warunkach β-cyna ma tendencję do spontanicznego przekształcania się w α-cynę, zjawisko znane jako „ szkodnik cynowy ” lub „choroba cynowa”. Niektóre źródła mówią nieweryfikowalne również, że podczas Napoleona "rosyjskiej kampanii s 1812, temperatura była tak zimna, że przyciski cyny na żołnierskich mundurach rozpadła się w czasie, przyczyniając się do porażki Grande Armée , trwałe legendy.
Temperatura przemiany α-β wynosi 13,2 °C (55,8 °F), ale zanieczyszczenia (np. Al, Zn, itp.) obniżają ją znacznie poniżej 0 °C (32 °F). Po dodaniu antymonu lub bizmutu przemiana może w ogóle nie nastąpić, zwiększając trwałość.
Komercyjne gatunki cyny (zawartość 99,8% cyny) są odporne na przemianę ze względu na hamujące działanie niewielkich ilości bizmutu, antymonu, ołowiu i srebra obecnych jako zanieczyszczenia. Pierwiastki stopowe takie jak miedź, antymon, bizmut, kadm i srebro zwiększają twardość cyny. Cyna łatwo tworzy twarde, kruche fazy międzymetaliczne, które są zazwyczaj niepożądane. Nie miesza się w roztworze z większością metali i pierwiastków, więc cyna nie ma zbyt dużej rozpuszczalności w stanie stałym. Cyna dobrze miesza się z bizmutem , galem , ołowiem , talem i cynkiem tworząc proste układy eutektyczne .
Cyna staje się nadprzewodnikiem poniżej 3,72 K i była jednym z pierwszych badanych nadprzewodników. Efekt Meissnera , jedna z charakterystycznych cech nadprzewodników, została po raz pierwszy odkryta w nadprzewodzących kryształach cyny.
Chemiczny
Cyna jest odporna na korozję powodowaną przez wodę , ale może być korodowana przez kwasy i zasady . Cyna może być wysoko polerowana i służy jako powłoka ochronna dla innych metali, ochronna warstwa tlenku ( pasywacja ) zapobiega dalszemu utlenianiu. Cyna działa jak katalizator, wyzwalając reakcję chemiczną roztworu zawierającego tlen i pomaga zwiększyć szybkość zachodzącej reakcji chemicznej.
Izotopy
Cyna ma dziesięć stabilnych izotopów , najwięcej spośród wszystkich pierwiastków. Izotopy cyny mają masy atomowe 112, 114, 115, 116, 117, 118, 119, 120, 122 i 124. 120 Sn stanowi prawie jedną trzecią wszystkich izotopów; 118 Sn i 116 Sn są również powszechne, podczas gdy 115 Sn jest najmniej powszechnym stabilnym izotopem. Izotopy o parzystych liczbach masowych nie mają spinu jądrowego , podczas gdy te o nieparzystych liczbach masowych mają spin +1/2. Cyna jest jednym z najłatwiejszych pierwiastków do wykrycia i analizy za pomocą spektroskopii NMR, która opiera się na masie cząsteczkowej, a jej przesunięcia chemiczne są odnoszone do SnMe
4. Uważa się, że duża liczba stabilnych izotopów jest bezpośrednim wynikiem posiadania przez cynę liczby atomowej 50, „ magicznej liczby ” w fizyce jądrowej.
Cyna ma 31 niestabilnych izotopów, których liczba masowa wynosi od 99 do 139. Niestabilne izotopy cyny mają okres półtrwania krótszy niż rok, z wyjątkiem 126 Sn, którego okres półtrwania wynosi 230 000 lat. 100 Sn i 132 Sn to dwa z nielicznych nuklidów z „ podwójnie magicznym ” jądrem, które pomimo niestabilności, ponieważ mają bardzo nierówne stosunki neutron-proton , są punktami końcowymi, poza którymi izotopy cyny lżejsze niż 100 Sn i cięższe niż 132 Sn są znacznie mniej stabilny. Kolejnych 30 metastabilnych izomerów zidentyfikowano dla izotopów cyny między 111 a 131, z których najbardziej stabilnym jest 121 m Sn , z okresem półtrwania 43,9 lat.
Względne różnice w liczbie stabilnych izotopów cyny można wytłumaczyć sposobem ich powstawania podczas gwiezdnej nukleosyntezy . 116 Sn przez 120 Sn są utworzone w Ś -Process (powolne wychwytywanie neutronów), w większości gwiazdek , który prowadzi do nich jest najczęstszą izotopy cyny, a 122 Sn i 124 Sn powstają tylko w r -Process (szybkie wychwytywanie neutronów) w supernowych i są mniej powszechne. W procesie r wytwarzane są również izotopy cyny od 117 Sn do 120 Sn . 112 Sn, 114 Sn i 115 Sn nie mogą być wytworzone w znaczących ilościach w procesach s - lub r - i należą do jąder p, których pochodzenie nie jest dobrze poznane. Kilka pomysłów dla ich formowania obejmują wychwytywania protonów i fotodezintegracja , 115 Sn może być częściowo produkowane w s -Process zarówno bezpośrednio, jak i córki długotrwałymi 115 W .
Etymologia
Słowo tin jest wspólne dla języków germańskich i można je prześledzić wstecz do zrekonstruowanego protogermańskiego * tin-om ; pokrewne to niemiecki Zinn , szwedzki tenn i holenderska cyna . Nie występuje w innych gałęziach indoeuropejskiego , z wyjątkiem zapożyczenia z germańskiego (np. irlandzki tinne z angielskiego).
Łacińska nazwa stannum pierwotnie oznaczało stopu srebra i ołowiu, a przyszedł oznacza „puszkę” w 4 wieku-na wcześniej łacińskiego słowa było Plumbum candidum lub „white lead”. Stannum najwyraźniej pochodzi od wcześniejszego stagnum (oznaczającego tę samą substancję), pochodzenia romańskiego i celtyckiego określenia cyny . Pochodzenie stannum / stagnum jest nieznane; może być przed- indoeuropejskich .
Meyers Konversations-Lexikon sugeruje natomiast, że stannum pochodzi z Kornwalii stean i dowody, że Cornwall w pierwszych wiekach naszej ery był głównym źródłem cyny.
Historia

Wydobycie i stosowanie cyny można datować na początki epoki brązu około 3000 roku p.n.e., kiedy to zaobserwowano, że wyroby miedziane powstałe z rud polimetalicznych o różnej zawartości metali mają różne właściwości fizyczne. Najwcześniejsze przedmioty z brązu zawierały mniej niż 2% cyny lub arsenu i uważa się, że są one wynikiem niezamierzonego stopowania z powodu zawartości metali śladowych w rudzie miedzi. Dodanie drugiego metalu do miedzi zwiększa jej twardość, obniża temperaturę topnienia i poprawia proces odlewania , wytwarzając bardziej płynny stop, który chłodzi się do gęstszego, mniej gąbczastego metalu. Była to ważna innowacja, która pozwoliła na znacznie bardziej złożone kształty odlewane w zamkniętych formach z epoki brązu. Obiekty z brązu arsenowego pojawiają się najpierw na Bliskim Wschodzie, gdzie arsen jest powszechnie spotykany z rudą miedzi, ale szybko zdano sobie sprawę z zagrożenia dla zdrowia, a poszukiwania źródeł znacznie mniej niebezpiecznych rud cyny rozpoczęły się na początku epoki brązu. Stworzyło to zapotrzebowanie na rzadki metal cynowy i utworzyło sieć handlową, która połączyła odległe źródła cyny z rynkami kultur epoki brązu.
Kasyteryt ( SnO
2), tlenkowa forma cyny, była najprawdopodobniej pierwotnym źródłem cyny. Inne rudy cyny są mniej powszechnymi siarczkami, takimi jak stannit, które wymagają bardziej skomplikowanego procesu wytapiania . Kasyteryt często gromadzi się w kanałach aluwialnych jako osady podkładowe, ponieważ jest twardszy, cięższy i bardziej odporny chemicznie niż towarzyszący mu granit . Kasyteryt ma zwykle czarny lub ciemny kolor, a osady te można łatwo dostrzec na brzegach rzek . Przypadkowo osady aluwialne ( placer ) mogły być zbierane i oddzielane metodami podobnymi do płukania złota .
Związki i chemia
W zdecydowanej większości swoich związków cyna ma stopień utlenienia II lub IV.
Związki nieorganiczne
Związki halogenków są znane z obu stopni utlenienia. SN (IV) wszystkie cztery halogenki, są dobrze znane w SNF 4 , SnCl 4 , SnBr 4 i Sni 4 . Trzy cięższe składniki to lotne związki molekularne, podczas gdy tetrafluorek jest polimerem. Wszystkie cztery halogenki są również znane dla Sn(II): SnF 2 , SnCl
2, SnBr 2 i Sni 2 . Wszystkie są polimerowymi ciałami stałymi. Spośród tych ośmiu związków tylko jodki są zabarwione.
Chlorek cyny(II) (znany również jako chlorek cynawy) jest najważniejszym handlowym halogenkiem cyny. Ilustrując drogi do takich związków, chlor reaguje z metaliczną cyną, dając SnCl 4, podczas gdy reakcja kwasu solnego i cyny wytwarza SnCl
2i gazowy wodór. Alternatywnie SnCl 4 Sn łączą się chlorkiem cyny w procesie zwanym comproportionation :
- SnCl 4 + Sn → 2 SnCl
2
Cyna może tworzyć wiele tlenków, siarczków i innych pochodnych chalkogenków . Dwutlenek Sn)
2(kasyteryt) powstaje, gdy cyna jest podgrzewana w obecności powietrza . Sn)
2jest amfoteryczny , co oznacza, że rozpuszcza się zarówno w roztworach kwaśnych, jak i zasadowych. Cyniany o strukturze [ Sn(OH)
6] 2− , jak K
2[ Sn(OH)
6], są również znane, chociaż wolny kwas cynowy H
2[ Sn(OH)
6] jest nieznany.
Siarczki cyny występują na obu stopniach utlenienia +2 i +4: siarczek cyny(II) i siarczek cyny(IV) ( złoto mozaikowe ).
Wodorki
Stannan ( SnH
4), z cyną na stopniu utlenienia +4, jest niestabilny. Wodorki cynoorganiczne są jednak dobrze znane, na przykład wodorek tributylocyny (Sn (C 4 H 9 ) 3 H). Związki te uwalniają przejściowe rodniki tributylocyny , które są rzadkimi przykładami związków cyny(III).
Związki cynoorganiczne
Związki cynoorganiczne , czasami nazywane stannanami, są związkami chemicznymi z wiązaniami cyna-węgiel. Spośród związków cyny najbardziej użyteczne handlowo są pochodne organiczne. Niektóre związki cynoorganiczne są wysoce toksyczne i są stosowane jako biocydy . Pierwszy związek cynoorganiczny należy uwzględnić to diethyltin dijodku ((C 2 H 5 ) 2 Sni 2 ), wyrażone w Edward Frankland 1849.
Większość związków cynoorganicznych to bezbarwne ciecze lub ciała stałe, które są odporne na powietrze i wodę. Przyjmują geometrię czworościenną. Związki tetraalkilo- i tetraarylocyny można wytworzyć przy użyciu odczynników Grignarda :
-
SnCl
4+ 4 RMgBr → R
4Sn + 4 MgBrCl
Mieszane halogenki-alkile, które są bardziej powszechne i ważniejsze komercyjnie niż pochodne tetraorganiczne, wytwarza się w reakcjach redystrybucji :
-
SnCl
4+ R
4Sn → 2 SnCl
2R 2
Związki dwuwartościowy cynoorganiczne są rzadkie, jednak częściej niż powiązanej dwuwartościowych organogermanium i krzemoorganiczne związki. Większa stabilizacja Sn(II) przypisywana jest „ efektowi pary inercyjnej ”. Cyny (II), związki obejmują oba stannylenes (wzór: R 2 Sn, jak widać na singlet karbenów ) i distannylenes (R 4 Sn 2 ), które są w przybliżeniu równoważne alkenów . Obie klasy wykazują niezwykłe reakcje.
Występowanie

Cyna jest generowany poprzez LONG s -Process w niskiej do średniej masy gwiazdek (o masie od 0,6 do 10 razy większą od Sun ) i wreszcie rozpadu beta ciężkiego izotopów indu .
Cyna jest 49. najobficiej występującym pierwiastkiem w skorupie ziemskiej , stanowiąc 2 ppm w porównaniu z 75 ppm dla cynku, 50 ppm dla miedzi i 14 ppm dla ołowiu.
Cyna nie występuje jako pierwiastek rodzimy, ale musi być wydobywana z różnych rud. Kasyteryt ( SnO
2) jest jedynym ważnym komercyjnie źródłem cyny, chociaż niewielkie ilości cyny są odzyskiwane ze złożonych siarczków, takich jak stannit , cylindrycznyt , franckeit , kanfieldit i teallit . Minerały z cyną prawie zawsze kojarzą się ze skałą granitową , zwykle na poziomie 1% zawartości tlenku cyny.
Ze względu na wyższy ciężar właściwy dwutlenku cyny, około 80% wydobytej cyny pochodzi z wtórnych osadów znajdujących się poniżej złóż pierwotnych. Cyna jest często odzyskiwana z granulek spłukiwanych w przeszłości i osadzanych w dolinach lub w morzu. Najbardziej ekonomiczne sposoby wydobywania cyny to pogłębianie , hydraulika lub odkrywki . Większość światowych cyny jest produkowany z pakowacz depozytów, które mogą zawierać jak najmniej 0,015% cyny.
| Kraj | Rezerwy |
|---|---|
|
|
1 500 000 |
|
|
250 000 |
|
|
310 000 |
|
|
800 000 |
|
|
590.000 |
|
|
400 000 |
|
|
350 000 |
|
|
180 000 |
|
|
170 000 |
| Inne | 180 000 |
| Całkowity | 4 800 000 |
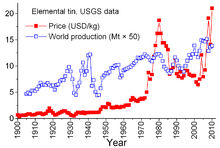
W 2011 roku wydobyto około 253 000 ton cyny, głównie w Chinach (110 000 t), Indonezji (51 000 t), Peru (34 600 t), Boliwii (20 700 t) i Brazylii (12 000 t). Szacunki dotyczące produkcji cyny historycznie różniły się w zależności od rynku i technologii wydobycia. Szacuje się, że przy obecnych wskaźnikach zużycia i technologiach, za 40 lat na Ziemi zabraknie cyny nadającej się do wydobycia. W 2006 r. Lester Brown zasugerował, że cyna może się wyczerpać w ciągu 20 lat, opierając się na ostrożnych szacunkach 2% rocznego wzrostu.
| Rok | Miliony ton |
|---|---|
| 1965 | 4265 |
| 1970 | 3930 |
| 1975 | 9060 |
| 1980 | 9100 |
| 1985 | 3060 |
| 1990 | 7100 |
| 2000 | 7100 |
| 2010 | 5200 |
Złom jest ważnym źródłem metalu. Odzysk cyny poprzez recykling szybko rośnie. Podczas gdy Stany Zjednoczone nie wydobywały (od 1993 r.) ani nie wytapiały (od 1989 r.) cyny, były największym producentem wtórnym, przetwarzając prawie 14 000 ton w 2006 r.
Odnotowano nowe złoża w Mongolii , aw 2009 r. odkryto nowe złoża cyny w Kolumbii.
Produkcja
Cyna jest wytwarzany karbotermicznej redukcji tlenku rudy z węgla lub koksu. Można stosować zarówno piec rewerberacyjny, jak i piec elektryczny .
Górnictwo i hutnictwo
Przemysł
Dziesięć największych firm wyprodukowało większość światowej cyny w 2007 roku.
Większość światowej cyny jest sprzedawana na LME, z 8 krajów, pod 17 markami.
| Spółka | Ustrój | 2006 | 2007 | 2017 | 2006-2017 % zmiana |
|---|---|---|---|---|---|
| Yunnan Tin | Chiny | 52 339 | 61,129 | 74 500 | 42,3 |
| PT Timah | Indonezja | 44 689 | 58,325 | 30 200 | -32.4 |
| Malezja Smelting Corp | Malezja | 22.850 | 25 471 | 27 200 | 19,0 |
| Yunnan Chengfeng | Chiny | 21.765 | 18 000 | 26 800 | 23,1 |
| Minsur | Peru | 40,977 | 35 940 | 18 000 | -56,1 |
| EM Vinto | Boliwia | 11 804 | 9448 | 12.600 | 6,7 |
| Guangxi Chiny cyna | Chiny | / | / | 11500 | / |
| Thaisarco | Tajlandia | 27 828 | 19 826 | 10600 | -61,9 |
| Metallo-Chimique | Belgia | 8049 | 8372 | 9700 | 20,5 |
| Gejiu Zi Li | Chiny | / | / | 8700 | / |
Międzynarodowa Rada Cyny powstała w 1947 roku, aby kontrolować ceny cyny. Upadł w 1985 r. W 1984 r. utworzono Stowarzyszenie Krajów Produkujących Cynę , którego członkami są Australia, Boliwia, Indonezja, Malezja, Nigeria, Tajlandia i Zair.
Cena i wymiany
Cyna jest wyjątkowa wśród surowców mineralnych ze względu na złożone umowy między krajami produkującymi a krajami konsumenckimi, datowane na 1921 r. Wcześniejsze umowy miały raczej charakter nieformalny i doprowadziły do „Pierwszej międzynarodowej umowy cynowej” w 1956 r., pierwszej z serii, która skutecznie upadła. w 1985 r. Dzięki tym umowom Międzynarodowa Rada ds. Cyny (ITC) miała znaczący wpływ na ceny cyny. ITC wspierała cenę cyny w okresach niskich cen, kupując cynę do swojego zapasu buforowego i była w stanie powstrzymać cenę w okresach wysokich cen, sprzedając ją z zapasów. Było to podejście antywolnorynkowe, mające zapewnić wystarczający przepływ cyny do krajów konsumenckich i zysk dla krajów producenckich. Jednak zapasy buforowe nie były wystarczająco duże i przez większość tych 29 lat ceny cyny rosły, czasami gwałtownie, zwłaszcza w latach 1973-1980, kiedy szalejąca inflacja nękała wiele gospodarek światowych.
Pod koniec lat siedemdziesiątych i na początku osiemdziesiątych Stany Zjednoczone zmniejszyły swoje strategiczne zapasy cyny, częściowo po to, by wykorzystać historycznie wysokie ceny cyny. 1981/82 recesja zniszczony przemysł cyny. Zużycie cyny dramatycznie spadło. ITC udało się uniknąć naprawdę gwałtownych spadków dzięki przyspieszonemu zakupowi dla swojego zapasu buforowego; działalność ta wymagała rozległych pożyczek. ITC kontynuowało zaciąganie pożyczek aż do końca 1985 r., kiedy osiągnął limit kredytowy. Natychmiast nastąpił poważny „kryzys cynowy” — cyna została wycofana z obrotu na Londyńskiej Giełdzie Metali na około trzy lata. wkrótce potem się rozpuścił, a cena cyny, obecnie w warunkach wolnorynkowych, spadła do 4 dolarów za funt i utrzymywała się na tym poziomie do lat 90. XX wieku. Cena ponownie wzrosła do 2010 r. wraz z odbiciem konsumpcji po kryzysie gospodarczym 2007-2008 , towarzyszącemu uzupełnianiu zapasów i ciągłemu wzrostowi konsumpcji.
Londyńska Giełda Metali (LME) jest głównym miejscem handlu cyny. Inne rynki kontraktów cynowych to rynek cyny w Kuala Lumpur (KLTM) i indonezyjska giełda cyny (INATIN).
Cena za kg na lata:
| 2008 | 2009 | 2010 | 2011 | 2012 | |
|---|---|---|---|---|---|
| Cena | 18,51 | 13.57 | 20.41 | 26.05 | 21.13 |
Aplikacje
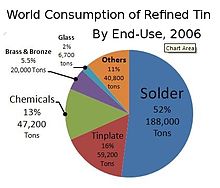
W 2018 roku prawie połowa całej wyprodukowanej cyny była wykorzystywana do lutowania. Reszta została podzielona między cynowanie, chemikalia do cyny, mosiądz i stopy brązu oraz zastosowania niszowe.
Lutować
Cyna jest od dawna stosowana w stopach z ołowiem jako lutem , w ilościach od 5 do 70% wag. Cyna z ołowiem tworzy mieszankę eutektyczną o udziale wagowym 61,9% cyny i 38,1% ołowiu (proporcja atomowa 73,9% cyny i 26,1% ołowiu) o temperaturze topnienia 183°C (361,4°F). Takie luty stosuje się przede wszystkim do łączenia rur lub obwodów elektrycznych . Od momentu wejścia w życie 1 lipca 2006 r. dyrektywy Unii Europejskiej w sprawie zużytego sprzętu elektrycznego i elektronicznego ( dyrektywa WEEE) oraz dyrektywy w sprawie ograniczenia stosowania substancji niebezpiecznych , zawartość ołowiu w takich stopach spadła. Podczas gdy narażenie na ołów wiąże się z poważnymi problemami zdrowotnymi , lut bezołowiowy nie jest pozbawiony wyzwań, w tym wyższej temperatury topnienia i tworzenia wąsów cyny, które powodują problemy elektryczne. W lutowiach bezołowiowych może wystąpić szkodnik cyny , co prowadzi do utraty połączenia lutowanego. Znaleziono stopy zastępcze, ale problemy z integralnością złącza pozostają.
Cynowanie

Cyna łatwo łączy się z żelazem i jest używana do powlekania ołowiu , cynku i stali w celu zapobiegania korozji. Pojemniki ze stali powlekanej cyną są szeroko stosowane do konserwacji żywności , co stanowi dużą część rynku cyny metalicznej. Puszka z blachy cynowej do przechowywania żywności została po raz pierwszy wyprodukowana w Londynie w 1812 roku. Osoby mówiące w brytyjskim języku angielskim nazywają je „puszkami”, podczas gdy osoby mówiące w amerykańskim angielskim nazywają je „ puszkami ” lub „puszkami”. Jednym z wyprowadzeń takiego użycia jest slangowe określenie „ tinnie ” lub „tinny”, co w Australii oznacza „puszka piwa” . Cyny gwizdek jest tak nazywane, ponieważ jest masowo produkowany najpierw cynowanej stali. Miedziane naczynia kuchenne, takie jak rondle i patelnie, są często wyłożone cienką warstwą cyny , ponieważ połączenie kwaśnych potraw z miedzią może być toksyczne.
Stopy specjalistyczne
Cyna w połączeniu z innymi pierwiastkami tworzy szeroką gamę użytecznych stopów. Cyna jest najczęściej stapiana z miedzią. Cyna zawiera 85-99% cyny; metal łożyskowy ma również wysoki procent cyny. Brąz to głównie miedź z 12% cyną, natomiast dodatek fosforu daje brąz fosforowy . Metal dzwonowy jest również stopem miedzi z cyną, zawierającym 22% cyny. Cyna była czasami używana w monetach; kiedyś tworzył jednocyfrowy procent (zwykle pięć procent lub mniej) pensów amerykańskich i kanadyjskich. Ponieważ często głównym metalem w takich monetach jest miedź, w tym czasami cynk, można je nazwać brązem lub stopami mosiądzu.
Niobu -tin związku Nb 3 Sn są przemysłowo stosowane w artykułach cewek z nadprzewodzących magnesów o wysokiej temperaturze krytycznej (18 K) i krytycznego pola magnetycznego (25 T ). Magnes nadprzewodzący ważący zaledwie dwa kilogramy jest w stanie wytworzyć pole magnetyczne konwencjonalnego elektromagnesu ważącego tony.
Niewielki procent cyny dodaje się do stopów cyrkonu do platerowania paliwa jądrowego.
Większość metalowych piszczałek w organach piszczałkowych jest wykonana ze stopu cyny i ołowiu, przy czym najczęstszym składem jest 50/50. Proporcja cyny w piszczałce określa jej ton, ponieważ cyna ma pożądany rezonans tonalny. Gdy stop cyny/ołowiu ochładza się, faza ołowiu najpierw zestala się, a po osiągnięciu temperatury eutektycznej pozostała ciecz tworzy warstwową strukturę eutektyczną cyny/ołowiu, która jest błyszcząca; kontrast z fazą ołowiu daje efekt cętkowany lub nakrapiany. Ten stop metalu jest określany jako metal nakrapiany. Główne zalety stosowania cyny do rur to jej wygląd, urabialność i odporność na korozję.
Optoelektronika
W tlenków indu i cyny są elektrycznie przewodzące i przezroczyste i są wykorzystywane do przezroczystych przewodzących elektrycznie folie z zastosowań optoelektronicznych urządzeń, takich jak wyświetlacze ciekłokrystaliczne .
Inne aplikacje
Perforowana stal ocynowana, zwana także perforowaną cyną, jest rzemieślniczą techniką wywodzącą się z Europy Środkowej, służącą do tworzenia funkcjonalnych i dekoracyjnych artykułów gospodarstwa domowego. Ozdobne wzory piercingu istnieją w szerokiej gamie, w oparciu o lokalną tradycję i rzemieślnika. Najczęstszym zastosowaniem tej techniki rzemieślniczej są lampiony z perforowanej cyny. Światło świecy wpadające przez dziurkowany wzór tworzy dekoracyjny wzór świetlny w pomieszczeniu, w którym stoi. Latarnie i inne wyroby z perforowanej cyny powstały w Nowym Świecie od najwcześniejszego osadnictwa europejskiego. Dobrze znanym przykładem jest latarnia Revere, nazwana na cześć Paula Revere .
Przed erą nowożytną w niektórych rejonach Alp ostrzono róg kozy lub barani i wycinano blaszany panel przy użyciu alfabetu i cyfr od jednego do dziewięciu. To narzędzie do nauki było znane jako „róg”. Nowoczesne reprodukcje zdobią takie motywy jak serca i tulipany.
W Ameryce sejfy na ciasto i żywność były używane w czasach przed chłodzeniem. Były to drewniane szafki w różnych stylach i rozmiarach – stojące lub wiszące, mające odstraszać szkodniki i owady oraz chronić przed kurzem łatwo psującą się żywność. Szafki te miały wstawki z blachy ocynowanej w drzwiach, a czasem po bokach, wycinane przez właściciela domu, stolarza lub blacharza w różnych wzorach, aby umożliwić cyrkulację powietrza, jednocześnie wykluczając muchy. Nowoczesne reprodukcje tych artykułów pozostają popularne w Ameryce Północnej.
Szyba okienna jest najczęściej wykonywana przez zatapianie stopionego szkła na stopionej cynie ( szkło float ), co daje płaską i nieskazitelną powierzchnię. Nazywa się to również „ procesem Pilkingtona ”.
Cyna jest używana jako elektroda ujemna w zaawansowanych akumulatorach litowo-jonowych . Jego zastosowanie jest nieco ograniczone faktem, że niektóre powierzchnie cyny katalizują rozkład elektrolitów na bazie węglanów stosowanych w akumulatorach litowo-jonowych.
Cyny (II), fluorek dodaje niektórych produktach do pielęgnacji zębów, jak fluorek cyny (SNF 2 ). Fluorek cyny(II) można mieszać ze środkami ściernymi wapniowymi, podczas gdy bardziej powszechny fluorek sodu stopniowo staje się nieaktywny biologicznie w obecności związków wapnia. Wykazano również, że jest bardziej skuteczny niż fluorek sodu w zwalczaniu zapalenia dziąseł .
Cyna jest wykorzystywana jako cel do tworzenia plazmy indukowanej laserem, która działa jako źródło światła w ekstremalnej litografii ultrafioletowej .
Związki cynoorganiczne
Najsilniej wykorzystywane są związki cynoorganiczne. Światowa produkcja przemysłowa prawdopodobnie przekracza 50 000 ton .
stabilizatory PCV
Głównym zastosowaniem komercyjnym związków cynoorganicznych jest stabilizacja tworzyw sztucznych PVC . W przypadku braku takich stabilizatorów, PVC ulegałby gwałtownej degradacji pod wpływem ciepła, światła i tlenu atmosferycznego, powodując przebarwione, kruche produkty. Cyna zmiata nietrwałe jony chlorkowe (Cl - ), które w przeciwnym razie pozbawiłyby HCl tworzywa sztucznego. Typowe związki cyny są pochodne kwasów karboksylowych, dichlorek dibutylocyny, takie jak di laurynian .
Biocydy
Niektóre związki cynoorganiczne są stosunkowo toksyczne, co ma zarówno zalety, jak i problemy. Wykorzystywane są do właściwości biobójczych jako fungicydy , pestycydy , algicydy , środki do konserwacji drewna i środki przeciwporostowe . Tlenek tributylocyny jest używany jako środek do konserwacji drewna . Tributylocyna jest również wykorzystywana do różnych celów przemysłowych, takich jak kontrola szlamu w papierniach i dezynfekcja cyrkulujących przemysłowych wód chłodzących. Tributylocynę zastosowano jako dodatek do farb okrętowych, aby zapobiec wzrostowi organizmów porostowych na statkach, przy czym zastosowanie zmniejszyło się po uznaniu związków cynoorganicznych za trwałe zanieczyszczenia organiczne o wysokiej toksyczności dla niektórych organizmów morskich ( na przykład trąbka psa ). UE zakazała stosowania związków cynoorganicznych w 2003 r., jednocześnie obawiając się toksyczności tych związków dla życia morskiego oraz szkód w reprodukcji i rozwoju niektórych gatunków morskich (niektóre raporty opisują skutki biologiczne dla życia morskiego przy stężeniu 1 nanograma na litr ) doprowadziły do światowego zakazu wydanego przez Międzynarodową Organizację Morską . Wiele krajów ogranicza obecnie stosowanie związków cynoorganicznych do statków o długości większej niż 25 m (82 ft). Trwałość tributylocyny w środowisku wodnym zależy od charakteru ekosystemu. Z powodu tej trwałości i jej stosowania jako dodatku do farb okrętowych, wysokie stężenia tributylocyny zostały znalezione w osadach morskich znajdujących się w pobliżu doków morskich. Tributylocyny został użyty jako biomarkera imposex w neograstropods , przy czym co najmniej 82 znanych gatunków. Przy wysokim poziomie TBT na lokalnych obszarach przybrzeżnych, spowodowanym działalnością żeglugową, mięczaki miały niekorzystny wpływ. Imposex to nakładanie męskich cech płciowych na osobniki żeńskie, w których wyrastają penis i pallialny nasieniowód . Wysoki poziom TBT może uszkadzać gruczoły dokrewne ssaków , układ rozrodczy i ośrodkowy układ nerwowy , strukturę kości i przewód pokarmowy . Tributylotyna wpływa nie tylko na ssaki, ale także na wydry morskie, wieloryby, delfiny i ludzi.
Chemia organiczna
Niektóre odczynniki cynowe są przydatne w chemii organicznej . W największym zastosowaniu chlorek cyny(II) jest powszechnym środkiem redukującym do konwersji grup nitrowych i oksymowych do amin . W reakcji Stille pary cynoorganiczne z organicznymi halogenkami lub pseudohalogenkiem .
Akumulatory litowo-jonowe
Cyna tworzy kilka faz międzymetalicznych z metalicznym litem, co czyni ją potencjalnie atrakcyjnym materiałem do zastosowań akumulatorowych. Duża ekspansja objętościowa cyny po stopowaniu z litem i niestabilność granicy faz cyna-elektrolit organiczny przy niskich potencjałach elektrochemicznych to największe wyzwania w zastosowaniu w ogniwach komercyjnych. Problem częściowo rozwiązała firma Sony . Związek międzymetaliczny cyny z kobaltem i węglem został zastosowany przez Sony w swoich ogniwach Nexelion wprowadzonych na rynek pod koniec 2000 roku. Skład materiału aktywnego wynosi w przybliżeniu Sn 0,3 Co 0,4 C 0,3 . Badania wykazały, że tylko niektóre krystaliczne fasetki tetragonalnego (beta) Sn są odpowiedzialne za niepożądaną aktywność elektrochemiczną.
Środki ostrożności
Przypadki zatrucia metaliczną cyną, jej tlenkami i solami są prawie nieznane. Z drugiej strony, niektóre związki cynoorganiczne są prawie tak toksyczne jak cyjanek .
Narażenie na cynę w miejscu pracy może nastąpić poprzez wdychanie, kontakt ze skórą i kontakt z oczami. USA Podawanie BHP (OSHA) ustawić graniczną ekspozycji cyny ekspozycji w miejscu pracy, w dawce 2 mg / m 3 dla 8-godzinnego dnia pracy. Narodowy Instytut Zdrowia i Bezpieczeństwa Pracy (NIOSH) określa się granicznych zalecanych ekspozycji (REL) z 2 mg / m 3 dla 8-godzinnego dnia pracy. Przy poziomie 100 mg/m 3 cyna jest bezpośrednio niebezpieczna dla życia i zdrowia .
Zobacz też
- Cassiterides (mityczne Wyspy Cynowe )
- Lista krajów według produkcji cyny
- Stannary
- Terne
- Szkodnik z cyny
- Wydobycie cyny w Wielkiej Brytanii
- Cynowanie
- Whisker (metalurgia) (blaszane wąsy)
Uwagi
Bibliografia
Bibliografia
-
 Ten artykuł zawiera tekst z tego źródła, które jest w domenie publicznej : Carlin, James F., Jr. (1998). „Znaczące wydarzenia wpływające na ceny cyny od 1958 roku” . US National Geodetic Survey
Ten artykuł zawiera tekst z tego źródła, które jest w domenie publicznej : Carlin, James F., Jr. (1998). „Znaczące wydarzenia wpływające na ceny cyny od 1958 roku” . US National Geodetic Survey
- Współtwórcy CRC (2006). David R. Lide (red.). Podręcznik chemii i fizyki (wyd. 87.). Boca Raton, Floryda: CRC Press, Taylor & Francis Group. Numer ISBN 978-0-8493-0487-3.
- Emsley, John (2001). „Puszka” . Bloki konstrukcyjne natury: przewodnik od A do Z po żywiołach . Oxford, Anglia, Wielka Brytania: Oxford University Press. s. 445–450 . Numer ISBN 978-0-19-850340-8.
- Greenwood, Norman N .; Earnshaw, Alan (1997). Chemia pierwiastków (wyd. 2). Butterwortha-Heinemanna . Numer ISBN 978-0-08-037941-8.
- Heiserman, David L. (1992). „Element 50: Cyna” . Poznawanie pierwiastków chemicznych i ich związków . Nowy Jork: Książki TAB. Numer ISBN 978-0-8306-3018-9.
- MacIntosh, Robert M. (1968). "Cyna". W Clifford A. Hampel (red.). Encyklopedia pierwiastków chemicznych . Nowy Jork: Reinhold Book Corporation. s. 722–732. LCCN 68-29938 .
- Stwertka, Albert (1998). „Cyna” . Przewodnik po elementach (wyd. poprawione). Oxford University Press. Numer ISBN 978-0-19-508083-4.
Zewnętrzne linki
- Tin w układzie okresowym filmów wideo (University of Nottingham)
- Drewniany stół okresowy Theodore'a Graya : Próbki i odlewy cyny
- Metale nieszlachetne: Cyna
- CDC — Kieszonkowy przewodnik NIOSH po zagrożeniach chemicznych
- Cyna (centy USD za kg)