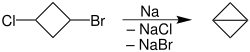Reakcja Wurtza - Wurtz reaction
| Reakcja Wurtza | |
|---|---|
| Nazwany po | Charles Adolphe Wurtz |
| Typ reakcji | Reakcja sprzęgania |
| Identyfikatory | |
| Portal chemii organicznej | reakcja wurtza |
Reakcji Wurtza , nazwany Charles Adolphem Wurtza , to reakcję sprzęgania w chemii organicznej , związki metaloorganiczne , a ostatnio nieorganicznych głównej grupy polimerów , przy czym dwa halogenki alkilowe, poddaje się reakcji z metalicznym sodem w roztworze suchego eteru, z wytworzeniem wyższe alkany. W tej reakcji halogenki alkilowe są traktowane metalicznym sodem w suchym eterowym (wolnym od wilgoci) roztworze w celu wytworzenia wyższych alkanów. Służy również do otrzymywania wyższych alkanów zawierających parzystą liczbę atomów węgla:
- 2 R − X + 2 Na → R − R + 2 Na + X -
Do uzyskania sprzężenia Wurtza stosowano również inne metale, między innymi srebro , cynk , żelazo , aktywowaną miedź , ind oraz mieszaninę manganu i chlorku miedzi . Pokrewna reakcja dotycząca halogenków arylu nazywana jest reakcją Wurtza-Fittiga . Można to wytłumaczyć tworzeniem wolnego rodnika pośredniego i jego późniejszą dysproporcjonowaniem do alkenu. Reakcja Wurtza zachodzi poprzez mechanizm wolnorodnikowy, który umożliwia reakcje uboczne wytwarzające produkty alkenowe .
Mechanizm
Reakcja ta polega na wymianie metal-halogen z udziałem rodników R · (w podobny sposób do tworzenia odczynnika Grignarda ) z tworzeniem wiązania węgiel-węgiel zachodzącym w reakcji podstawienia nukleofilowego .
Jeden elektron z metalu jest przenoszony do halogenu w celu wytworzenia halogenku metalu i rodnika alkilowego:
- R − X + M → R · + M + X -
Rodnik alkilowy następnie przyjmuje elektron z innego atomu metalu, tworząc anion alkilowy:
- R · + M → R - M +
Ten półprodukt został wyodrębniony w kilku przypadkach.
Następnie nukleofilowy węgiel anionu alkilowego wypiera halogenek w reakcji S N 2 , tworząc nowe wiązanie kowalencyjne węgiel-węgiel:
- R - M + + R − X → R − R + M + X -
Przykłady i warunki reakcji
Z powodu kilku ograniczeń ta reakcja jest rzadko stosowana. Na przykład nie toleruje szeregu grup funkcyjnych . Sprzęgło Wurtza jest jednak przydatne do zamykania małych, zwłaszcza trójczłonowych pierścieni. W ten sposób otrzymano bicyklobutan z 1-bromo-3-chlorocyklobutanu z 95% wydajnością. Reakcję prowadzi się we wrzącym dioksanie, w której temperaturze sód jest ciekły. Ta reakcja ma słabą wydajność, co jest konsekwencją tworzenia wielu produktów. W przypadku dihalogenków (1,3), (1,4), (1,5), (1,6) prowadzi to do powstawania produktów cyklicznych. W dihalogenkach wicynalnych tworzy alkeny, natomiast w dihalogenkach geminalnych tworzy alkiny.
Ograniczenia
Reakcja Wurtza jest rzadko stosowana z powodu reakcji ubocznych. Ma ograniczone zastosowanie do syntezy symetrycznych alkanów. Jeśli jako reagenty przyjmie się dwa odmienne halogenki alkilu, wówczas produkt jest mieszaniną alkanów, którą często trudno jest rozdzielić drogą destylacji frakcjonowanej, ponieważ różnice między temperaturami wrzenia produktów są zazwyczaj bardzo małe. Metanu nie można uzyskać tą metodą. Ten typ reakcji zawodzi w przypadku trzeciorzędowych halogenków. Ponadto, ponieważ reakcja obejmuje wolne rodniki, zachodzi reakcja uboczna prowadząca do wytworzenia alkenu . Ta reakcja uboczna staje się bardziej znacząca, gdy halogenki alkilowe są masywne przy atomie węgla przyłączonym do chlorowca.
Zobacz też
Bibliografia
- Adolphe Wurtz (1855). „Sur une nouvelle classe de radicaux organiques” . Annales de chimie et de physique . 44 : 275–312.
- Adolphe Wurtz (1855). „Ueber eine neue Klasse organischer Radicale” . Annalen der Chemie und Pharmacie . 96 (3): 364–375. doi : 10.1002 / jlac.18550960310 .
- Organic-chemistry.org
- Organie Chemistry autorstwa Morrisona i Boyda
- Organic Chemistry , Graham Solomons i Craig Fryhle, Wiley Publications