Heksachloroiidan (IV) amonu - Ammonium hexachloroiridate(IV)
|
|

|
|
| Identyfikatory | |
|---|---|
|
Model 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| Karta informacyjna ECHA |
100.037.264 |
| Numer WE | |
|
PubChem CID
|
|
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| H 8 N 2 Cl 6 Ir | |
| Masa cząsteczkowa | 441.01 |
| Wygląd | brązowe kryształy |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
| Referencje Infobox | |
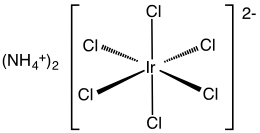
Heksachloroiidan amonu (IV) jest związkiem nieorganicznym o wzorze (NH 4 ) 2 [IrCl 6 ]. To ciemnobrązowe ciało stałe jest solą amonową kompleksu irydu (IV) [IrCl 6 ] 2− . Jest handlowo ważnym związkiem irydu, jednym z najpowszechniejszych kompleksów irydu (IV). Pokrewnym, ale źle zdefiniowanym związkiem jest tetrachlorek irydu , który jest często używany zamiennie.
Struktura
Związek scharakteryzowano metodą krystalografii rentgenowskiej . Sól krystalizuje w sześciennym motywie, takim jak heksachloroplatynian amonu . Centra [IrCl 6 ] 2− mają oktaedryczną geometrię molekularną .
Używa
Jest kluczowym półproduktem do izolacji irydu z rud. Większość innych metali tworzy nierozpuszczalne siarczki, gdy wodne roztwory ich chlorków są traktowane siarkowodorem , ale [IrCl 6 ] 2− jest odporny na podstawienie ligandem. Podczas ogrzewania pod wodorem, stała sól przekształca się w metal:
- (NH 4 ) 2 [IrCl 6 ] + 2 H 2 → Ir + 6 HCl + 2 NH 3
Klejenie
Wiele uwagi wzbudziła struktura elektronowa heksachloroiridanu (IV) amonu. Jego moment magnetyczny jest mniejszy niż obliczony dla jednego elektronu. Wynik ten jest interpretowany jako wynik antyferromagnetycznego sprzężenia między centrami Ir, w którym pośredniczą interakcje Cl --- Cl. Badania rezonansu spinowego elektronów wykazały, że ponad połowa gęstości spinu znajduje się na chlorkach, dlatego opis kompleksu jako Ir (IV) jest nadmiernym uproszczeniem.
