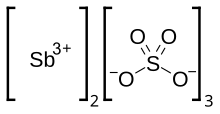
Siarczan antymonu - Antimony sulfate
|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Trisiarczan antymonu (3+)
|
|
| Inne nazwy
Antymonu (III), siarczan
Antimonous siarczan antymonu trisulfate diantymonu trisulfate diantymonu tris (VI) |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.028.370 |
| Numer WE | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| Sb 2 (SO 4 ) 3 | |
| Masa cząsteczkowa | 531,7078 g/mol |
| Gęstość | 3,6246 g/cm 3 |
| rozpuszczalny | |
| Zagrożenia | |
| Arkusz danych dotyczących bezpieczeństwa | MSDS |
| NIOSH (limity ekspozycji dla zdrowia w USA): | |
|
PEL (dopuszczalne)
|
TWA 0,5 mg/m 3 (jako Sb) |
|
REL (zalecane)
|
TWA 0,5 mg/m 3 (jako Sb) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Siarczan antymonu Sb 2 (SO 4 ) 3 jest higroskopijną solą powstałą w wyniku reakcji antymonu lub jego związków z gorącym kwasem siarkowym . Jest on stosowany w dopingu od półprzewodników oraz w produkcji materiałów wybuchowych i fajerwerków.
Struktura
Stały siarczan antymonu zawiera nieskończone drabiny czworościanów SO 4 i piramid SbO 3 dzielących się narożami. Jest często opisywany jako tlenek mieszany, Sb 2 O 3 .3SO 3 .
Właściwości chemiczne
Siarczan antymonu jest czasami nazywany „solą”, ponieważ może być wytwarzany w reakcji antymonu i kwasu siarkowego, ale antymon nie tworzy azotanu po rozpuszczeniu w kwasie azotowym (kwas utleniający), ale wytwarza mieszaninę tlenków antymonu i kontrastuje to z bizmutem, który rozpuszcza się w obu kwasach, tworząc sole. Jest rozpływający się i rozpuszczalny w kwasach . Można go wytworzyć przez rozpuszczenie antymonu, trójtlenek antymonu , antymonu trisiarczkową lub antymonu tlenochlorek w gorący, stężony kwas siarkowy .
- 2 Sb (s) + 6 H 2 SO 4 → Sb 2 (SO 4 ) 3 + 3SO 2 + 6 H 2 O
Zastosowania
Dzięki swojej rozpuszczalności siarczan antymonu ma zastosowanie w domieszkowaniu półprzewodników . Wykorzystywany jest również do powlekania anod w elektrolizie oraz przy produkcji materiałów wybuchowych i fajerwerków.
Bezpieczeństwo
Siarczan antymonu(III) powoduje podrażnienie skóry i błon śluzowych.
Naturalne występowanie
Naturalny analog tego konkretnego związku jest jeszcze nieznany. Jednak zasadowe uwodnione siarczany Sb są znane jako minerały klebelsbergit i coquandite .
