Kwas arsenowy - Arsenous acid
|
|
|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Kwas aromatyczny
|
|
| Inne nazwy
Kwas
arsenowy Tlenek arsenu |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CZEBI | |
| ChemSpider | |
| DrugBank | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| H 3 AsO 3 | |
| Masa cząsteczkowa | 125,94 g/mol |
| Wygląd | Występuje tylko w roztworach wodnych |
| Podstawa sprzężona | Arsenit |
| -51,2 x 10 -6 cm 3 / mol | |
| Zagrożenia | |
| Główne zagrożenia | Toksyczny, żrący |
| NIOSH (limity ekspozycji dla zdrowia w USA): | |
|
PEL (dopuszczalne)
|
[1910.1018] TWA 0,010 mg/m 3 |
|
REL (zalecane)
|
Ca C 0,002 mg/m 3 [15 minut] |
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
Ca [5 mg/m 3 (jako As)] |
| Związki pokrewne | |
|
Związki pokrewne
|
kwas arsenowy |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
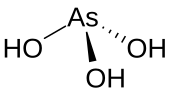
Kwas arsenawy (lub kwas arsenawy ) jest związkiem nieorganicznym o wzorze H 3 AsO 3 . Wiadomo, że występuje w roztworach wodnych , ale nie został wyizolowany jako czysty materiał, chociaż fakt ten nie umniejsza znaczenia As(OH) 3 .
Nieruchomości
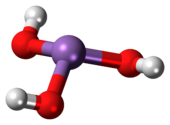
As(OH) 3 to cząsteczka piramidalna składająca się z trzech grup hydroksylowych związanych z arsenem. 1 H -NMR widmo roztworów kwasu arsenawy składa się z pojedynczego spójnego sygnału o wysokiej symetrii molekuły. W przeciwieństwie do tego, teoretycznie związane kwas fosforowy H 3 PO 3 przyjmuje HPO konstrukcja (OH) 2 . Strukturalny analog kwasu arsenawego (P(OH) 3 ) jest bardzo niewielkim składnikiem równowagi takich roztworów. Różne zachowania związków As i P odzwierciedlają trend, w którym wysokie stany utlenienia są bardziej stabilne dla lżejszych elementów pierwiastków grupy głównej niż ich cięższych kongenerów.
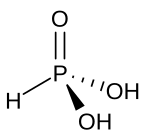
Jednym z tautomerów kwasu arsenowego jest HAsO(OH) 2 , który nazywa się kwasem arsenowym . Nie został wyizolowany ani dobrze scharakteryzowany.
Synteza
Wytwarzanie As (OH) 3 obejmuje powolną hydrolizę w trójtlenek arsenu w wodzie. Dodanie zasady przekształca kwas arsenowy w jony arseninowe [AsO(OH) 2 ] − , [AsO 2 (OH)] 2- , oraz [AsO 3 ] 3- .
Reakcje
Z pierwszym P K jest 9,2, As (OH) 3 jest słaby kwas. Reakcje przypisywane wodnemu trójtlenkowi arsenu zachodzą z kwasem arsenawym i jego sprzężonymi zasadami.
Podobnie jak trójtlenek arsenu, kwas arsenawy jest czasami amfoteryczny . Na przykład reaguje z kwasami chlorowodorowym, bromowodorowym i jodowodorowym, tworząc trichlorek, tribromek i trijodek arsenu.
- As(OH) 3 + 3 HCl ⇌ AsCl 3 + 3 H 2 O
- As(OH) 3 + 3 HBr AsBr 3 + 3 H 2 O
- As(OH) 3 + 3 HI ⇌ AsI 3 + 3 H 2 O
Reakcja kwasu arsenowego z jodkiem metylu daje kwas metyloarsonowy . Ta historycznie ważna konwersja jest reakcją Meyera :
- As(OH) 3 + CH 3 I + NaOH ⇌ CH 3 AsO(OH) 2 + NaI + H 2 O
Alkilacja zachodzi w przypadku arsenu, a stopień utlenienia arsenu wzrasta od +3 do +5.
Toksykologia
Związki zawierające arsen są wysoce toksyczne i rakotwórcze . Bezwodnik postać kwasu arsenawy, trójtlenek arsenu , stosuje się jako herbicydy , pestycydy i gryzonie .
