Wiązanie węgiel-węgiel - Carbon–carbon bond
Wiązanie węgiel-węgiel jest wiązaniem kowalencyjnym pomiędzy dwoma atomów węgla . Najpopularniejszą formą jest wiązanie pojedyncze : wiązanie złożone z dwóch elektronów , po jednym z każdego z dwóch atomów. Pojedyncze wiązanie węgiel-węgiel jest wiązaniem sigma i powstaje między jednym zhybrydyzowanym orbitalem z każdego z atomów węgla. W etanu , orbitale są sp 3 - hybrydyzowano orbitale, ale tworzą pojedyncze wiązania między atomami węgla, z innymi hybrydyzacji występują (np sp 2 SP 2 ). W rzeczywistości atomy węgla w pojedynczym wiązaniu nie muszą mieć tej samej hybrydyzacji. Atomy węgla mogą również tworzyć wiązania podwójne w związkach zwanych alkenami lub wiązania potrójne w związkach zwanych alkinami . Tworzone jest wiązanie podwójne z orbitalem zhybrydyzowanym sp 2 i orbitalem p, który nie jest zaangażowany w hybrydyzację. Powstaje potrójne wiązanie z orbitalem zhybrydyzowanym sp i dwoma orbitalami p z każdego atomu. Użycie orbitali p tworzy wiązanie pi .
Łańcuchy i rozgałęzienia
Węgiel jest jednym z nielicznych pierwiastków, które mogą tworzyć długie łańcuchy własnych atomów, właściwość nazywana katencją . To, w połączeniu z siłą wiązania węgiel-węgiel, daje początek ogromnej liczbie form molekularnych, z których wiele jest ważnymi elementami strukturalnymi życia, dlatego związki węgla mają swój własny kierunek badań: chemię organiczną .
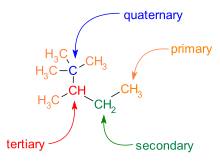
Rozgałęzienie jest również powszechne w szkieletach C−C. Atomy węgla w cząsteczce są klasyfikowane według liczby sąsiadów węgla, które mają:
- Podstawowy węglowy ma jeden węgla sąsiada.
- Węgla wtórna ma dwie sąsiadów węgla.
- Trzeciorzędowy węgiel ma trzy sąsiadów węgla.
- Czwartorzędowy węgiel ma cztery sąsiadów węgla.
W „strukturalnie złożonych cząsteczkach organicznych” to trójwymiarowa orientacja wiązań węgiel-węgiel w czwartorzędowych loci dyktuje kształt cząsteczki. Ponadto, czwartorzędowe loci znajdują się w wielu biologicznie aktywnych małych cząsteczkach, takich jak kortyzon i morfina .
Synteza
Reakcje tworzenia wiązania węgiel-węgiel to reakcje organiczne, w których powstaje nowe wiązanie węgiel-węgiel. Są ważne w produkcji wielu chemikaliów wytwarzanych przez człowieka, takich jak farmaceutyki i tworzywa sztuczne .
Niektóre przykłady reakcji, które tworzą wiązania węgiel-węgiel są reakcje aldolowe , reakcje Dielsa-Aldera , dodanie odczynnika Grignarda do grupy karbonylowej , w reakcji Hecka , w reakcji Michaela i reakcji Wittiga .
Ukierunkowana synteza pożądanych struktur trójwymiarowych dla węgli trzeciorzędowych została w dużej mierze rozwiązana pod koniec XX wieku, ale ta sama zdolność do bezpośredniej syntezy czwartorzędowego węgla pojawiła się dopiero w pierwszej dekadzie XXI wieku.
Siły i długości wiązania
Pojedyncze wiązanie węgiel-węgiel jest słabsze niż wiązania CH, OH, NH, HH, H-Cl, CF i wielu podwójnych lub potrójnych wiązań i jest porównywalne pod względem siły z wiązaniami CO, Si-O, PO i SH, ale powszechnie uważany za silny.
| Wiązanie C–C | Cząsteczka | Energia dysocjacji wiązania (kcal/mol) |
|---|---|---|
| CH 3 CH 3 | etan | 90 |
| C 6 H 5 -CH 3 | toluen | 102 |
| C 6 H 5 -C 6 H 5 | bifenyl | 114 |
| CH 3 C (O) -CH 3 | aceton | 84 |
| CH 3 -CN | acetonitryl | 136 |
| CH 3 -CH 2 OH | etanol | 88 |
Podane powyżej wartości reprezentują energie dysocjacji wiązania CC, które są powszechnie spotykane; czasami wartości odstające mogą drastycznie odbiegać od tego zakresu.
| Cząsteczka | Etan | Etylen | Acetylen |
|---|---|---|---|
| Formuła | C, 2 H 6 | C 2 H 4 | C, 2 H 2 |
| Klasa | alkany | alken | alkin |
| Struktura |

|

|

|
| Hybrydyzacja węgla | sp 3 | sp 2 | sp |
| Długość wiązania CC | 1,535 Å | 1,339 Å | 1.203 Å |
| Proporcja pojedynczego wiązania CC | 100% | 87% | 78% |
| Metoda określania struktury | spektroskopia mikrofalowa | spektroskopia mikrofalowa | spektroskopia w podczerwieni |
Skrajne przypadki
Długie, słabe wiązania pojedyncze CC
Zidentyfikowano różne skrajne przypadki wydłużenia wiązania CC. W dimerze Gomberga jedno wiązanie CC jest dość długie i wynosi 159,7 pikometra . Jest to wiązanie, które odwracalnie i łatwo pęka w temperaturze pokojowej w roztworze:
W jeszcze bardziej zatłoczonej cząsteczce heksakis(3,5-di- tert- butylofenylo)etanie energia dysocjacji wiązania do utworzenia stabilizowanego rodnika triarylometylowego wynosi tylko 8 kcal/mol. Również w wyniku silnego przeciążenia przestrzennego, heksakis(3,5-di- tert- butylofenylo)etan ma znacznie wydłużone wiązanie centralne o długości 167 µm.
Skręcone, słabe wiązania podwójne CC
Struktura tetrakis(dimetyloamino)etylenu (TDAE) jest mocno zniekształcona. Kąt dwuścienny z dwiema N dwóch końcach C wynosi 28º chociaż odległość C = normalne 135 pM. Prawie izostrukturalne tetraisopropylethylene również odległość, C = 135 pm, a jej części C 6 rdzenia jest płaska.
Krótkie, mocne wiązania potrójne CC
Z drugiej strony, centralne pojedyncze wiązanie węgiel-węgiel diacetylenu jest bardzo silne przy 160 kcal/mol, ponieważ pojedyncze wiązanie łączy dwa węgle o hybrydyzacji sp. Wiązania wielokrotne węgiel-węgiel są na ogół silniejsze; określono, że podwójne wiązanie etylenu i potrójne wiązanie acetylenu mają energie dysocjacji wiązania odpowiednio 174 i 230 kcal/mol. Zaobserwowano bardzo krótkie wiązanie potrójne 115 µm dla form jodonu [HC≡C–I + Ph][CF 3 SO 3 – ], ze względu na silnie odciągające elektrony ugrupowanie jodu.