Syntaza metioniny - Methionine synthase
Syntaza metioniny znana również jako MS , MeSe , MTR odpowiada za regenerację metioniny z homocysteiny . U ludzi jest kodowany przez gen MTR (metylotransferaza 5-metylotetrahydrofoliano-homocysteiny). Syntaza metioniny jest częścią cyklu biosyntezy i regeneracji S-adenozylometioniny (SAMe) . U zwierząt enzym ten wymaga witaminy B12 (kobalaminy) jako kofaktora , podczas gdy forma występująca w roślinach jest niezależna od kobalaminy. Mikroorganizmy wyrażają zarówno formy zależne od kobalaminy, jak i niezależne od kobalaminy.
Mechanizm
Syntaza metioniny katalizuje ostatni etap regeneracji metioniny (Met) z homocysteiny (Hcy). Cała reakcja przekształca 5-metylotetrahydrofolian (N 5- MeTHF) w tetrahydrofolian (THF), jednocześnie przenosząc grupę metylową do homocysteiny z wytworzeniem metioniny. Metionina jest jedynym syntazy ssaczy enzym, który metabolizuje N 5 -MeTHF regenerację aktywnego kofaktora THF. W formach enzymu zależnych od kobalaminy reakcja przebiega w dwóch etapach w reakcji ping-ponga. Enzym wstępnie zagruntowane w reaktywnej przez przeniesienie grupy metylowej z N 5 -MeTHF do CO (i) enzym związany kobalaminy (COB), tworząc metylo-kobalaminy (Me-cob), który zawiera teraz Me-Co (III) i aktywacja enzymu. Następnie Hcy, który skoordynował się ze związanym z enzymem cynkiem, tworząc reaktywny tiolan, reaguje z Me-Cob. Aktywowana grupa metylowa jest przenoszona z Me-Cob do tiolanu Hcy, który regeneruje Co(I) w kolbie, a Met jest uwalniany z enzymu. Mechanizm kolby niezależne ma taką samą ogólną drogę ale z bezpośrednią reakcję pomiędzy tiolanu cynku i N 5 -MeTHF.
Mechanizm działania enzymu zależy od ciągłej regeneracji Co(I) w kolbie, ale nie zawsze jest to gwarantowane. Zamiast tego, co 1–2000 katalitycznych obrotów, Co(I) może zostać utleniony do Co(II), co spowoduje trwałe zatrzymanie aktywności katalitycznej. Oddzielne białko, reduktaza syntazy metioniny , katalizuje regenerację Co(I) i przywrócenie aktywności enzymatycznej. Ponieważ utlenianie kolb-Co(I) nieuchronnie wyłącza zależną od kolb aktywność syntazy metioninowej, defekty lub niedobory reduktazy syntazy metioninowej są powiązane z niektórymi chorobami związanymi z niedoborem syntazy metioninowej omówionych poniżej. Te dwa enzymy tworzą sieć zmiataczy widoczną w lewym dolnym rogu.
Struktura
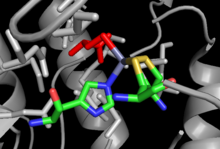
Rozwiązano struktury krystaliczne zarówno dla MetH niezależnego od kolb, jak i zależnego od kolb MetH, z niewielkim podobieństwem w ogólnej strukturze, pomimo identycznej reakcji netto przeprowadzanej przez każdy z nich i podobieństw w obrębie miejsc wiązania, takich jak miejsce wiązania Hcy. Kolby zależne met jest podzielona na 4 odrębnych domen: Aktywacja, wiążących kobalaminę (domena cob) , homocysteiny wiążące (Hcy domen) i N 5 -methylTHF wiązania (domena MeTHF). Domena aktywacyjna jest miejscem interakcji z reduktazą syntazy metioninowej i wiąże SAM, która jest wykorzystywana jako część cyklu reaktywacji enzymu. Domena Cob zawiera Cob umieszczony pomiędzy kilkoma dużymi alfa helisami i związany z enzymem, tak że atom kobaltu grupy jest wystawiony na kontakt z innymi domenami. Domena Hcy zawiera krytyczne miejsce wiązania cynku, składające się z reszt cysteiny lub histydyny skoordynowanych z jonem cynku, który może wiązać Hcy, z przykładem MetH niezależnego od Cob pokazanym po prawej stronie. N 5 -MeTHF domena wiążąca zawiera konserwowany lufy, w którym n 5 wiązań wodorowych -MeTHF puszki z asparaginą , argininą i kwasu asparaginowego pozostałości. Cała struktura przechodzi dramatyczny ruch wahadłowy podczas katalizy, gdy domena Cob przemieszcza się tam iz powrotem z domeny Hcy do domeny Fol, przenosząc aktywną grupę metylową z domeny Fol do domeny Hcy.
Funkcjonować
Głównym celem syntazy metioniny jest regeneracja Met w cyklu S-adenozylometioniny, która w jednym obrocie zużywa Met i ATP oraz generuje Hcy. Cykl ten jest krytyczny, ponieważ S-adenozylometionina jest szeroko stosowana w biologii jako źródło aktywnej grupy metylowej, a zatem syntaza metioniny pełni podstawową funkcję, pozwalając na utrwalenie cyklu SAM bez stałego dopływu Met. W ten sposób, metionina syntazy służy również do utrzymania niskiego poziomu Hcy a ponieważ metionina syntazy jeden z kilku enzymów stosowanych N 5 -MeTHF jako podłoże do pośredniego utrzymywania poziomu THF.
W roślinach i mikroorganizmach syntaza metioniny służy podwójnemu celowi, zarówno utrwalania cyklu SAM, jak i katalizowania końcowego etapu syntezy w syntezie Met de novo . Chociaż reakcja jest dokładnie taka sama dla obu procesów, ogólna funkcja jest różna od syntazy metioniny u ludzi, ponieważ Met jest niezbędnym aminokwasem, który nie jest syntetyzowany de novo w organizmie.
Znaczenie kliniczne
Mutacje w genie MTR zostały zidentyfikowane jako podstawowa przyczyna niedoboru metylokobalaminy grupy G lub niedoboru metylokobalaminy typu cblG. Niedobór lub deregulacja enzymu z powodu niedoboru reduktazy syntazy metioninowej może bezpośrednio skutkować podwyższonym poziomem homocysteiny ( hiperhomocysteinemią ), co wiąże się ze ślepotą, objawami neurologicznymi i wadami wrodzonymi. Większość przypadków niedoboru syntazy metioniny objawia się w ciągu 2 lat od urodzenia, au wielu pacjentów szybko rozwija się ciężka encefalopatia. Jedną z konsekwencji zmniejszonej aktywności syntazy metioniny, którą można zmierzyć rutynowymi klinicznymi badaniami krwi, jest niedokrwistość megaloblastyczna .
Genetyka
Zidentyfikowano kilka polimorfizmów w genie MTR.
- 2756D→G (Asp 919 Gly)
Zobacz też
- metylotransferaza
- Zespół Arakawy II
- 5-metylotetrahydroksyfolian (5-Me-THF, 5-Me H 4 F, 5-MTHF)
- Betaina — S-metylotransferaza homocysteiny
Bibliografia
Dalsza lektura
- Ludwig ML, Matthews RG (1997). „Perspektywy strukturalne na enzymy zależne od witaminy B12”. Roczny Przegląd Biochemii . 66 : 269–313. doi : 10.1146/annurev.biochem.66.1.269 . PMID 9242908 .
- Matthews RG, Sheppard C, Goulding C (kwiecień 1998). „Reduktaza metylenotetrahydrofolianu i syntaza metioniny: biochemia i biologia molekularna” (PDF) . European Journal of Pediatrics . 157 Dodatek 2: S54–9. doi : 10.1007/PL00014305 . PMID 9587027 . S2CID 8709190 .
- Garovic-Kocic V, Rosenblatt DS (sierpień 1992). „Auksotrofia metioniny we wrodzonych błędach metabolizmu kobalaminy”. Medycyna kliniczna i śledcza . 15 (4): 395–400. PMID 1516297 .
- O'Connor DL, Moriarty P, Picciano MF (1992). „Wpływ niedoboru żelaza na przepływ folianów w obrębie gruczołu sutkowego”. Międzynarodowy Dziennik Badań nad Witaminą i Odżywianiem. Internationale Zeitschrift für Vitamin- und Ernährungsforschung. Journal International de Vitaminologie et de Nutrition . 62 (2): 173–80. PMID 1517041 .
- Everman BW, Koblin DD (marzec 1992). „Starzenie się, przewlekłe podawanie etanolu i ostre narażenie na podtlenek azotu: wpływ na witaminę B12 i stan kwasu foliowego u szczurów”. Mechanizmy starzenia się i rozwoju . 62 (3): 229–43. doi : 10.1016/0047-6374(92)90109-Q . PMID 1583909 . S2CID 11766691 .
- Vassiliadis A, Rosenblatt DS, Cooper BA, Bergeron JJ (sierpień 1991). „Lisosomalna akumulacja kobalaminy w fibroblastach od pacjenta z wrodzonym błędem metabolizmu kobalaminy (grupa komplementacji cblF): wizualizacja za pomocą radioautografii pod mikroskopem elektronowym”. Eksperymentalne badania nad komórkami . 195 (2): 295–302. doi : 10.1016/0014-4827(91)90376-6 . PMID 2070814 .
- Li YN, Gulati S, Baker PJ, Brody LC, Banerjee R, Kruger WD (grudzień 1996). „Klonowanie, mapowanie i analiza RNA ludzkiego genu syntazy metioniny” . Genetyka molekularna człowieka . 5 (12): 1851-8. doi : 10.1093/hmg/5.12.1851 . PMID 8968735 .
- Gulati S, Baker P, Li YN, Fowler B, Kruger W, Brody LC, Banerjee R (grudzień 1996). „Defekty w ludzkiej syntazie metioniny u pacjentów z cblG” . Genetyka molekularna człowieka . 5 (12): 1859–65. doi : 10.1093/hmg/5.12.1859 . PMID 8968736 .
- Leclerc D, Campeau E, Goyette P, Adjalla CE, Christensen B, Ross M, Eydoux P, Rosenblatt DS, Rozen R, Gravel RA (grudzień 1996). „Ludzka syntaza metioniny: klonowanie cDNA i identyfikacja mutacji u pacjentów z grupy komplementacji cblG zaburzeń folianów/kobalaminy” . Genetyka molekularna człowieka . 5 (12): 1867-74. doi : 10.1093/hmg/5.12.1867 . PMID 8968737 .
- Chen LH, Liu ML, Hwang HY, Chen LS, Korenberg J, Shane B (luty 1997). „Ludzka syntaza metioniny. Klonowanie cDNA, lokalizacja genów i ekspresja” . Czasopismo Chemii Biologicznej . 272 (6): 3628–34. doi : 10.1074/jbc.272.6.3628 . PMID 9013615 .
- Wilson A, Leclerc D, Saberi F, Campeau E, Hwang HY, Shane B, Phillips JA, Rosenblatt DS, Gravel RA (sierpień 1998). „Funkcjonalnie zerowe mutacje u pacjentów z wariantem cblG niedoboru syntazy metioniny” . American Journal of Human Genetics . 63 (2): 409–14. doi : 10.1086/301976 . PMC 1377317 . PMID 9683607 .
- Salomon O, Rosenberg N, Zivelin A, Steinberg DM, Kornbrot N, Dardik R, Inbal A, Seligsohn U (2002). „Polimorfizmy syntazy metioniny A2756G i reduktazy metylenotetrahydrofolianowej A1298C nie są czynnikami ryzyka idiopatycznej żylnej choroby zakrzepowo-zatorowej”. Czasopismo Hematologiczne . 2 (1): 38–41. doi : 10.1038/sj.thj.6200078 . PMID 11920232 .
- Watkins D, Ru M, Hwang HY, Kim CD, Murray A, Philip NS, Kim W, Legakis H, Wai T, Hilton JF, Ge B, Doré C, Hosack A, Wilson A, Gravel RA, Shane B, Hudson TJ , Rosenblatt DS (lipiec 2002). „Hiperhomocysteinemia spowodowana niedoborem syntazy metioninowej, cblG: struktura genu MTR, różnorodność genotypów i rozpoznanie wspólnej mutacji P1173L” . American Journal of Human Genetics . 71 (1): 143-53. doi : 10.1086/341354 . PMC 384971 . PMID 12068375 .
- De Marco P, Calevo MG, Moroni A, Arata L, Merello E, Finnell RH, Zhu H, Andreussi L, Cama A, Capra V (2002). „Badanie polimorfizmów MTHFR i stwardnienia rozsianego jako czynników ryzyka NTD w populacji włoskiej” . Journal of Human Genetics . 47 (6): 319–24. doi : 10.1007/s100380200043 . PMID 12111380 .
- Doolin MT, Barbaux S, McDonnell M, Hoess K, Whitehead AS, Mitchell LE (listopad 2002). „Efekty genetyczne matki, wywierane przez geny zaangażowane w remetylację homocysteiny, wpływają na ryzyko rozszczepu kręgosłupa” . American Journal of Human Genetics . 71 (5): 1222–6. doi : 10.1086/344209 . PMC 385102 . PMID 12375236 .
- Zhu H, Wicker NJ, Shaw GM, Lammer EJ, Hendricks K, Suarez L, Canfield M, Finnell RH (marzec 2003). „Polimorfizmy enzymu remetylacji homocysteiny i zwiększone ryzyko wad cewy nerwowej”. Genetyka molekularna i metabolizm . 78 (3): 216–21. doi : 10.1016/S1096-7192(03)00008-8 . PMID 12649067 .
Zewnętrzne linki
- Wpis GeneReviews/NCBI/NIH/UW dotyczący zaburzeń wewnątrzkomórkowego metabolizmu kobalaminy
- ENZYM: EC 2.1.1.13
- 5-metylotetrahydrofolian-homocysteina + S-metylotransferaza w amerykańskiej National Library of Medicine Medical Subject Headings (MeSH)