Prostacyklina - Prostacyclin
 | |
 | |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Flolan, Veletri |
| AHFS / Drugs.com | Monografia |
| Dane licencyjne | |
Kategoria ciąży |
|
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Dane farmakokinetyczne | |
| Okres półtrwania eliminacji | 42 sekundy |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEMBL | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Dane chemiczne i fizyczne | |
| Formuła | C 20 H 32 O 5 |
| Masa cząsteczkowa | 352.471 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
|
| |
Prostacyklina (zwany również prostaglandyny I2 lub PGI 2 ) jest prostaglandyna członkiem eikozanoidów rodzinę lipidowych cząsteczek . Hamuje aktywację płytek krwi, a także jest skutecznym środkiem rozszerzającym naczynia krwionośne.
Stosowany jako lek jest również znany jako epoprostenol . Terminy są czasami używane zamiennie.
Funkcjonować
Prostacyklina (PGI 2 ) zapobiega przede wszystkim tworzeniu się czopa płytkowego zaangażowanego w pierwotną hemostazę (część tworzenia skrzepu krwi ). Czyni to poprzez hamowanie aktywacji płytek krwi. Jest również skutecznym środkiem rozszerzającym naczynia krwionośne . Prostacykliny w interakcje kontrast z tymi tromboksanu (TXA 2 ), kolejny eikozanoidem. To silnie sugeruje mechanizm homeostazy sercowo-naczyniowej między tymi dwoma hormonami w związku z uszkodzeniem naczyń .
Zastosowania medyczne
Jest stosowany w leczeniu tętniczego nadciśnienia płucnego .
Degradacja
Prostacyklina, której okres półtrwania wynosi 42 sekundy, jest rozkładana na 6-keto-PGF 1 , który jest znacznie słabszym środkiem rozszerzającym naczynia krwionośne.
Mechanizm
Efekt prostacykliny Mechanizm Odpowiedź komórkowa
Funkcje klasyczneTon statku ↑cAMP, ↓ET-1
↓Ca 2+ , ↑K +↓Proliferacja SMC
↑Rozszerzenie naczyń krwionośnychAntyproliferacyjny ↑cAMP
↑PPARgamma↓Wzrost fibroblastów
↑ApoptozaPrzeciwzakrzepowe ↓Tromboksan-A2
↓PDGF↓Agregacja płytek
↓Przyleganie płytek do ściany naczyniaNowatorskie
funkcjePrzeciwzapalny ↓IL-1, IL-6
↑IL-10↓Cytokiny prozapalne
↑ Cytokiny przeciwzapalneAntymitogenne ↓VEGF
↓TGF-β↓Angiogeneza
↑Przebudowa ECM
Jak wspomniano powyżej, prostacyklina (PGI 2 ) jest zwolnione przez zdrowe komórki śródbłonka i spełnia swoją funkcję przez parakrynnego sygnału, który wiąże się z receptorami sprzężonymi z białkiem G. na sąsiednich płytek krwi i komórek śródbłonka. Receptor płytkowy sprzężony z białkiem Gs ( receptor prostacykliny ) jest aktywowany , gdy wiąże się z PGI 2 . Ta aktywacja z kolei sygnalizuje cyklazie adenylylowej wytwarzanie cAMP . cAMP dalej hamuje nadmierną aktywację płytek krwi (w celu pobudzenia krążenia), a także przeciwdziała wzrostowi poziomu wapnia w cytozolu, który byłby wynikiem wiązania tromboksanu A2 (TXA 2 ) (prowadzącego do aktywacji płytek i późniejszej koagulacji ). PGI 2 wiąże się również ze śródbłonkowymi receptorami prostacykliny iw ten sam sposób podnosi poziom cAMP w cytozolu. Ten cAMP następnie aktywuje kinazę białkową A (PKA). Następnie PKA kontynuuje kaskadę, promując fosforylację kinazy lekkiego łańcucha miozyny , co hamuje ją i prowadzi do rozluźnienia mięśni gładkich i rozszerzenia naczyń . Można zauważyć, że PGI 2 i TXA 2 działają jako antagoniści fizjologiczni.
Członkowie
| PROSTACYKLINY | |||
|---|---|---|---|
| Flolan (epoprostenol sodu) do wstrzykiwań |
Ciągła infuzja | 2 ng/kg/min na początek, zwiększane o 2 ng/kg/min co 15 minut lub dłużej, aż do osiągnięcia odpowiedniej równowagi skuteczności/tolerancji | Klasa III Klasa IV |
|
Veletri (epoprostenol) do wstrzykiwań |
Ciągła infuzja | 2 ng/kg/min na początek, zwiększane o 2 ng/kg/min co 15 minut lub dłużej, aż do osiągnięcia odpowiedniej równowagi skuteczności/tolerancji | Klasa III Klasa IV |
| Remodulin SC§ ( treprostinil sodu) do wstrzykiwań |
Ciągła infuzja | 1,25 ng/kg/min na początek, zwiększone do 1,25 ng/kg/min na tydzień przez 4 tygodnie, następnie do 2,5 ng/kg/min na tydzień do
osiągnięto odpowiednią równowagę skuteczności/tolerancji |
Klasa II Klasa III Klasa IV |
|
Ventavis ( iloprost ) roztwór do inhalacji |
Wdychany 6–9 razy dziennie | 2,5 μg 6–9 razy dziennie na początku, zwiększona do 5,0 μg 6–9 razy dziennie, jeśli jest dobrze tolerowana | Klasa III Klasa IV |
Farmakologia
Syntetyczne analogi prostacykliny ( iloprost , cisaprost) stosuje się dożylnie, podskórnie lub wziewnie:
- jako środek rozszerzający naczynia krwionośne w ciężkim zjawisku Raynauda lub niedokrwieniu kończyny;
- w nadciśnieniu płucnym .
- w pierwotnym nadciśnieniu płucnym (PPH)
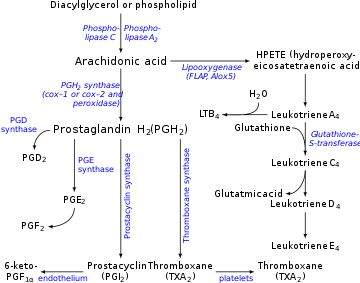
Wytwarzanie prostacykliny jest hamowane przez działanie NLPZ na enzymy cyklooksygenazy COX1 i COX2. Te konwersji kwasu arachidonowego do prostaglandyny H2 (pgh 2 ), bezpośredniego prekursora prostacykliny. Ponieważ tromboksan ( eikozanoidowy stymulator agregacji płytek) również znajduje się za enzymami COX, można by pomyśleć, że działanie NLPZ działałoby na rzecz równowagi. Jednak stężenia prostacyklin wracają znacznie szybciej niż poziomy tromboksanu, więc podawanie aspiryny początkowo ma niewielki lub żaden efekt, ale ostatecznie zapobiega agregacji płytek krwi (działanie prostaglandyn dominuje podczas ich regeneracji). Wyjaśnia to zrozumienie komórek, które produkują każdą cząsteczkę, TXA 2 i PGI 2 . Od PIG 2 składa się przede wszystkim w jądrzastych komórek śródbłonka, hamowanie COX przez NLPZ można przezwyciężyć w czasie przez zwiększoną aktywację genu COX, a następnie wytwarzanie większej ilości enzymów Cox katalizować powstawanie PIG 2 . W przeciwieństwie do tego, TXA 2 jest uwalniany głównie przez płytki bezjądrzaste, które nie są w stanie odpowiedzieć na hamowanie NLPZ COX dodatkową transkrypcją genu COX, ponieważ brakuje im materiału DNA niezbędnego do wykonania takiego zadania. Pozwala to NLPZ na dominację PGI 2 , która promuje krążenie i opóźnia zakrzepicę .
U pacjentów z nadciśnieniem płucnym epoprostenol wziewny obniża ciśnienie płucne i poprawia objętość wyrzutową prawej komory u pacjentów poddawanych zabiegom kardiochirurgicznym. Dawka 60 μg jest bezpieczna hemodynamicznie, a jej działanie całkowicie odwraca się po 25 minutach. Nie znaleziono dowodów na dysfunkcję płytek krwi lub zwiększenie krwawień chirurgicznych po podaniu wziewnego epoprostenolu. Wiadomo, że lek powoduje zaczerwienienie, bóle głowy i niedociśnienie.
Synteza
Biosynteza
Prostacyklina jest wytwarzana w komórkach śródbłonka , które wyściełają ściany tętnic i żył, z prostaglandyny H 2 (PGH 2 ) w wyniku działania enzymu syntazy prostacykliny . Chociaż prostacyklina jest uważana za niezależny mediator, w nomenklaturze eikozanoidów nazywana jest PGI 2 (prostaglandyna I 2 ) i należy do prostanoidów (razem z prostaglandynami i tromboksanem ). PGI2, pochodzący głównie z COX-2 u ludzi, jest głównym metabolitem arachidonianu uwalnianym ze śródbłonka naczyniowego. Jest to kontrowersyjna kwestia, niektórzy przypisują COX 1 jako główną cyklooksygenazę wytwarzającą prostacyklinę w komórkach śródbłonka naczyń krwionośnych.
Seria 3-prostaglandyny PGH 3 wynika również, szlak syntazy prostacykliny, otrzymując kolejne prostacykliny PGI 3 . Nieokreślony termin „prostacyklina” zwykle odnosi się do PGI 2 . PGI 2 pochodzi od kwasu ω-6 arachidonowego . PGI 3 pochodzi z ω-3 EPA .
Sztuczna synteza
Prostacykliny mogą być syntetyzowane z metylowego estru z prostaglandyny F 2a . Po jego syntezie lek jest odtwarzany w soli fizjologicznej i glicerynie.
Historia
W latach 60. brytyjski zespół badawczy kierowany przez profesora Johna Vane'a zaczął badać rolę prostaglandyn w anafilaksji i chorobach układu oddechowego. Pracując z zespołem z Royal College of Surgeons , Vane odkrył, że aspiryna i inne doustne leki przeciwzapalne działają poprzez hamowanie syntezy prostaglandyn. To krytyczne odkrycie otworzyło drzwi do szerszego zrozumienia roli prostaglandyn w organizmie.
Zespół The Wellcome Foundation kierowany przez Salvadora Moncadę zidentyfikował mediatora lipidowego, który nazwali „PG-X”, który hamuje agregację płytek krwi. PG-X, później znany jako prostacyklina, jest 30 razy silniejszy niż jakikolwiek inny znany wówczas środek przeciwagregacyjny.
W 1976 roku Vane i jego koledzy badacze Salvador Moncada , Ryszard Gryglewski i Stuart Bunting opublikowali pierwszą pracę na temat prostacykliny w Naturze . Współpraca doprowadziła do powstania zsyntetyzowanej cząsteczki, którą nazwano epoprostenolem. Jednak, podobnie jak w przypadku natywnej prostacykliny, cząsteczka epoprostenolu jest niestabilna w roztworze i podatna na szybką degradację. Stanowiło to wyzwanie zarówno dla eksperymentów in vitro, jak i zastosowań klinicznych.
Aby przezwyciężyć to wyzwanie, zespół badawczy, który odkrył prostacyklinę, kontynuował badania. Zespół badawczy zsyntetyzował blisko 1000 analogów.
Zobacz też
Bibliografia
Zewnętrzne linki
- „Epoprostenol” . Portal informacyjny o narkotykach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „Sól sodowa epoprostenolu” . Portal informacyjny o narkotykach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.