Ximelagatran - Ximelagatran
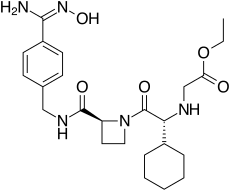 | |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Exanta |
Kategoria ciąży |
|
| Drogi administracji |
Doustnie ( tabletki ) |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Dane farmakokinetyczne | |
| Biodostępność | 20% |
| Metabolizm | do melagatranu |
| Okres półtrwania eliminacji | 3–5 godzin |
| Wydalanie | Nerki (80%) |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEMBL | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Dane chemiczne i fizyczne | |
| Formuła | C 24 H 35 N 5 O 5 |
| Masa cząsteczkowa | 473,574 g·mol -1 (429 g/mol po konwersji) |
| Model 3D ( JSmol ) | |
| |
| |
|
| |
Ximelagatran ( Exanta lub Exarta , H 376/95) jest antykoagulantem , który był szeroko badany jako zamiennik warfaryny , który przezwycięża problematyczne diety , interakcje i monitorowanie problemów związanych z terapią warfaryną. W 2006 roku jej producent AstraZeneca ogłosił, że wycofa oczekujące wnioski o dopuszczenie do obrotu po doniesieniach o hepatotoksyczności (uszkodzeniu wątroby) podczas badań i zaprzestanie jego dystrybucji w krajach, w których lek został dopuszczony (Niemcy, Portugalia, Szwecja, Finlandia, Norwegia, Islandia, Austria, Dania, Francja, Szwajcaria, Argentyna i Brazylia).
Sposób działania
Ximelagatran, bezpośredni inhibitor trombiny , był pierwszym przedstawicielem tej klasy, który można przyjmować doustnie. Działa wyłącznie poprzez hamowanie działania trombiny . Jest przyjmowany doustnie dwa razy dziennie i szybko wchłaniany przez jelito cienkie . Ximelagatran jest prolekiem , który w warunkach in vivo jest przekształcany w substancję czynną melagatran. Ta konwersja zachodzi w wątrobie i wielu innych tkankach poprzez hydrolizę i dehydroksylację (zastąpienie grup etylowych i hydroksylowych wodorem ).
Zastosowania
Oczekiwano, że ksymelagatran zastąpi warfarynę, a czasami aspirynę i heparynę w wielu ustawieniach terapeutycznych, w tym w zakrzepicy żył głębokich , zapobieganiu wtórnej żylnej chorobie zakrzepowo - zatorowej i powikłaniom migotania przedsionków, takim jak udar. Skuteczność ksymelagatranu w tych wskazaniach została dobrze udokumentowana, z wyjątkiem migotania przedsionków niezastawkowego.
Zaletą, zgodnie z wczesnymi doniesieniami producenta, było to, że można go było przyjmować doustnie bez monitorowania jego właściwości przeciwkrzepliwych. To odróżniałoby go od warfaryny i heparyny , które wymagają monitorowania odpowiednio międzynarodowego współczynnika znormalizowanego (INR) i czasu częściowej tromboplastyny (PTT). Wadą rozpoznaną wcześnie był brak antidotum na wypadek wystąpienia ostrego krwawienia, podczas gdy warfarynę można antagonizować za pomocą koncentratu kompleksu protrombiny i/lub witaminy K i heparyny za pomocą siarczanu protaminy .
Skutki uboczne
Ximelagatran był ogólnie dobrze tolerowany w populacjach objętych badaniem, ale u niewielkiej części (5–6%) wystąpił podwyższony poziom enzymów wątrobowych , co skłoniło FDA do odrzucenia wstępnego wniosku o zatwierdzenie w 2004 r. Dalsze prace nad nim przerwano w 2006 r. po doniesieniach o hepatotoksyczność. Późniejsza analiza danych z badań klinicznych fazy 2 przy użyciu modelowania wartości ekstremalnych (patrz teoria wartości ekstremalnych ) wykazała, że można było przewidzieć podwyższone poziomy enzymów wątrobowych obserwowane w badaniach klinicznych fazy 3; gdyby było to wówczas znane, mogło to wpłynąć na decyzje dotyczące przyszłego rozwoju związku.
Chemicznie odmienna, ale farmakologicznie podobna substancja, AZD-0837 , została opracowana przez Aztrazeneca do podobnych wskazań. Jest prolekiem silnego, konkurencyjnego, odwracalnego inhibitora wolnej i związanej z fibryną trombiny o nazwie ARH0637 . Rozwój AZD-0837 został przerwany. Ze względu na stwierdzone ograniczenie długoterminowej stabilności produktu leczniczego AZD-0837 o przedłużonym uwalnianiu, w 2010 r. po 2 latach przedwcześnie zamknięto badanie kontrolne ASSURE dotyczące zapobiegania udarom mózgu u pacjentów z niezastawkowym migotaniem przedsionków. Wystąpiła również liczebnie wyższa śmiertelność wobec warfaryny. W badaniu II fazy dotyczącym AF średnie stężenie kreatyniny w surowicy wzrosło o około 10% w stosunku do wartości wyjściowych u pacjentów leczonych AZD-0837, które powróciły do wartości wyjściowych po zaprzestaniu leczenia.

