Interakcja agostyczna - Agostic interaction
Oddziaływanie agostyczne to termin w chemii metaloorganicznej dla interakcji koordynacyjnie nienasyconego metalu przejściowego z wiązaniem CH , gdy dwa elektrony zaangażowane w wiązanie CH wchodzą na pusty orbital d metalu przejściowego, co powoduje trzycentrowe wiązanie dwuelektronowe . Proponuje się, aby wiele przemian katalitycznych, np. addycja oksydacyjna i eliminacja redukcyjna , przebiegało przez związki pośrednie o oddziaływaniu agostycznym. Oddziaływania agostyczne obserwuje się w całej chemii metaloorganicznej w ligandach alkilowych, alkilidenowych i polienylowych.
Historia
Termin agostyczny, wywodzący się ze starożytnego greckiego słowa oznaczającego „trzymać się blisko siebie”, został ukuty przez Maurice'a Brookharta i Malcolma Greena , na sugestię klasyka Jaspera Griffina , w celu opisania tej i wielu innych interakcji między metalem przejściowym a metalem przejściowym. Wiązanie C-H . Często takie oddziaływania agostyczne obejmują grupy alkilowe lub arylowe, które są utrzymywane blisko centrum metalu przez dodatkowe wiązanie a.
Krótkie interakcje pomiędzy podstawnikami węglowodorowymi a koordynacyjnie nienasyconymi kompleksami metali notowano od lat 60. XX wieku. Na przykład w dichlorku tris( trifenylofosfiny ) rutenu obserwuje się krótkie oddziaływanie między centrum rutenu (II) a atomem wodoru w pozycji orto jednego z dziewięciu pierścieni fenylowych. Kompleksy borowodorku opisano przy użyciu trzycentrowego modelu wiązania dwuelektronowego .
Charakter oddziaływania został zapowiedziany w chemii grup głównych w chemii strukturalnej trimetyloglinu .
Charakterystyka więzi agostycznych
Oddziaływania agostyczne najlepiej demonstruje krystalografia . Dane z dyfrakcji neutronowej wykazały, że odległości wiązań C-H i M┄H są o 5-20% dłuższe niż oczekiwano dla izolowanych wodorków metali i węglowodorów. Odległość między metalem a wodorem wynosi zwykle 1,8-2,3 Å , a kąt M┄H-C mieści się w zakresie 90°-140°. Obecność 1 H NMR sygnału, który jest przesunięty w kierunku bramki ze zwykłej aryl lub alkan, często regionie zazwyczaj przypisanego wodorku ligandy. Stała sprzężenia 1 J CH jest zazwyczaj obniżona do 70-100 Hz w porównaniu do 125 Hz oczekiwanego dla normalnego wiązania węgiel-wodór sp 3 .
Siła wiązania
Na podstawie badań doświadczalnych i obliczeniowych stabilizację wynikającą z oddziaływania agostycznego szacuje się na 10–15 kcal/mol. Ostatnie obliczenia wykorzystujące stałe podatności wskazują na słabszą stabilizację (<10 kcal/mol). Zatem oddziaływania agostyczne są silniejsze niż większość wiązań wodorowych . Wiązania agostyczne czasami odgrywają rolę w katalizie, zwiększając „sztywność” w stanach przejściowych. Na przykład w katalizie Zieglera-Natty wysoce elektrofilowe centrum metalu ma agostyczne interakcje z rosnącym łańcuchem polimeru. Ta zwiększona sztywność wpływa na stereoselektywność procesu polimeryzacji.
Powiązane interakcje wiążące

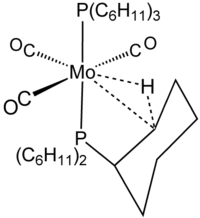
Termin „agostyk” jest zarezerwowany dla opisania dwuelektronowych, trójośrodkowych oddziaływań wiązań między węglem, wodorem i metalem. Dwuelektronowych trzy środek wiążący jest wyraźnie powiązano z kompleksowania H 2 , na przykład w W (CO) 3 (PCy 3 ) 2 H 2 , który jest ściśle związany z agostic złożone pokazane na rysunku. Silan wiąże się z centrami metali często poprzez oddziaływania agostykopodobne, trójcentryczne Si┄H-M. Ponieważ jednak te interakcje nie zawierają węgla, nie są klasyfikowane jako agostyczne.
Więzy anagostyczne
Pewne oddziaływania M┄H-C nie są klasyfikowane jako agostyczne, ale są określane terminem anagostyczne . Oddziaływania anagostyczne mają charakter bardziej elektrostatyczny. W zakresie struktur oddziaływań anagostycznych odległości M┄H i kąty M┄H−C mieszczą się odpowiednio w przedziałach 2,3–2,9 Å i 110–170.
Funkcjonować
Oddziaływania agostyczne pełnią kluczową funkcję w polimeryzacji i stereochemii alkenów , jak również w insercji migracyjnej .

