Silylen - Silylene
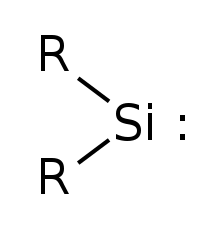 Najprostszy silylen ma R=wodór
|
|

|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Silylen
|
|
|
Systematyczna nazwa IUPAC
Syliliden |
|
| Inne nazwy
Krzemionek wodoru (-II) Silicene |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
|
Identyfikator klienta PubChem
|
|
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| H 2 Si | |
| Masa cząsteczkowa | 30,101 g·mol -1 |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Silylene jest związek chemiczny o wzorze SiH 2 . Jest to krzemowy analog metylenu , najprostszego karbenu . Silylen jest stabilną cząsteczką jako gaz, ale po kondensacji szybko reaguje dwucząsteczkowo. W przeciwieństwie do karbenów, które mogą występować w stanie singletowym lub tripletowym , silylen (i wszystkie jego pochodne) są singletami.
Silyleny są formalnymi pochodnymi silylenu z wodorami zastąpionymi innymi podstawnikami. Większość przykładów wyposażone amidowe (nr 2 ) lub grupy alkilo / arylowe. Jako reaktywne produkty pośrednie zaproponowano silyleny . Są to analogi karbenów .
Synteza i właściwości
Silylenes są na ogół syntetyzowane przez termolizę lub fotolizę z polisilany przez krzem reakcji atomu ( wstawiania , addycji lub poboru) poprzez pirolizę z silanów , albo przez redukcję 1,1-dihalosilane. Od dawna zakładano, że konwersja metalicznego Si do czterowartościowych związków krzemu odbywa się poprzez pośrednie silylenowe:
- Si + CI 2 → SiCU 2
- SiCU 2 + CI 2 → SiCU 4
Podobne rozważania dotyczą procesu bezpośredniego , tj. reakcji chlorku metylu i krzemu w masie.
Wczesne obserwacje silylenów obejmowały wytwarzanie dimetylosililenu przez odchlorowanie dimetylodichlorosilanu :
- SiCl 2 (CH 3 ) 2 + 2 K → Si(CH 3 ) 2 + 2 KCl
Tworzenie dimetylosililenu wykazano przez przeprowadzenie dechloracji w obecności trimetylosilanu , przy czym uwięzionym produktem jest pentametylodisilan:
- Si(CH 3 ) 2 + HSi(CH 3 ) 3 → (CH 3 ) 2 Si(H)-Si(CH 3 ) 3
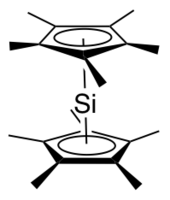
Izolowany w temperaturze pokojowej N -heterocykliczny silylen to N,N'- di - tert -butylo-1,3-diaza-2-silacyklopent-4-en-2-yliden, po raz pierwszy opisany w 1994 przez Michaela K. Denka i in. .
Centra α-amidowe stabilizują silyleny przez β-donację. Szeroko wykorzystywana jest dehalogenacja dwuhalogenków diorganokrzemu.
Powiązane reakcje
W jednym badaniu difenylosililen jest generowany przez błyskawiczną fotolizę trisilanu:
W tej reakcji difenylosililen jest wytłaczany z pierścienia trisila. Silylen można obserwować za pomocą spektroskopii UV przy 520 nm i jest on krótkotrwały z chemicznym okresem półtrwania wynoszącym dwie mikrosekundy . Dodano metanolu działa jako pułapki chemicznym z drugim stałej szybkości rzędu od 13x10 9 moli -1 S -1 , która jest blisko kontroli dyfuzji.
Zobacz też
- Analogi karbenów
- N -heterocykliczny silylen
- Silènes , R2Si = Sir2
- Jony sililowe , protonowane silyleny


