Akrylonitryl - Acrylonitrile
|
|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Prop-2-enonitryl |
|||
| Inne nazwy | |||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| CZEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.003.152 |
||
| Numer WE | |||
| KEGG | |||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS | |||
| UNII | |||
| Numer ONZ | 1093 | ||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 3 H 3 N | |||
| Masa cząsteczkowa | 53,064 g·mol -1 | ||
| Wygląd | Bezbarwna ciecz | ||
| Gęstość | 0,81 g/cm 3 | ||
| Temperatura topnienia | -84 ° C (-119 ° F; 189 K) | ||
| Temperatura wrzenia | 77 ° C (171 ° F; 350 K) | ||
| 70g/L | |||
| log P | 0,19 | ||
| Ciśnienie pary | 83 mmHg | ||
| Zagrożenia | |||
| Główne zagrożenia |
palny reaktywny potencjalny toksyczny zawodowy czynnik rakotwórczy |
||
| Arkusz danych dotyczących bezpieczeństwa | ICSC 0092 | ||
| NFPA 704 (ognisty diament) | |||
| Temperatura zapłonu | -1°C; 30°C; 272 tys | ||
| 471 ° C (880 ° F; 744 K) | |||
| Granice wybuchowości | 3–17% | ||
| Dawka lub stężenie śmiertelne (LD, LC): | |||
|
LC 50 ( mediana stężenia )
|
500 ppm (szczur, 4 godz.) 313 ppm (mysz, 4 godz.) 425 ppm (szczur, 4 godz.) |
||
|
LC Lo ( najniższa opublikowana )
|
260 ppm (królik, 4 godz.) 575 ppm (świnka morska, 4 godz.) 636 ppm (szczur, 4 godz.) 452 ppm (człowiek, 1 godz.) |
||
| NIOSH (limity ekspozycji dla zdrowia w USA): | |||
|
PEL (dopuszczalne)
|
TWA 2 ppm C 10 ppm [15 minut] [skóra] | ||
|
REL (zalecane)
|
Ca TWA 1 ppm C 10 ppm [15 minut] [skóra] | ||
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
85 ppm | ||
| Związki pokrewne | |||
|
Powiązane nitryle
|
acetonitryl propionitryl |
||
|
Związki pokrewne
|
kwas akrylowy akroleina |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
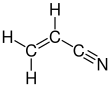
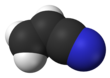
Akrylonitryl jest związkiem organicznym o wzorze CH 2 CHCN. Jest to bezbarwna, lotna ciecz, chociaż próbki handlowe mogą być żółte z powodu zanieczyszczeń. Ma ostry zapach czosnku lub cebuli. Pod względem struktury molekularnej składa się z grupy winylowej połączonej z nitrylem . Jest ważnym monomerem do produkcji użytecznych tworzyw sztucznych, takich jak poliakrylonitryl . Jest reaktywny i toksyczny w niskich dawkach. Akrylonitryl został po raz pierwszy zsyntetyzowany przez francuskiego chemika Charlesa Moureu (1863-1929) w 1893 roku.
Występowanie
Akrylonitryl nie powstaje naturalnie w atmosferze Ziemi. Jednak może wystąpić na poziomie do 0,11 ppm w zakładach przemysłowych. Utrzymuje się w powietrzu do tygodnia. Rozkłada się w reakcji z tlenem i rodnikiem hydroksylowym, tworząc cyjanek formylu i formaldehyd . Akrylonitryl jest szkodliwy dla organizmów wodnych .
Akrylonitryl wykryto w atmosferze Tytana , księżyca Saturna . Symulacje komputerowe sugerują, że na Tytanie istnieją takie warunki, że związek może tworzyć struktury podobne do błon komórkowych i pęcherzyków na Ziemi, zwane azotosomami.
Produkcja
Akrylonitryl jest wytwarzany przez katalityczną ammoxidation z propylenu , znanych również jako SOHIO procesu. W 2002 r. światowe moce produkcyjne oszacowano na 5 mln ton rocznie. Acetonitryl i cyjanowodór są istotnymi produktami ubocznymi, które są odzyskiwane na sprzedaż. W rzeczywistości niedobór acetonitrylu w latach 2008–2009 spowodowany był spadkiem zapotrzebowania na akrylonitryl.
- 2 CH 3 −CH=CH 2 + 2 NH 3 + 3 O 2 → 2 CH 2 =CH–C≡N + 6 H 2 O
W procesie SOHIO propylen , amoniak i powietrze (utleniacz) przepuszczane są przez reaktor ze złożem fluidalnym zawierający katalizator w temperaturze 400–510 °C i 50–200 kPa g . Reagenty przechodzą przez reaktor tylko raz, zanim zostaną ostudzone w wodnym kwasie siarkowym. Nadmiar propylenu, tlenku węgla, dwutlenku węgla i diazotu, które nie rozpuszczają się, są odprowadzane bezpośrednio do atmosfery lub spalane. Wodny roztwór składa się z akrylonitrylu, acetonitrylu, kwasu cyjanowodorowego i siarczanu amonu (z nadmiaru amoniaku). Kolumna do odzyskiwania usuwa wodę w masie, a akrylonitryl i acetonitryl oddziela się przez destylację. W przeszłości jednym z pierwszych skutecznych katalizatorów bizmutu fosfomolibdenianu (Bi 9 PMO 12 O 52 ) wspiera się na krzemionce jako katalizatora heterogenicznego. Od tego czasu dokonano dalszych ulepszeń.
Powstające szlaki przemysłowe
Opracowywane są różne szlaki zielonej chemii do syntezy akrylonitrylu z surowców odnawialnych, takich jak biomasa lignocelulozowa , glicerol (z produkcji biodiesla ) lub kwas glutaminowy (który sam może być wytwarzany z surowców odnawialnych). Droga lignocelulozowa obejmuje fermentację biomasy do kwasu propionowego i kwasu 3-hydroksypropionowego, które są następnie przekształcane w akrylonitryl poprzez odwodnienie i amoksydację . Droga glicerolowa zaczyna się od pirolizy do akroleiny , która ulega amoksydacji do akrylonitrylu. Droga kwasu glutaminowego wykorzystuje dekarboksylację oksydacyjną do kwasu 3-cyjanopropanowego, a następnie dekarbonylację-eliminację do akrylonitrylu. Spośród nich droga glicerolowa jest powszechnie uważana za najbardziej opłacalną, chociaż obecne metody nadal nie są w stanie konkurować z procesem SOHIO pod względem kosztów.
Zastosowania
Akrylonitryl jest używany głównie jako monomer do wytwarzania poliakrylonitrylu , homopolimeru lub kilku ważnych kopolimerów , takich jak styren-akrylonitryl (SAN), akrylonitryl-butadien-styren (ABS), akrylonitryl-akrylan styrenu (ASA) i inne kauczuki syntetyczne, takie jak butadien-akrylonitryl (NBR). Hydrodimeryzacja akrylonitrylu daje adyponitryl , stosowany w syntezie niektórych nylonów :
- 2 CH 2 = CHCN + 2 e − + 2 H + → NCCH 2 CH 2 CH 2 CH 2 CN
Niewielkie ilości są również używane jako fumigant . Akrylonitryl i pochodne, takie jak 2-chloroakrylonitryl, są dienofilami w reakcjach Dielsa-Aldera . Akrylonitryl jest również prekursorem w przemysłowej produkcji akryloamidu i kwasu akrylowego .
Efekty zdrowotne
Akrylonitryl jest wysoce łatwopalny i toksyczny w małych dawkach. Ulega wybuchowej polimeryzacji . Z palącego się materiału wydzielają się opary cyjanowodoru i tlenki azotu . Został sklasyfikowany jako rakotwórczy klasy 2B (prawdopodobnie rakotwórczy) przez Międzynarodową Agencję Badań nad Rakiem (IARC), a u pracowników narażonych na wysoki poziom akrylonitrylu przenoszonego drogą powietrzną diagnozuje się raka płuc częściej niż u reszty populacji. Akrylonitryl nasila raka w testach z zastosowaniem dużych dawek u samców i samic szczurów i myszy oraz indukuje apoptozę ludzkich mezenchymalnych komórek macierzystych pępowiny .
Szybko odparowuje w temperaturze pokojowej (20 °C), osiągając niebezpieczne stężenia; podrażnienie skóry, podrażnienie dróg oddechowych i podrażnienie oczu to bezpośrednie skutki tego narażenia. Drogi narażenia ludzi obejmują emisje , spaliny samochodowe i dym papierosowy, który może narazić człowieka bezpośrednio, jeśli wdycha lub pali. Drogi narażenia obejmują wdychanie, doustne i do pewnego stopnia wchłanianie przez skórę (testowane na ochotnikach i badaniach na szczurach). Powtarzające się narażenie powoduje uczulenie skóry i może powodować uszkodzenie ośrodkowego układu nerwowego i wątroby .
Istnieją dwa główne procesy wydalania akrylonitrylu. Podstawową metodą jest wydalanie z moczem, gdy akrylonitryl jest metabolizowany przez bezpośrednie sprzęganie z glutationem . Inna metoda polega na enzymatycznym przekształceniu akrylonitrylu w tlenek 2-cyjanoetylenu, który wytwarza końcowe produkty cyjankowe , które ostatecznie tworzą tiocyjanian , który jest wydalany z moczem. Narażenie można zatem wykryć poprzez pobranie krwi i pobranie próbki moczu.
Bibliografia
Linki zewnętrzne
- Krajowa Inwentaryzacja Zanieczyszczeń – Akrylonitryl
- Porównanie możliwych zagrożeń rakowych wynikających z narażenia ludzi na czynniki rakotwórcze u gryzoni
- Akrylonitryl – Zintegrowany System Informacji o Ryzyku , Agencja Ochrony Środowiska USA
- CDC – Kieszonkowy przewodnik NIOSH po zagrożeniach chemicznych – Akrylonitryl
- Tabela OSHA Z-1 dla zanieczyszczeń powietrza