Nadrenian amonu - Ammonium perrhenate

|
|

|
|
| Nazwy | |
|---|---|
| Inne nazwy
Nadrenian amonu,
Nadrenian (VII) amonu |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.033.690 |
| Numer WE | |
|
PubChem CID
|
|
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| NH 4 ReO 4 | |
| Masa cząsteczkowa | 268,2359 g / mol |
| Gęstość | 3,97 g / cm 3 , stałe |
| Temperatura topnienia | ° C |
| 2,8 g / 100 ml (0 ° C), 6,2 g / 100 ml (20 ° C), 12,0 g / 100 ml (40 ° C), 20,7 g / 100 ml (60 ° C), 32,3 g / 100 ml ( 80 ° C), 39,1 g / 100 ml (90 ° C) | |
| Struktura | |
| scheelite | |
| Nie dotyczy | |
| Zagrożenia | |
| Temperatura zapłonu | Nie palne |
| Związki pokrewne | |
|
Inne aniony
|
Manganian amonu ; nadtechnecjan amonu |
|
Inne kationy
|
Nadrenian sodu ; kwas nadrenowy |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Nadrenianu amonu (APR) jest amonu sól kwasu nadrenowego , NH 4 reo 4 . To jest najbardziej rozpowszechnioną formą, w której renu jest przedmiotem obrotu. Jest to biała, rozpuszczalna w wodzie sól. Po raz pierwszy został opisany wkrótce po odkryciu renu.
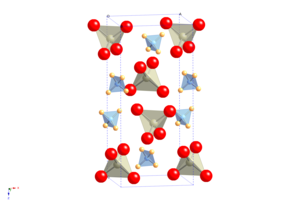
Struktura
Struktura krystaliczna APR jest strukturą scheelitu , w której kation atomowy jest zastąpiony kationem cząsteczkowym amonu. Podlega ona przemianom porządkującym w orientacji molekularnej podczas chłodzenia bez zmiany grupy przestrzennej, ale z wysoce anizotropową zmianą kształtu komórki elementarnej , co skutkuje niezwykłą właściwością posiadania dodatniego współczynnika temperatury i ciśnienia Re NQR .
NH 4 ReO 4 można uznać za prototypową strukturę rodziny scheelitów amonowych, do których należą nadtechnecjan (NH 4 TcO 4 ), nadjodan (NH 4 IO 4 ), tetrachlorotalan (NH 4 TlCl 4 ) i tetrachloroindat (NH 4 InCl 4 ).
Przygotowanie
Nadrenian amonu można wytwarzać z praktycznie wszystkich powszechnych źródeł renu. Metal, tlenki i siarczki można utlenić kwasem azotowym, a otrzymany roztwór potraktować wodnym roztworem amoniaku. Alternatywnie wodny roztwór Re 2 O 7 można potraktować amoniakiem, a następnie poddać krystalizacji.
Reakcje
Czysty proszek renu można wytworzyć z APR poprzez ogrzewanie go w obecności wodoru :
- 2 NH 4 ReO 4 + 7 H 2 → 2 Re + 8 H 2 O + 2 NH 3
Ogrzewanie należy przeprowadzać powoli, ponieważ nadrenian amonu rozkłada się do lotnego Re 2 O 7 począwszy od 250 ° C. Po podgrzaniu w szczelnie zamkniętej probówce w temperaturze 500 ° C, APR rozkłada się do dwutlenku renu :
- 2NH 4 ReO 4 → 2ReO 2 + N 2 + 4 H 2 O
Bibliografia
- ^ Noddack, J .; Noddack, W. (1929). „Die Sauerstoffverbindungen des Rheniums”. Zeitschrift für anorganische und allgemeine Chemie . 181 (6): 1–37. Bibcode : 1929NW ..... 17 ... 93N . doi : 10.1002 / zaac.19291810102 .
- ^ a b I. P. Swainson i RJC Brown (1997). „Udoskonalenie struktury nadrenianu amonu za pomocą modelu pseudospinowego orientacji jonów amonowych”. Acta Crystallographica . B53 : 76–81. doi : 10.1107 / S0108768196011160 .
- ^ RJC Brown i SL Segel (1977). „ 187 Re, 14 N i 2 H jądrowych sprzężeń kwadrupolowych w NH 4 ReO 4 : Dowody na możliwą przemianę fazową”. Journal of Chemical Physics . 67 (7): 3163–7. Bibcode : 1977JChPh..67.3163B . doi : 10,1063 / 1,435229 .
- ^ a b c O. Glemser "Ammonium Perrhenate" w Handbook of Preparative Inorganic Chemistry , wyd. Pod redakcją G. Brauera, Academic Press, 1963, Nowy Jork. vol. 1. p. 1476–85.
- ^ Richard J. Thompson (1966). „Nadrenian amonu”. Syntezy nieorganiczne . 8 : 171–173. doi : 10.1002 / 9780470132395.ch44 . ISBN 9780470132395 .
- Wm. T. Smith, S. Harmon Long (1948). „Sole kwasu perhenicowego. I. Metale alkaliczne i amon”. Dziennik Amerykańskiego Towarzystwa Chemicznego . 70 (1): 354–356. doi : 10.1021 / ja01181a110 .