Dendralen - Dendralene
Dendralene jest dyskretnym acykliczny wzajemnie skoniugowane polienowy . Najprostszym dendralenem jest buta-1,3-dien (1) lub [2]dendralen, a następnie [3]dendralen (2), [4]dendralen (3) i [5]dendralen (4) i tak dalej. [2]dendralen (butadien) jest jedynym, który nie jest skoniugowany krzyżowo.
Nazwa dendralen jest połączona ze słowami dendrymer , liniowy i alken . Wyższe dendraleny są przedmiotem zainteresowania naukowego, ponieważ otwierają szeroką gamę nowych związków organicznych ze stosunkowo prostego prekursora, zwłaszcza w chemii Dielsa-Aldera . Ich cykliczne odpowiedniki są trafnie nazywane radialenami .
Synteza
Winylobutadien ([3]dendralen) został po raz pierwszy wytworzony w 1955 przez pirolizę trioctanu:
Związek ten reaguje z dwoma równoważnikami bezwodnika maleinowego w tandemowej reakcji DA:
Z benzochinonem produkt reakcji był liniowym polimerem.
Opisano kilka syntez podstawionych [3]dendralenów, jedną poprzez allen , jedną poprzez reakcję Hornera-Wadswortha-Emmonsa , jedną poprzez reakcję sprzęgania krzyżowego i jedną z węglanu allilu.
Jedna droga syntezy do [4]dendralenu zaczyna się od chloroprenu . Związek ten jest przekształcany w odczynnik Grignarda przez działanie metalicznego magnezu, który jest następnie poddawany reakcji z chlorkiem miedzi(I) do związku pośredniego miedzioorganicznego, który z kolei jest dimeryzowany przy użyciu chlorku miedzi(II) w reakcji sprzęgania utleniającego, dając dimer butadienu o nazwie [ 4]dendralen.
Opisano strukturę molekularną [4]dendralenu w fazie gazowej
Związek [8]-dendralenu został zgłoszony w 2009 roku:
w kolejnym sprzężeniu Kumada–Tamao–Corriu i Negishi .
W 2016 r. zgłoszono serię od [9] do [12]-dendralenów
Nieruchomości
Dendraleny o parzystej strukturze (np. [6]dendralen, [8]dendralen) mają tendencję do zachowywania się jak łańcuchy odłączonych i izolowanych jednostek dienowych . Ultrafioletowe absorpcji maksima równa tej samej butadienu. Dendraleny z nieparzystą liczbą jednostek alkenowych są bardziej reaktywne ze względu na obecność korzystnych konformacji s-cis dienu, a reakcje Dielsa-Aldera zachodzą łatwiej z preferencją końców.
Reakcje
Dzięki prostym dienofilom dendrale mogą zapewnić szybki dostęp do złożonych cząsteczek w reakcjach Dielsa-Aldera . Zgłoszono kilka schematów reakcji
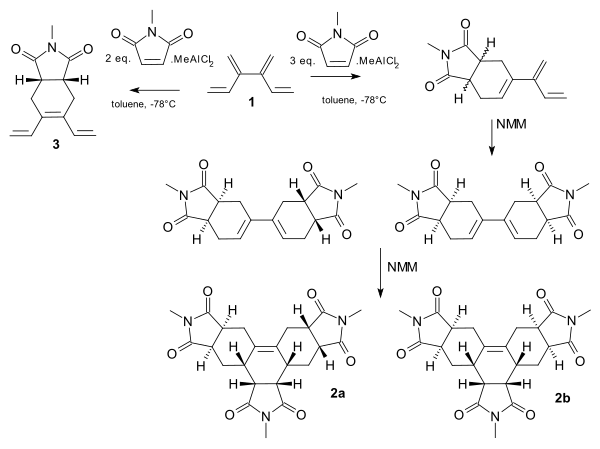
[4]dendralen wykazuje tandemową reakcję Dielsa-Aldera z dienofilowym N-metylo-maleimidem (NMM). Pełna selektywność względem miejsca jest możliwa dzięki dodaniu metylodichloroglinu kwasu Lewisa . Z jednym zestawem wstępnego mieszania i 2 równoważnikami NMM, centralna grupa dienowa jest ukierunkowana na monoaddukt 3 . Z innym zestawem i większą ilością dienofila, grupy końcowe reagują i reakcja przebiega od monoadduktu do trisadduktów 2 i 2b .
Jeden z wariantów reakcji cyklopropanowania do klasy związków nazywanych ivyanes z omawianym syntezy w reakcji Simmonsa-Smitha ( dietylowy cynk / kwas trifluorooctowy ) w ciągu pierwszych 6 osób. Te 1,1-oligocyklopropany są stabilne (z wyjątkiem wystawienia na działanie kwasów) i mają duże ciepło spalania z [6]ivyanem przewyższające ciepło cubane . Łańcuchy oligocyklopropanowe przyjmują konformację helikalną. W przypadku [3]dendralenu opisano fotochemiczną reakcję cyklizacji
Pochodne
Opisano bicykliczny [4] związek dendralenowy.




![[4]Schemat syntezy dendralenu z chloroprenu](https://upload.wikimedia.org/wikipedia/commons/thumb/4/40/4-dendralene.svg/569px-4-dendralene.svg.png)
![[8]-synteza dendralenu](https://upload.wikimedia.org/wikipedia/commons/thumb/9/9d/8-dendralene.svg/411px-8-dendralene.svg.png)