Terapia przeciwciałem monoklonalnym - Monoclonal antibody therapy
Terapia przeciwciałem monoklonalnym jest formą immunoterapii, która wykorzystuje przeciwciała monoklonalne (mAb) do monoswoistego wiązania się z niektórymi komórkami lub białkami . Celem jest, aby ta terapia stymulowała układ odpornościowy pacjenta do atakowania tych komórek. Alternatywnie, w radioimmunoterapii dawka radioaktywna lokalizuje docelową linię komórkową, dostarczając śmiertelne dawki chemiczne. Ostatnio zastosowano przeciwciała do wiązania się z cząsteczkami zaangażowanymi w regulację komórek T w celu usunięcia szlaków hamujących, które blokują odpowiedzi komórek T. Jest to znane jako terapia punktów kontrolnych układu odpornościowego .
Możliwe jest wytworzenie mAb, które jest specyficzne dla prawie każdego celu zewnątrzkomórkowego /powierzchni komórki. Trwają prace badawczo-rozwojowe nad stworzeniem przeciwciał na choroby (takie jak reumatoidalne zapalenie stawów , stwardnienie rozsiane , choroba Alzheimera , Ebola i różne rodzaje nowotworów ).
Struktura i funkcja przeciwciał
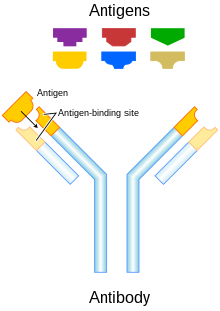
Przeciwciała immunoglobuliny G ( IgG ) są dużymi cząsteczkami heterodimerycznymi , około 150 kDa i składają się z dwóch rodzajów łańcucha polipeptydowego , zwanego ciężkim (~50 kDa) i lekkim (~25 kDa). Dwa typy łańcuchów lekkich to kappa (κ) i lambda (λ). Przez rozszczepienie enzymem papainą , część Fab ( wiązanie fragmentu z antygenem ) można oddzielić od części Fc ( stała fragmentu ) cząsteczki. Fragmenty Fab zawierają domeny zmienne, które składają się z trzech hiperzmiennych domen aminokwasowych przeciwciała odpowiedzialnych za specyficzność przeciwciała osadzonych w regionach stałych. Cztery znane podklasy IgG biorą udział w cytotoksyczności komórkowej zależnej od przeciwciał . Przeciwciała są kluczowym elementem adaptacyjnej odpowiedzi immunologicznej , odgrywając kluczową rolę zarówno w rozpoznawaniu obcych antygenów, jak i stymulacji odpowiedzi immunologicznej na nie. Pojawienie się technologii przeciwciał monoklonalnych umożliwiło uzyskanie przeciwciał przeciwko specyficznym antygenom prezentowanym na powierzchni nowotworów. Przeciwciała monoklonalne mogą być nabywane w układzie odpornościowym poprzez odporność bierną lub odporność czynną . Zaletą terapii aktywnymi przeciwciałami monoklonalnymi jest fakt, że układ odpornościowy będzie wytwarzał przeciwciała przez długi czas, a jedynie krótkotrwałe podawanie leku w celu wywołania tej odpowiedzi. Jednak odpowiedź immunologiczna na niektóre antygeny może być niewystarczająca, zwłaszcza u osób starszych. Dodatkowo mogą wystąpić niepożądane reakcje tych przeciwciał z powodu długotrwałej odpowiedzi na antygeny. Bierna terapia przeciwciałami monoklonalnymi może zapewnić stałe stężenie przeciwciał i kontrolować reakcje niepożądane poprzez zaprzestanie podawania. Jednak wielokrotne podawanie i wynikający z tego wyższy koszt tej terapii są głównymi wadami.
Terapia przeciwciałem monoklonalnym może okazać się korzystna w przypadku raka , chorób autoimmunologicznych i zaburzeń neurologicznych, które powodują degenerację komórek organizmu, takich jak choroba Alzheimera . Terapia przeciwciałem monoklonalnym może wspomóc układ odpornościowy, ponieważ wrodzony układ odpornościowy reaguje na napotkane czynniki środowiskowe, dyskryminując obce komórki z komórek ciała. Dlatego też komórki nowotworowe , które szybko się namnażają, lub komórki organizmu, które umierają, co następnie powoduje problemy fizjologiczne, nie są na ogół konkretnie kierowane przez układ odpornościowy, ponieważ komórki nowotworowe są komórkami własnymi pacjenta. Jednak komórki nowotworowe są wysoce nieprawidłowe i wiele z nich wykazuje nietypowe antygeny . Niektóre takie antygeny nowotworowe są nieodpowiednie dla typu komórki lub jej środowiska. Przeciwciała monoklonalne mogą atakować komórki nowotworowe lub nieprawidłowe komórki w ciele, które są rozpoznawane jako komórki ciała, ale osłabiają zdrowie.
Historia

Immunoterapia rozwinęła się w latach 70. po odkryciu struktury przeciwciał i opracowaniu technologii hybrydom , która dostarczyła pierwszego wiarygodnego źródła przeciwciał monoklonalnych . Te postępy pozwoliły na specyficzne ukierunkowanie na nowotwory zarówno in vitro, jak i in vivo . Wstępne badania nad nowotworami złośliwymi wykazały, że terapia mAb jest ograniczona i generalnie krótkotrwała w przypadku nowotworów krwi. Leczenie musiało być również dostosowane do każdego pacjenta z osobna, co było niewykonalne w rutynowych warunkach klinicznych.
Cztery główne typy przeciwciał, które zostały opracowane, to mysie , chimeryczne , humanizowane i ludzkie. Przeciwciała każdego typu są rozróżniane przyrostkami przy ich nazwie.
Mysi
Początkowymi przeciwciałami terapeutycznymi były mysie analogi (przyrostek -omab ). Przeciwciała te mają: krótki okres półtrwania in vivo (ze względu na tworzenie kompleksu immunologicznego ), ograniczoną penetrację do miejsc guza i niewystarczającą rekrutację funkcji efektorowych gospodarza. Przeciwciała chimeryczne i humanizowane generalnie zastąpiły je w zastosowaniach terapeutycznych przeciwciał. Zrozumienie proteomiki okazało się kluczowe w identyfikacji nowych celów nowotworowych.
Początkowo mysie przeciwciała uzyskano technologią hybrydom, za którą Jerne, Köhler i Milstein otrzymali nagrodę Nobla. Jednak odmienność między mysim i ludzkim układem odpornościowym doprowadziła do klinicznego niepowodzenia tych przeciwciał, z wyjątkiem pewnych szczególnych okoliczności. Główne problemy związane z przeciwciałami mysimi obejmowały zmniejszoną stymulację cytotoksyczności i tworzenie kompleksów po wielokrotnym podaniu, co skutkowało łagodnymi reakcjami alergicznymi, a czasami wstrząsem anafilaktycznym . Technologia hybrydoma została zastąpiona technologią rekombinacji DNA , transgenicznymi myszami i prezentacją fagową .
Chimeryczny i humanizowany
Aby zmniejszyć immunogenność mysich przeciwciał (ataki układu odpornościowego na przeciwciało), zmodyfikowano mysie cząsteczki w celu usunięcia zawartości immunogennej i zwiększenia wydajności immunologicznej. Zostało to początkowo osiągnięte przez produkcję przeciwciał chimerycznych (przyrostek -ximab) i humanizowanych (przyrostek -zumab ). Przeciwciała chimeryczne składają się z mysich regionów zmiennych połączonych z ludzkimi regionami stałymi. Pobranie sekwencji ludzkiego genu z łańcucha lekkiego kappa i łańcucha ciężkiego IgG1 daje przeciwciała, które w około 65% są ludzkie. Zmniejsza to immunogenność, a tym samym wydłuża okres półtrwania w surowicy .
Humanizowane przeciwciała są wytwarzane przez przeszczepienie mysich regionów hiperzmiennych na domenach aminokwasowych do ludzkich przeciwciał. Daje to cząsteczkę w około 95% pochodzenia ludzkiego. Humanizowane przeciwciała wiążą antygen znacznie słabiej niż rodzicielskie mysie przeciwciało monoklonalne, z odnotowanymi nawet kilkusetkrotnymi spadkami powinowactwa. Zwiększenie siły wiązania przeciwciało-antygen osiągnięto poprzez wprowadzenie mutacji do regionów determinujących dopasowanie (CDR), przy użyciu technik takich jak tasowanie łańcuchów, randomizacja regionów determinujących dopasowanie i przeciwciała z mutacjami w obrębie regionów zmiennych wywołanych przez podatną na błędy PCR , szczepy mutacyjne E. coli i mutageneza miejscowo-specyficzna .
Ludzkie przeciwciała monoklonalne
Ludzkie przeciwciała monoklonalne (sufiks -umab ) są wytwarzane przy użyciu transgenicznych myszy lub bibliotek fagowych poprzez przeniesienie genów ludzkiej immunoglobuliny do genomu mysiego i zaszczepienie myszy transgenicznej przeciwko pożądanemu antygenowi, co prowadzi do wytworzenia odpowiednich przeciwciał monoklonalnych. Mysie przeciwciała in vitro są w ten sposób przekształcane w całkowicie ludzkie przeciwciała.
Ciężkie i lekkie łańcuchy ludzkich białek IgG ulegają ekspresji w strukturalnych formach polimorficznych (allotypowych). Allotyp ludzkiej IgG jest jednym z wielu czynników, które mogą przyczyniać się do immunogenności.
Ukierunkowane warunki
Nowotwór
Przeciwnowotworowe przeciwciała monoklonalne mogą być skierowane przeciwko komórkom nowotworowym za pomocą kilku mechanizmów. Ramucirumab jest rekombinowanym ludzkim przeciwciałem monoklonalnym i jest stosowany w leczeniu zaawansowanych nowotworów złośliwych. W przypadku chłoniaka dziecięcego badania I i II fazy wykazały pozytywny efekt stosowania terapii przeciwciałami.
Choroby autoimmunologiczne
Przeciwciała monoklonalne stosowane w chorobach autoimmunologicznych obejmują infliksymab i adalimumab , które są skuteczne w reumatoidalnym zapaleniu stawów , chorobie Leśniowskiego-Crohna i wrzodziejącym zapaleniu jelita grubego dzięki ich zdolności do wiązania i hamowania TNF-α . Basiliximab i daklizumab hamują IL-2 na aktywowanych limfocytach T, a tym samym pomagają zapobiegać ostremu odrzuceniu przeszczepionej nerki. Omalizumab hamuje ludzką immunoglobulinę E (IgE) i jest przydatny w astmie alergicznej o nasileniu umiarkowanym do ciężkiego .
Choroba Alzheimera
Choroba Alzheimera (AD) jest wieloaspektowym, zależnym od wieku, postępującym zaburzeniem neurodegeneracyjnym i jest główną przyczyną demencji. Zgodnie z hipotezą amyloidową , akumulacja pozakomórkowych betapeptydów amyloidowych (Aβ) w płytkach poprzez oligomeryzację prowadzi do charakterystycznych stanów objawowych AD poprzez dysfunkcję synaptyczną i neurodegenerację. Wiadomo, że immunoterapia przez podawanie egzogennego przeciwciała monoklonalnego (mAb) leczy różne zaburzenia ośrodkowego układu nerwowego, takie jak AD, poprzez hamowanie oligomeryzacji Aβ, zapobiegając w ten sposób neurotoksyczności. Jednak mAb są duże dla pasywnych kanałów białkowych i dlatego są nieefektywne ze względu na barierę krew-mózg zapobiegającą przechodzeniu mAb do mózgu. Jednak hipoteza Peripheral Sink proponuje mechanizm, w którym mAb może nie musieć przekraczać bariery krew-mózg. Dlatego wiele badań naukowych jest prowadzonych na podstawie nieudanych prób leczenia AD w przeszłości.
Jednak szczepionki anty-Aβ mogą promować usuwanie płytek Aβ za pośrednictwem przeciwciał w modelach myszy transgenicznych z białkami prekursorowymi amyloidu (APP) i mogą zmniejszać zaburzenia funkcji poznawczych. Szczepionki mogą stymulować układ odpornościowy do wytwarzania własnych przeciwciał, w tym przypadku poprzez wprowadzenie Aβ do transgenicznych modeli zwierzęcych, co określa się mianem aktywnej immunizacji . Mogą również wprowadzać przeciwciała do modeli zwierzęcych, co jest znane jako immunizacja bierna . U myszy z ekspresją APP wykazano, że zarówno aktywna, jak i bierna immunizacja przeciwciał anty-Aβ jest skuteczna w usuwaniu blaszek miażdżycowych i może poprawiać funkcje poznawcze. Obecnie nie ma zatwierdzonych terapii przeciwciałami monoklonalnymi w chorobie Alzheimera, ale kilka prób klinicznych wykorzystujących metody biernej i aktywnej immunizacji poprzez opracowanie pewnych leków zatwierdzonych przez FDA jest obecnie w toku i oczekuje się, że przyniosą wyniki w ciągu kilku lat. Wdrożenie tych leków ma miejsce na początku AD. Trwają inne badania i opracowywanie leków do wczesnej interwencji i profilaktyki AD. Różne leki, które są przedmiotem badań w leczeniu AD, obejmują Bapineuzumab, Solanezumab, Gautenerumab i BAN2401.
Bapineuzumab
Bapineuzumab, humanizowane mAb anty-Aβ, jest skierowane przeciwko końcowi N Aβ. Badania kliniczne fazy II bapineuzumabu u pacjentów z AD o nasileniu łagodnym do umiarkowanego wykazały zmniejszenie stężenia Aβ w mózgu. Jednak u pacjentów ze zwiększonym poziomem nosicieli apolipoproteiny (APOE) e4 leczeniu bapineuzumabem towarzyszy również obrzęk naczyniopochodny , stan cytotoksyczny, w którym bariera krew-mózg została naruszona , co wpływa na istotę białą z powodu nadmiernego gromadzenia się płynu z naczyń włosowatych w przestrzeniach wewnątrzkomórkowych i zewnątrzkomórkowych mózg. W badaniach klinicznych III fazy leczenie bapineuzumabem wiąże się ze zmniejszoną szybkością akumulacji Aβ w mózgu u pacjentów z APOE e4 i brakiem istotnego zmniejszenia stężenia Aβ u pacjentów z APOE e4 i pacjentów bez APOE e4. Dlatego stężenie blaszki Aβ nie uległo zmniejszeniu i nie ma znaczących korzyści klinicznych w funkcjonowaniu poznawczym. Bapineuzumab przerwano po niepowodzeniu w badaniu klinicznym III fazy.
Solanezumab
Solanezumab, mAb anty-Aβ, jest skierowany na N-koniec Aβ. W badaniach klinicznych fazy I i fazy II leczenie solanezumabem powodowało podwyższenie poziomu Aβ w płynie mózgowo-rdzeniowym , tym samym wykazując zmniejszone stężenie blaszek Aβ. Ponadto nie ma żadnych związanych z tym niepożądanych skutków ubocznych. Badania kliniczne III fazy Solanezumabu przyniosły istotne zmniejszenie zaburzeń poznawczych u pacjentów z łagodną AD, ale nie u pacjentów z ciężką AD. Jednak stężenie Aβ nie zmieniło się znacząco wraz z innymi biomarkerami AD, w tym ekspresją fosfo-tau i objętością hipokampa. Obecnie trwają badania kliniczne III fazy.
BAN2401
BAN2401 to humanizowane mAb, które selektywnie celuje w toksyczne rozpuszczalne protofibryle Aβ, a terapia jest obecnie poddawana badaniu klinicznym fazy 3, które ma zostać zakończone w 2022 roku.
Badania prewencyjne
Niepowodzenie kilku leków w badaniach klinicznych fazy III doprowadziło do zapobiegania AD i wczesnej interwencji w przypadku rozpoczęcia leczenia AD. Bierne leczenie mAb anty-Aβ można zastosować do prewencyjnych prób modyfikacji progresji AD, zanim spowoduje ona rozległe uszkodzenie mózgu i objawy. Trwają badania z zastosowaniem leczenia mAb dla pacjentów z pozytywnymi genetycznymi czynnikami ryzyka i starszych pacjentów z pozytywnymi objawami AD. Obejmuje to leczenie anty-AB w bezobjawowej chorobie Alzheimera (A4), inicjatywę zapobiegania chorobie Alzheimera (API) i DIAN-TU. Badanie A4 na starszych osobach, które mają dodatnie wskaźniki AD, ale ujemne czynniki ryzyka genetycznego, będą testować Solanezumab w badaniach klinicznych fazy III, jako kontynuacja poprzednich badań Solanezumabu. Projekt DIAN-TU, uruchomiony w grudniu 2012 r., skupia się na młodych pacjentach, u których stwierdzono mutacje genetyczne, które stanowią zagrożenie dla AD. W badaniu wykorzystano Solanezumab i Gautenerumab. Gautenerumab, pierwszy w pełni ludzki MAB, który preferencyjnie oddziałuje z oligomeryzowanymi płytkami Aβ w mózgu, spowodował znaczne zmniejszenie stężenia Aβ w badaniach klinicznych fazy I, zapobiegając tworzeniu się i tworzeniu płytek bez zmiany stężenia w osoczu mózgu. Obecnie prowadzone są badania kliniczne fazy II i III.
Rodzaje terapii
Radioimmunoterapia
Radioimmunoterapia (RIT) obejmuje zastosowanie mysich przeciwciał skoniugowanych radioaktywnie przeciwko antygenom komórkowym. Większość badań dotyczy ich zastosowania w chłoniakach , ponieważ są to nowotwory o dużej wrażliwości na promieniowanie. Aby ograniczyć ekspozycję na promieniowanie, wybrano mysie przeciwciała, ponieważ ich wysoka immunogenność sprzyja szybkiemu usuwaniu guza. Tositumomab jest przykładem stosowanym w chłoniaku nieziarniczym.
Enzymatyczna terapia prolekowa ukierunkowana na przeciwciała
Enzymatyczna terapia prolekowa ukierunkowana na przeciwciała (ADEPT) obejmuje zastosowanie przeciwciał monoklonalnych związanych z rakiem, które są połączone z enzymem aktywującym lek. Podawanie ogólnoustrojowe środka nietoksycznego powoduje konwersję przeciwciała do leku toksycznego, co skutkuje efektem cytotoksycznym, który może być ukierunkowany na komórki nowotworowe. Kliniczny sukces terapii ADEPT jest ograniczony.
Koniugaty przeciwciało-lek
Koniugaty przeciwciało-lek (ADC) to przeciwciała połączone z jedną lub większą liczbą cząsteczek leku. Zazwyczaj, gdy ADC spotyka komórkę docelową (np. komórkę rakową), uwalniany jest lek, który ją zabija. Wiele ADC jest w fazie rozwoju klinicznego. Od 2016 roku kilka zostało zatwierdzonych.
Terapia immunoliposomowa
Immunoliposomy to liposomy skoniugowane z przeciwciałem . Liposomy mogą przenosić leki lub terapeutyczne nukleotydy, a gdy są sprzężone z przeciwciałami monoklonalnymi, mogą być skierowane przeciwko komórkom nowotworowym. Immunoliposomów z powodzeniem stosowano in vivo do przenoszenia genów hamujących nowotwór do guzów przy użyciu fragmentu przeciwciała przeciwko ludzkiemu receptorowi transferyny . Tkankowo-specyficzne dostarczanie genów za pomocą immunoliposomów osiągnięto w tkance mózgu i raka piersi.
Terapia w punkcie kontrolnym
Terapia Checkpoint wykorzystuje przeciwciała i inne techniki w celu obejścia mechanizmów obronnych, których używają guzy do tłumienia układu odpornościowego. Każda obrona nazywana jest punktem kontrolnym. Terapie złożone łączą przeciwciała w celu stłumienia wielu warstw obronnych. Znane punkty kontrolne obejmują CTLA-4 kierowane przez ipilimumab, PD-1 kierowane przez niwolumab i pembrolizumab oraz mikrośrodowisko guza.
Cechy mikrośrodowiska guza (TME) zapobiegają rekrutacji limfocytów T do guza. Sposoby obejmują nitrację chemokiny CCL 2 , która wyłapuje komórki T w zrębie . Unaczynienie guzów umożliwia korzystnie rekrutują inne komórki układu odpornościowego na komórki T, częściowo przez komórki śródbłonka (EC), swoistej wobec ekspresji FasL , ET B R i B7H3. Komórki mielomonocytowe i nowotworowe mogą zwiększać ekspresję PD-L1 , częściowo napędzaną stanami niedotlenienia i wytwarzaniem cytokin, takich jak IFNβ. Nieprawidłową metabolit produkcji w TME, takich jak regulacja szlaku przez IDO może wpływać na funkcje komórki T bezpośrednio i pośrednio przez komórki, takie jak T reg komórek. Komórki CD8 mogą być tłumione przez regulację fenotypów TAM przez komórki B. Fibroblasty związane z rakiem (CAF) pełnią wiele funkcji TME, częściowo poprzez wychwytywanie limfocytów T za pośrednictwem macierzy zewnątrzkomórkowej (ECM) i wykluczanie limfocytów T regulowane przez CXCL12 .
Przeciwciała terapeutyczne zatwierdzone przez FDA
Pierwszym zatwierdzonym przez FDA terapeutycznym przeciwciałem monoklonalnym był mysi lek przeciw odrzuceniu przeszczepu IgG2a CD3 , OKT3 (zwany również muromonabem), w 1986 roku. Lek ten znalazł zastosowanie u biorców przeszczepów narządów miąższowych, którzy stali się oporni na steroidy . Setki terapii przechodzi badania kliniczne . Większość dotyczy celów immunologicznych i onkologicznych.
Tositumomab – Bexxar – 2003 – CD20
Mogamulizumab – Poteligeo – sierpień 2018 – CCR4
Moksetumomab pasudotok – Lumoxiti – wrzesień 2018 – CD22
Cemiplimab – Libtayo – wrzesień 2018 – PD-1
Polatuzumab wedotyny – Polivy – czerwiec 2019 – CD79B
Niedawno przeciwciała bispecyficzne , nowa klasa przeciwciał terapeutycznych, przyniosły obiecujące wyniki w badaniach klinicznych. W kwietniu 2009 roku w Unii Europejskiej zatwierdzono bispecyficzne przeciwciało katumaksomab .
Ekonomia
Od 2000 roku rynek terapeutyczny przeciwciał monoklonalnych rósł wykładniczo. W 2006 roku „Big 5” terapeutyczne przeciwciała na rynku były bewacizumab , trastuzumab (zarówno onkologia), adalimumab , infliksymab (oba autoimmunologiczne oraz zaburzenia zapalne „AIID”) i rytuksymab (onkologia i AIID) stanowiły 80% przychodów w 2006. W 2007 roku osiem z 20 najlepiej sprzedających się leków biotechnologicznych w USA to terapeutyczne przeciwciała monoklonalne. Ten szybki wzrost zapotrzebowania na produkcję przeciwciał monoklonalnych został dobrze skompensowany przez uprzemysłowienie wytwarzania mAb.
Zobacz też
- Antygen 5T4
- Immunoterapia
- Immunokoniugat
- Nomenklatura przeciwciał monoklonalnych
- Lista przeciwciał monoklonalnych , w tym badanych i wycofanych